Хімічний зв’язок і валентність
ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ
Частина І. ЗАГАЛЬНА ХІМІЯ
Розділ 3. ХІМІЧНИЙ ЗВ’ЯЗОК
§ 3.10. Хімічний зв’язок і валентність
Валентність атома (елемента) також належить до основних понять хімії. Вона характеризує здатність атомів елементів до утворення хімічних зв’язків. Раніше її визначали як число атомів одновалентного елемента, з яким сполучається один атом даного елемента. Так, у хлоридній кислоті НСl хлор одновалентний, у воді Н2О оксиген двовалентний, в аміаку NH3 нітроген тривалентний,
Зрозуміти фізичний зміст валентності й структурних формул допомогло вчення про будову атомів і хімічний зв’язок. Атоми елементів здатні віддавати, приєднувати електрони або утворювати спільні електронні пари. Електрони, що беруть участь в утворенні хімічних зв’язків між атомами, називаються валентними. Це найслабкіше сполучені електрони.
У хімічних елементів загальне число валентних електронів в атомі, як правило, дорівнює номеру групи періодичної
До валентних належать насамперед електрони зовнішніх незавершених рівнів. Однак валентними можуть бути й електрони другого ззовні рівня (наприклад, у d-елементів), а також електрони третього ззовні рівня (наприклад, у f-елементів).
Із розвитком учення про хімічний зв’язок змінювалось і саме поняття валентності. Останнім часом валентність визначається як число хімічних зв’язків, якими даний атом з’єднаний з іншими.
Число ж зв’язків, які може утворювати атом, дорівнює числу його неспарених електронів. І валентність атома елемента в найпростіших випадках визначається числом неспарених електронів у ньому, що йдуть на утворення спільних електронних пар. При цьому не враховується полярність зв’язків, що утворились, а тому валентність не має знака. Слід підкреслити, що валентність, яка визначається як число зв’язків, не може бути ні від’ємною, ні нульовою. Розглянемо це положення на прикладах азоту N2, гідразину N2H4, аміаку NH3, іона амонію NH4 й нітратної кислоти HNO3. Схема розподілу електронів по квантових комірках атома нітрогену подана в § 2.7. З неї легко дійти висновку, що, оскільки нітроген має три неспарених електрони, він може утворювати три хімічних зв’язки і його валентність дорівнює трьом. Позначивши кожну електронну пару ковалентного зв’язку рискою, одержимо структурні формули:
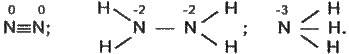
У всіх цих сполуках нітроген тривалентний. Однак ступінь окиснення нітрогену різний і відповідно дорівнює 0, -2, – З (цифри над символами). В іоні амонію NH4 нітроген чотиривалентний (чотири зв’язки, див. § 3.1), але ступінь окиснення нітрогену дорівнює -3. Під час приєднання протона до молекули NH3 валентність нітрогену збільшилася з 3 до 4, але ступінь окиснення не змінився.
Валентність нітрогену в молекулі нітратної кислоти також дорівнює чотирьом. Тепер структурну формулу нітратної кислоти зображують так:
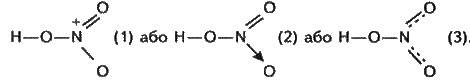
При цьому мається на увазі, що обидва атоми оксигену, сполучені тільки з нітрогеном, рівноцінні; вони перебувають на однаковій відстані від атома нітрогену і несуть кожний по пoловині заряду електрона, тобто четвертий зв’язок нітрогену розділений порівну між двома атомами оксигену. При цьому атоми в молекулі мають стійкі електронні конфігурації зовнішніх рівнів: в оксигену й нітрогену – восьмиелектронні, а у гідрогену – двохелектронні.
Електронну структуру нітратної кислоти послідовно можна вивести так.
1. Атом гідрогену сполучається з атомом оксигену ковалентним зв’язком:
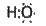
2. За рахунок неспареного електрона атом оксигену утворює ковалентний зв’язок з атомом нітрогену:
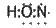
3. Два неспарених електрони атома нітрогену утворюють ковалентний зв’язок з другим атомом оксигену:
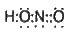
4. Третій атом оксигену, переходячи у збуджений стан, утворює вільну 2р-орбіталь шляхом спарювання неспарених електронів (при збудженні таке спарювання можливе). Взаємодія неподіленої пари електронів атома нітрогену з вільною орбіталлю третього атома оксигену зумовлює утвоpення молекули нітратної кислоти:
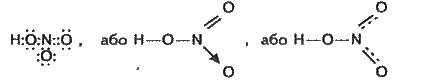
Атом нітрогену нітратної кислоти може віддати один електрон з підрівня 2s одному з атомів оксигену і тоді матиме чотири неспарених електрони, тобто стане чотиривалентним у вигляді N (перша формула).
Нітроген не може бути п’ятивалентним. Вищою межею є таке значення валентності, яке дорівнює числу можливих орбіталей (квантових комірок) на зовнішньому рівні атома. В атомів елементів II періоду, куди входить і нітроген, на зовнішньому рівні є чотири орбіталі: одна s – і три р-орбіталі. Отже, максимальне число ковалентних зв’язків (у тому числі й утворених за донорно-акцепторним механізмом) 4. Із збільшенням номера періоду збільшується число зв’язків, утворених атомом, тобто збілшується валентність елементів. Однак ступінь окиснення атома нітрогену в нітратній кислоті дорівнює +5.
Розглянемо ще один приклад визначення валентності атомів. Хімічний зв’язок у молекулі СО дуже міцний (1 071 кДж/моль), а фізичні властивості оксиду карбону(ІІ) подібні до властивостей нітрогену. Це пояснюється утворенням потрійного зв’язку у молекулі СО:
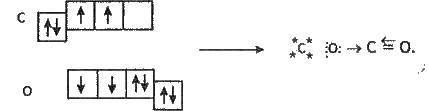
Із цієї схеми видно, що за рахунок двох неспарених електронів атомів карбону і оксигену виникає два ковалентних зв’язки. Третій зв’язок виникає за донорно-акцепторним механізмом за рахунок неподіленої електронної пари атома оксигену (донора) і вільної орбіталі атома карбону (акцептора) (на схемі електрони атома карбону зображені хрестиками). Отже, валентність карбону і оксигену в оксиді карбону(ІІ) дорівнює 3, а ступінь окиснення: карбону +2, оксигену -2.
Порівняємо обидва поняття. Ступінь окиснення – умовне, формальне поняття. Наприклад, ефективний заряд хлору у хлороводні дорівнює -0,18, а в хлориді натрію -0,87, однак ступінь окиснення хлору дорівнює -1 (враховується тільки число приєднаних або відданих електронів). До того ж далеко не всі речовини складаються з іонів (див. означення ступеня окиснення).
Здебільшого ступінь окиснення атома елемента не збігається з числом зв’язків, які він утворює, тобто не дорівнює валентності даного елемента. Особливо наочно це простежується на прикладі органічних сполук. Відомо, що в органічних сполуках валентність атома карбону дорівнює 4 (утворює чотири зв’язки), однак ступінь окиснення атома карбону, як легко підрахувати, у метані СН4 дорівнює – А, у метанолі СН3ОН -2, у формальдегіді СН2О 0, в мурашиній кислоті НСООН +2, в СО2 +4.
Валентність вимірюється тільки числом ковалентних хімічних зв’язків, в тому числі і тих, що виникли за донорно – акцепторним механізмом. Не можна говорити про валентність атомів у сполуках, у яких немає ковалентних зв’язків, слід говорити про ступінь окиснення. У неорганічній хімії в багатьох випадках валентність атома втрачає визначеність: її числова величина залежить від знання хімічної будови сполуки.
За формулами більшості неорганічних сполук можна судити лише про ступінь окиснення елементів, а не про їх валентність. Тому в неогранічній хімії віддають перевагу поняттю ступеня окиснення, а в органічній – валентності (валентність – основне поняття теорії будови органічних сполук О. М. Бутлерова). Це виправдано тим, що більшість неорганічних сполук мають немолекулярну будову, а більшість органічних – молекулярну. І не можна ці два поняття ототожнювати, навіть якщо вони чисельно збігаються.
