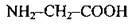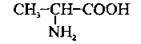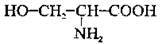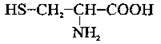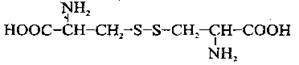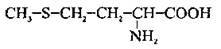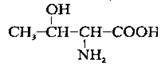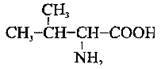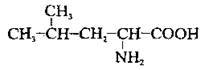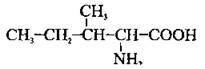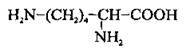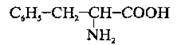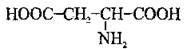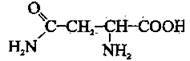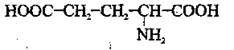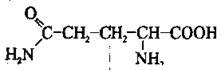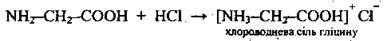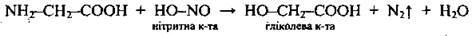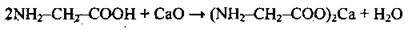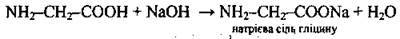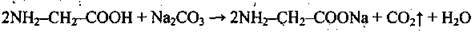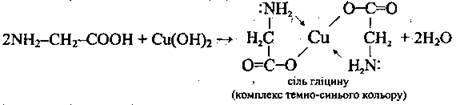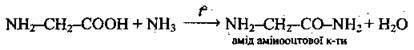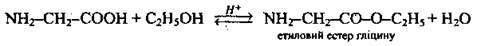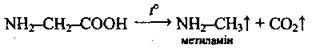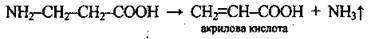Амінокислоти – Нітрогеновмісні органічні сполуки
ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання
РОЗДІЛ III. ОРГАНІЧНА ХІМІЯ
13. Нітрогеновмісні органічні сполуки
13.3. Амінокислоти
Амінокислоти – це органічні сполуки, що містять карбоксильну – СООН та аміногрупу – NH2. Амінокислоти, як і органічні сполуки інших класів, утворюють гомологічні ряди, аналогічні до гомологічних рядів насичених карбонових кислот.
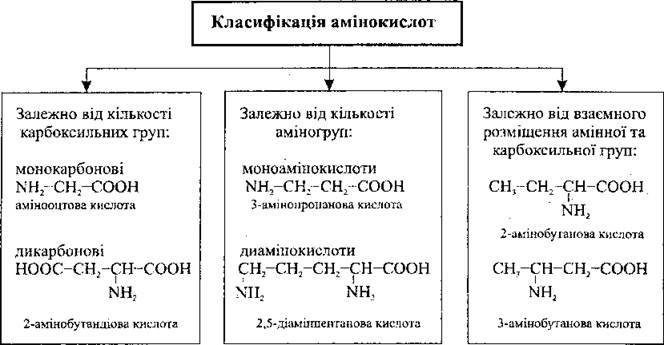
Крім зазначених критеріїв, амінокислоти вирізняються:
А) будовою карбонового ланцюга:
– розгалужені,
– насичені, ненасичені;
– ациклічні, циклічні, ароматичні;
Б) наявністю і розміщенням галогенів та інших характеристичних груп (гідроксильної – ОН, сульфанільної-SH, метилсульфанільної – CH3S, дисульфідної – S-S-, амідної (пептидної) 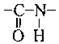 Тощо);
Тощо);
В) співвідношенням кількості карбоксильних та аміногруп (які визначають pH речовини):
– кислі (кількість карбоксильних більша за кількість аміногруп);
– нейтральні (кількість карбоксильних дорівнює кількості аміногруп);
– основні (кількість карбоксильних менша за кількість аміногруп);
Г) полярністю
Д) замінністю для людського організму (замінні, незамінні) тощо.
Номенклатура найпростіших ациклічних амінокислот, які мають по одній карбоксильній та аміногрупі, допускає використання як систематичних, так і традиційних назв з позначенням локантів буквами грецького алфавіту α, β, γ, δ, ε тощо. Слід мати на увазі, що при цьому перелік локантів починають з найближчого до карбоксильної групи атома Карбону:

Біполярна будова молекули амінокислоти
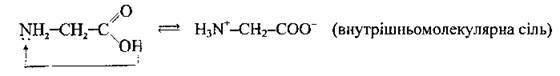
Молекули амінокислот існують у вигляді біполярних іонів (цвіттер-іонів). Біполярний іон – це своєрідна внутрішньо-молекулярна сіль, яка утворюється внаслідок переходу протона (Н+) від карбоксильної до аміногрупи. Ось чому індикатор фіксує нейтральне середовище в розчинах нейтральних амінокислот.
Найбільше значення мають а-амінокислоти. їхня загальна формула має такий вигляд:
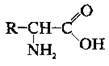
Усі α-амінокислоти (крім найпростішого гліцину) мають асиметричний атом Карбону, тому їм, як і багатьом іншим органічним речовинам, властива оптична ізомерія. Усі амінокислоти, синтезовані живими організмами, – це L-амінокислоти. Із часом в організмі відбувається повільна рацемація – вирівнювання концентрацій L – та D-форм у розчині; у цьому разі – перетворення L-форми на D-форму.
Для 20 білкових (протеїногенних) α-амінокислот у біохімії широко використовують історичні назви:
Назва | ||
Структурна формула | Історична (міжнародна скорочена) | Систематична |
| Гліцин (Gly) | Аміноетанова кислота |
| Аланін (Ala) | 2-амінопропанова кислота |
| Серин (Ser) | 2-аміно-3-гідроксипропанова кислота |
| Цистеїн (Cys) | 2-аміно-3-сульфанілпропанова кислота |
| Цистин | 2-аміно-3- пропанова кислота |
| Метіонін (Met) | 2-аміно-4-(метилсульфаніл)бутанова кислота |
| Треонін (Тге) | 2-аміно-3-гідроксибутанова кислота |
| Валін (Val) | 2-аміно-З – метилбутанова кислота |
| Лейцин (Leu) | 2-аміно-4-метилпентанова кислота |
| Ізолейцин (Не) | 2-аміно-3-метилпентанова кислота |
| Лізин (Lys) | 2,6-діаміногексанова кислота |
| Фенілаланін (Phe) | 2-аміно-3-фенілпропанова кислота |
| Аспарагінова кислота (Asp) | 2-амінобутандіова кислота |
| Аспарагін (Asn) | 2,4-діаміно-4-оксобутанова кислота |
| Глутамінова кислота (Glu) | 2-амінопентандіова кислота |
| Глутамін (Gin) | 2,5-діаміно-5-оксобутанова кислота |
Десять амінокислот (триптофан, лейцин, ізолейцин, лізин, метіонін, фенілаланін, треонін, валін, аргінін, гістидин) належать до незамінних. їх людина одержує винятково з їжею, вони не синтезуються в організмі людини (для кожного виду тварин існує свій список незамінних амінокислот). Деякі замінні амінокислоти організм виробляє недостатньо, отже, їхній синтез також повинен доповнюватись надходженням зовні.
Фізичні властивості амінокислот
Амінокислоти – це безбарвні кристалічні речовини, добре розчинні у воді, гірше – в органічних розчинниках. Мають високі температури плавлення. Одні амінокислоти не мають смаку, інші солодкі на смак (гліцин) або гіркі.
Хімічні властивості амінокислот
Амінокислоти – це типові амфотерні сполуки: реагують і з основами, і з кислотами.
Реакції аміногрупи (основні властивості) | ||
3 кислотами |
| |
3 нітритною кислотою |
| |
Реакції карбоксильної групи (кислотні властивості) | ||
3 основними Оксидами |
| |
3 лугами |
| |
Із солями слабших кислот |
| |
3 гідроксидами важких металічних Елементів |
| |
3 аміаком |
| |
Зі спиртами |
| |
Декарбоксилюваня |
| |
Реакції з одночасною участю карбоксильної та аміногрупи | ||
Дезамінування β-амінокислот |
| |
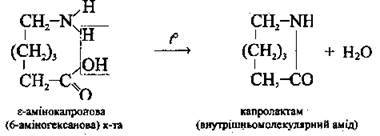
Утворення лактамів |
| Полімеризацією капролактаму отримують! капрон (перлон, найлон-6) |
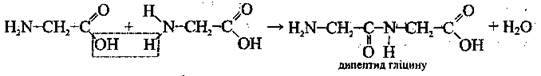
Утворення пептидів |
|
Реакція утворення пептидів (ди-, три-, тетра-, поліпептидів) є найважливішою природною властивістю амінокислот. Зв’язок між залишками амінокислот називають пептид ним, а групу атомів 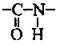 – пептидною, або амідною. Поліпептидний ланцюг є основою будови білка.
– пептидною, або амідною. Поліпептидний ланцюг є основою будови білка.
Добування амінокислот
1. Гідроліз білків призводить до одержання суміші різних амінокислот, залишки яких входять до складу цього білка. У промислових масштабах гідролізу піддають відходи переважно м’ясної галузі (кров, роги, копита). Гідролізом білків добувають цистеїн, лейцин, ізолейцин.
2. Дія аміаку на солі α-галогенокарбонових кислот:
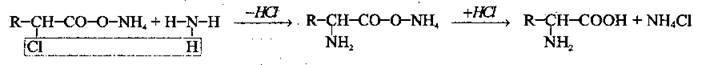
Процес можна відтворити й одним рівнянням:
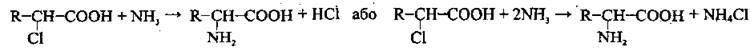
Застосування амінокислот
1. Синтез капрону (поліаміду), з якого виготовляють надзвичайно міцне й еластичне волокно і тканину, плівку, електроізолятори, деталі механізмів тощо.
2. Амінокислоти використовують у медичній практиці: 6-аміногексанову (ε-амінокапронову) кислоту застосовують як кровоспинний засіб, γ-аміномасляну кислоту (ГАМК) – як транквілізатор.
3. Деякі синтетичні амінокислоти використовують для підгодівлі тварин.