Кальцій – ДЕЯКІ ПРЕДСТАВНИКИ МЕТАЛІВ
Хімія підготовка до ЗНО та ДПА
Комплексне видання
ЧАСТИНА І
ЗАГАЛЬНА ХІМІЯ
ДЕЯКІ ПРЕДСТАВНИКИ МЕТАЛІВ
Кальцій
Характеристика хімічного елемента
Кальцій перебуває в головній підгрупі II групи, належить до лужноземельних металів разом з Барієм та Стронцієм. У зовнішній оболонці він має два електрони й може легко віддавати їх, утворюючи іони зі стійкими конфігураціями інертних газів.
Поширеність у природі
Кальцій має велику хімічну активність, тому зустрічається в природі тільки у вигляді сполук. Найважливіші
Фізичні властивості
Кальцій – метал сріблясто-білого кольору, дуже легкий, як і лужні метали, але значно твердіший за них і має більш високу температуру плавлення (+851 °С). Кальцій зберігають під шаром гасу.
Добування
Кальцій добувають шляхом електролізу його розплавленого хлориду.
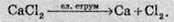
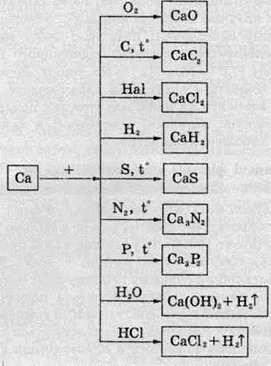
Хімічні властивості
Застосування
Найважливішою сполукою Кальцію є його карбонат СаС03. Він являє собою основну складову




 (1 votes, average: 5.00 out of 5)
(1 votes, average: 5.00 out of 5)Related posts:
- Кальцій. Кальцій гідроксид і кальцій оксид – Метали Хімія Неорганічна хімія Метали Кальцій. Кальцій гідроксид і кальцій оксид Кальцій Кальцій Розташований у IIА групі (II групі, головній підгрупі), 4 періоді Періодичної системи. Він належить до лужноземельних металів. Електронна конфігурація атома Кальцію: На зовнішньому енергетичному рівні розміщені два електрони; ступінь окиснення Кальцію в сполуках +2. У вільному вигляді Кальцій у природі не зустрічається, поширений […]...
- Алюміній – ДЕЯКІ ПРЕДСТАВНИКИ МЕТАЛІВ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ДЕЯКІ ПРЕДСТАВНИКИ МЕТАЛІВ Алюміній Характеристика хімічного елемента Алюміній перебуває в головній підгрупі III групи, належить до рідкісноземельних металів. На його зовнішньому електронному шарі міститься три електрони, які він здатний віддавати. Порівнюючи Алюміній з іншими елементами цієї підгрупи, можна відзначити неметалічність Бору, який стоїть […]...
- Загальна характеристика лужних металів – ДЕЯКІ ПРЕДСТАВНИКИ МЕТАЛІВ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ДЕЯКІ ПРЕДСТАВНИКИ МЕТАЛІВ Загальна характеристика Лужних металів Будова атомів лужних металів У зовнішньому електронному шарі атоми лужних металів мають по одному електрону. У передзовнішньому електронному шарі в атома Літію 2 електрони, а в атомів інших металів по 8 електронів. Однакова будова не тільки […]...
- Натрій і Калій – ДЕЯКІ ПРЕДСТАВНИКИ МЕТАЛІВ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ДЕЯКІ ПРЕДСТАВНИКИ МЕТАЛІВ Натрій і Калій Поширеність у природі Зі сполук лужних металів широко розповсюджені в природі лише сполуки Натрію й Калію. У вигляді простих речовин у природі вони не зустрічаються, тому що занадто активні. Найважливішими природними сполуками Натрію й Калію є: натрій […]...
- Кальцій – МЕТАЛИ ГОЛОВНИХ ПІДГРУП ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 13. МЕТАЛИ ГОЛОВНИХ ПІДГРУП § 13.6. Кальцій Поширення у природі. Кальцій належить до поширених елементів. Загальний вміст його в земній корі становить 3,6 %. У природі найбільш розповсюджені такі сполуки кальцію: мінерал кальцит СаСО3 (з нього утворені масиви вапняку, мармуру і […]...
- Ферум – ДЕЯКІ ПРЕДСТАВНИКИ МЕТАЛІВ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ДЕЯКІ ПРЕДСТАВНИКИ МЕТАЛІВ Ферум Властивості хімічного елемента Ферум належить до металічних елементів. За будовою електронної оболонки його відносять до d-елементів, тому що в нього відбувається заповнення електронами d-підрівня. Здебільшого Ферум виявляє ступінь окиснення +2 (за рахунок двох електронів зовнішнього рівня) або +3 (віддаючи […]...
- Кальцій – Металічні елементи головної підгрупи II групи ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 8. Металічні елементи та їхні сполуки. Метали 8.3. Металічні елементи головної підгрупи II групи1 8.3.5. Кальцій Кальцій – 20-й елемент періодичної таблиці, заряд ядра – +20. Хімічний символ – Са. Відносна атомна маса – 40. Утворює просту речовину – сріблясто-білий метал кальцій. Виявляє […]...
- Кальцій оксид – Металічні елементи головної підгрупи II групи ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 8. Металічні елементи та їхні сполуки. Метали 8.3. Металічні елементи головної підгрупи II групи1 8.3.6. Кальцій оксид Кальцій оксид СаО має технічні назви палене вапно, негашене вапно. Кальцій оксид – сполука з яскраво вираженими основними властивостями. Добування кальцій оксиду У лабораторії: А) окисненням […]...
- Натрій і Калій як представники лужних металів – Метали Хімія Неорганічна хімія Метали Натрій і Калій як представники лужних металів Лужні метали Розміщені в IА групі (у I групі головної підгрупи) Періодичної системи. На зовнішньому енергетичному рівні у лужних металів розміщений один неспарений електрон, який легко віддається окисникам. Ступінь окиснення лужних металів у сполуках дорівнює +1. Електронна конфігурація атома Натрію: Електронна конфігурація атома Калію: […]...
- Кальцій гідроксид – Металічні елементи головної підгрупи II групи ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 8. Металічні елементи та їхні сполуки. Метали 8.3. Металічні елементи головної підгрупи II групи1 8.3.7. Кальцій гідроксид Кальцій гідроксид (Са(ОН)2). Насичений водний розчин кальцій гідроксиду називають вапняною водою, а білу суспензію кальцій гідроксиду – вапняним молоком. Одержання кальцій гідроксиду У лабораторії Са(ОН)2 одержують […]...
- Тема 20. Кальцій Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА ІІ ЗАВДАННЯ ДЛЯ ПЕРЕВІРКИ ЗНАНЬ НЕОРГАНІЧНА ХІМІЯ Тема 20. Кальцій Серед чотирьох наведених варіантів відповідей виберіть одну правильну 1. Позначте символ хімічного елемента Кальцій: A. К; Б. Ка; B. Са; Г. С. 2. Позначте число протонів, що містить ядро атома Кальцію: A. 20; Б. 30; B. […]...
- КАЛЬЦІЙ – ХІМІЯ МЕТАЛІЧНИХ ЕЛЕМЕНТІВ Хімія – універсальний довідник ХІМІЯ МЕТАЛІЧНИХ ЕЛЕМЕНТІВ КАЛЬЦІЙ Одна з найважливіших сполук кальцію – оксид СаО (негашене вапно). Його одержують розкладом вапняку (що складається, в основному, з карбонату кальцію) при високій (біля 1000 °С) температурі: Це – оксид лужноземельного металу, тому він легко взаємодіє з водою, утворюючи луг – гідроксид кальцію: Технічна назва Са(ОН)2 – […]...
- Солі кальцію – Металічні елементи головної підгрупи II групи ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 8. Металічні елементи та їхні сполуки. Метали 8.3. Металічні елементи головної підгрупи II групи1 8.3.8. Солі кальцію Якісне виявлення: іони Са2+ забарвлюють полум’я газового пальника в цегляно-червоний колір. Карбонат амонію осаджує з розчинів солей Кальцію білий осад СаСО3. Гіпс CaSО4 · 2Н2О при […]...
- Кальцій. Кальцій оксид і гідроксид. Солі Кальцію. Поняття про твердість води. Використання найважливіших сполук Кальцію ІІ семестр Тема 2. МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ (13 годин) УРОК 29 Тема уроку. Кальцій. Кальцій оксид і гідроксид. Солі Кальцію. Поняття про твердість води. Використання найважливіших сполук Кальцію Цілі уроку: розширити знання учнів про метали на прикладі лужноземельних металів; вивчити властивості лужноземельних металів, їхніх сполук, способи одержання й застосування на прикладі Кальцію; продовжити […]...
- Загальні способи добування металів – ЗАГАЛЬНА ХАРАКТЕРИСТИКА МЕТАЛІВ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ЗАГАЛЬНА ХАРАКТЕРИСТИКА МЕТАЛІВ Загальні способи добування металів Лабораторні методи добування А) відновлення оксидів металів воднем; таким способом зазвичай добувають не дуже активні метали, які не взаємодіють із воднем: Б) розкладання оксидів важких металів: В) витіснення металів з їхніх солей більш активними металами: Добування […]...
- Загальні фізичні властивості металів – ЗАГАЛЬНА ХАРАКТЕРИСТИКА МЕТАЛІВ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ЗАГАЛЬНА ХАРАКТЕРИСТИКА МЕТАЛІВ Загальні фізичні властивості металів Металічні елементи займають в основному ліву нижню частину Періодичної системи хімічних елементів Д, І. Менделєєва. До металічних елементів належать ті елементи, в чиїх атомах на зовнішньому електронному рівні перебуває невелике (від одного до чотирьох) число електронів, […]...
- Загальні хімічні властивості металів – ЗАГАЛЬНА ХАРАКТЕРИСТИКА МЕТАЛІВ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ЗАГАЛЬНА ХАРАКТЕРИСТИКА МЕТАЛІВ Загальні хімічні властивості металів В атомах металів на зовнішній електронній оболонці утримується невелике число електронів. Ці електрони порівняно легко можуть відриватися від атомів. Така особливість металів є причиною не тільки їхніх фізичних, але й хімічних властивостей. Виходячи з того, що […]...
- Фізичні властивості металів – Метали Хімія Неорганічна хімія Метали Фізичні властивості металів Пластичність. Механічна дія на кристал із металічним зв’язком викликає зсув шарів атомів, але завдяки переміщенню валентних електронів по всьому зразку металу розриву зв’язків не відбувається. Найпластичніший метал – золото. Марганець і бісмут – крихкі метали. Металічний блиск, непрозорість. Вільні електрони взаємодіють із квантами світла, які падають на метал. […]...
- Положення металів у періодичній системі елементів Д. І. Менделєєва – ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 12. ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ § 12.1. Положення металів у періодичній системі елементів Д. І. Менделєєва Якщо в періодичній системі елементів Д. І. Менделєєва провести діагональ від берилію до астату, то праворуч угорі від діагоналі будуть елементи-неметали (виключаючи елементи побічних підгруп), а […]...
- Ряд електрохімічних потенціалів металів ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 6. Суміші речовин. Розчини 6.12. Ряд електрохімічних потенціалів металів Порівняльну активність металів в окисно-відновних реакціях, які відбуваються у водних розчинах речовин, характеризує електрохімічний ряд напруг металів (ряд електрохімічних потенціалів, витискувальний ряд, ряд активності). Електрохімічний ряд напруг – це розташування металів у послідовності збільшення […]...
- Солі карбонатної кислоти – ПІДГРУПА КАРБОНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 11. ПІДГРУПА КАРБОНУ § 11.4. Солі карбонатної кислоти Карбонатна кислота утворює два ряди солей: середні – карбонати і кислі – гідрокарбонати. Вони виявляють загальні властивості солей. Карбонати і гідрокарбонати лужних металів та амонію добре розчиняються у воді. Солі карбонатної кислоти – […]...
- Магній і Кальцій РОЗДІЛ 3 МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХ СПОЛУКИ ХІМІЧНІ ЕЛЕМЕНТИ ІА – ІІІА ГРУП § 62. Магній і Кальцій Усвідомлення змісту цього параграфа дає змогу: Характеризувати фізичні та хімічні властивості, способи добування, застосування магнію і кальцію; Складати рівняння, схеми електронного балансу відповідних хімічних реакцій. Фізичні властивості. Магній і Кальцій – сріблясто-білі, пластичні метали (мал. 109), порівняно […]...
- Основні способи добування металів – ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 12. ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ § 12.6. Основні способи добування металів Метали трапляються в природі як у вільному стані (самородні метали), так і, переважно, у вигляді хімічних сполук. У вигляді самородних металів перебувають найменш активні метали. Типовими їх представниками є золото і […]...
- ЗАГАЛЬНІ ФІЗИЧНІ ВЛАСТИВОСТІ МЕТАЛІВ. ПОШИРЕНІСТЬ МЕТАЛІЧНИХ ЕЛЕМЕНТІВ ТА ЇХНІХ СПОЛУК У ПРИРОДІ. МЕТАЛІЧНІ РУДИ. ЗАГАЛЬНІ МЕТОДИ ДОБУВАННЯ МЕТАЛІВ ТЕМА 2. МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ УРОК 2. ЗАГАЛЬНІ ФІЗИЧНІ ВЛАСТИВОСТІ МЕТАЛІВ. ПОШИРЕНІСТЬ МЕТАЛІЧНИХ ЕЛЕМЕНТІВ ТА ЇХНІХ СПОЛУК У ПРИРОДІ. МЕТАЛІЧНІ РУДИ. ЗАГАЛЬНІ МЕТОДИ ДОБУВАННЯ МЕТАЛІВ Цілі: вивчити загальні фізичні властивості металів; поширеність металічних елементів та їхніх сполук у природі; металічні руди й загальні методи добування металів; уміти пояснювати фізичні властивості металів з точки […]...
- Деякі сполуки галогенів – ГАЛОГЕНИ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЯ ЕЛЕМЕНТІВ ГАЛОГЕНИ Деякі сполуки галогенів Оксигеновмісні кислоти Хлору Характеристика оксигеновмісних кислот Хлору Формула кислоти Ступінь окиснення атома Хлору Назва кислоти Назва аніона Сила кислоти Стійкість кислоти HClO +1 Гіпохлоритна Гіпохлорит Дуже слабка Дуже нестійка HClO2 +3 Хлоритна Хлорит Середньої сили Існує тільки […]...
- Фізичні властивості металів – Загальні відомості про металічні елементи та метали ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 8. Металічні елементи та їхні сполуки. Метали 8.1. Загальні відомості про металічні елементи та метали 8.1.2. Фізичні властивості металів Особливості металічного зв’язку і кристалічних граток зумовлюють загальні фізичні властивості різних металів. 1. Агрегатний стан металів твердий (крім ртуті й, умовно, францію1). Температура плавлення […]...
- Фізичні властивості металів – ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 12. ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ § 12.2. Фізичні властивості металів Механічна дія на кристал з ковалентним зв’язком спричиняє зміщення окремих шарів атомів, внаслідок чого зв’язки розриваються і кристал руйнується (рис. 12.1, а). Така сама дія на кристал з металічним зв’язком також спричиняє […]...
- Хімічні властивості металів – ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 12. ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ § 12.3. Хімічні властивості металів Атоми металів порівняно легко віддають валентні електрони і перетворюються на позитивно заряджені іони. Тому метали є відновниками. В цьому, власне, і полягає їх головна і найзагальніша хімічна властивість. Рис. 12.2. Криві температур […]...
- ХІМІЧНІ ВЛАСТИВОСТІ ЛУЖНИХ МЕТАЛІВ – ЛУЖНІ МЕТАЛИ Хімія – універсальний довідник ЛУЖНІ МЕТАЛИ ХІМІЧНІ ВЛАСТИВОСТІ ЛУЖНИХ МЕТАЛІВ Лужні метали – хімічно дуже активні речовини. На повітрі вони швидко реагують з його складовими частинами. В результаті утвориться суміш речовин, що покривають поверхню металу товстим пухким шаром, тому лужні метали зберігають у рідинах, що не реагують з ними, наприклад, у гасі. Лужні метали бурхливо […]...
- Положення елементів-металів у періодичній системі, особливості будови атомів. Металічний зв’язок. Фізичні властивості металів ІІ семестр Тема 2. МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ (13 годин) УРОК 23 Тема уроку. Положення елементів-металів у періодичній системі, особливості будови атомів. Металічний зв’язок. Фізичні властивості металів Цілі уроку: поглибити знання учнів про металеві елементи, їх положення в періодичній системі, особливості будови атомів, будови речовини; ознайомити з типом хімічного зв’язку, властивим металам, – металічним […]...
- ЗАГАЛЬНІ ХІМІЧНІ ВЛАСТИВОСТІ МЕТАЛІВ. КОРОЗІЯ МЕТАЛІВ ТА ЇХ ЗАХИСТ ВІД КОРОЗІЇ ТЕМА 2. МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ УРОК 3. ЗАГАЛЬНІ ХІМІЧНІ ВЛАСТИВОСТІ МЕТАЛІВ. КОРОЗІЯ МЕТАЛІВ ТА ЇХ ЗАХИСТ ВІД КОРОЗІЇ Цілі: вивчити загальні хімічні властивості металів; мати уявлення про корозію металів і способи захисту металів від корозії; вміти складати рівняння хімічних реакцій, що ілюструють хімічні властивості металів і суть корозії металів, складати рівняння реакцій з […]...
- Солі кальцію – МЕТАЛИ ГОЛОВНИХ ПІДГРУП ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 13. МЕТАЛИ ГОЛОВНИХ ПІДГРУП § 13.8. Солі кальцію Карбонат кальцію широко розповсюджений в природі у вигляді гірської породи – вапняку. Багато гірських хребтів складаються з вапняку і крейди. Часто трапляється і мармур, що утворився у давні геологічні епохи з вапняку і […]...
- ПОРІВНЯННЯ ХІМІЧНОЇ АКТИВНОСТІ МЕТАЛІВ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС РЕАКЦІЇ ЗІ ЗМІНОЮ СТУПЕНІВ ОКИСНЕННЯ ЕЛЕМЕНТІВ ПОРІВНЯННЯ ХІМІЧНОЇ АКТИВНОСТІ МЕТАЛІВ Електрохімічний ряд напруг металів Хімічна активність металів у водних розчинах визначається його енергією атомізації ΔHатоміз, іонізації його атомів ΔHйоніз і гідратації його іонів ΔHгідрат: Наведені розрахунки показують, що за зменшенням хімічної активності у водних розчинах меркурій, водень, нікель розташовуються […]...
- РЯД АКТИВНОСТІ МЕТАЛІВ – ХІМІЯ МЕТАЛІЧНИХ ЕЛЕМЕНТІВ Хімія – універсальний довідник ХІМІЯ МЕТАЛІЧНИХ ЕЛЕМЕНТІВ РЯД АКТИВНОСТІ МЕТАЛІВ За числовим значенням своєї відновної здатності всі метали можуть бути розташовані в ряд, який називається р я д о м активності мета л і в. Його називають ще електрохімічним рядом, підкреслюючи тим самим, що, вступаючи в хімічну реакцію, метал віддає електрони – носії електричного струму. […]...
- Метали та сплави в техніці – ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 12. ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ § 12.4. Метали та сплави в техніці Сплавами називаються системи, що складаються з двох і більше металів, а також металів і неметалів. Властивості сплавів дуже різноманітні і відрізняються від властивостей вихідних компонентів. Так, наприклад, сплав, що складається […]...
- Ряд електроактивності металів ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання ДОДАТКИ Додаток 4. Ряд електроактивності металів...
- Оксид і гідроксид кальцію – МЕТАЛИ ГОЛОВНИХ ПІДГРУП ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 13. МЕТАЛИ ГОЛОВНИХ ПІДГРУП § 13.7. Оксид і гідроксид кальцію Оксид кальцію (технічні назви: негашене вапно, палене вапно, кипілка) – порошок білого кольору. У промисловості його добувають випалюванням вапняку, крейди чи інших карбонатних порід: СаСО3 = СаО + СО3; ∆Н° = […]...
- БУДОВА АТОМІВ ЛУЖНИХ МЕТАЛІВ – ЛУЖНІ МЕТАЛИ Хімія – універсальний довідник ЛУЖНІ МЕТАЛИ Лужними металами називаються елементи ІА групи. Якщо галогени є типовими, найяскравіше вираженими неметалами, то елементи ІА групи – це типові метали. БУДОВА АТОМІВ ЛУЖНИХ МЕТАЛІВ З елемента ІА групи розпочинається кожен період у таблиці Д. І. Менделєєва. Це означає, що саме в атомах цих елементів розпочинається заповнення наступного енергетичного […]...
- Корозія металів – ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 12. ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ § 12.7. Корозія металів Під час експлуатації виробів з металів та їх сплавів доводиться стикатися з явищем руйнування їх під дією навко яишнього середовища. Руйнування металів і сплавів внаслідок взаємодії їх з навколишнім середовищем називається корозією. Корозія […]...
- Загальні способи добування металів. Електроліз розплавів солей і лугів – Метали Хімія Неорганічна хімія Метали Загальні способи добування металів. Електроліз розплавів солей і лугів Металургія – це галузь промисловості, яка займається видобуванням металів із руд. Електроліз – окисно-відновний процес, що відбувається на електродах під час проходження електричного струму через розплав або розчин електроліту. Якщо в розплав електроліту, наприклад натрій хлориду, занурити інертні електроди й пропускати постійний […]...