Карбон – Елементи IV групи
ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання
РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ
9. Неметалічні елементи та їхні сполуки. Неметали
9.5. Елементи IV Групи
9.5.2. Карбон
Карбон – елемент 2-го періоду, IV групи. 6-й елемент періодичної таблиці, заряд ядра – +6. Хімічний символ – С. Відносна атомна маса – 12, молярна маса – 12 г/моль.
Природний Карбон складається з двох стабільних ізотопів – 12С (98,93 %) і 13С (1,07%)- та одного радіоактивного – 14С (10-10 %), який утворюється в атмосфері (на висоті 12-15 км). На утворенні
Електронна формула атома Карбону – 1s22s22p2. У сполуках виявляє валентності II, IV (у більшості сполук), а в молекулі чадного газу СО Карбон є тривалентним (за рахунок донорно-акцепторного зв’язку):
Ступені окиснення | -4 | -3 | -2 | -1 | 0 | +2 | +4 |
Приклади сполук | Al4C3CH4 | C2H6 | C2H4 | С2Н2 | C | СО | CO2, K2CO3 |
Поширеність у природі
Карбон у природі існує у вільному стані та у вигляді сполук.
Карбон – основна складова частина антрациту (94-97 %), кам‘яного (76-95 %) і бурого вугілля (64-80 %), горючих сланців (56-78 %), нафти (82-87 %), горючих природних газів (до 99 % метану), торфу (53-56 %), бітумів тощо.
Сучасна атмосфера містить 0,03 % (за об’ємом) вуглекислого газу СO2, а у Світовому океані – у 60 разів більше (у розчиненому стані й у вигляді карбонатів і гідрогенкарбонатів, що зумовлює тимчасову твердість води). Атмосфера Венери складається на 97 % з карбон(ІV) оксиду.
Цей елемент, завдяки здатності утворювати хімічні зв’язки різного типу (одинарні, подвійні, потрійні) і стабільності його сполук, становить основу живої природи: атоми Карбону входять до складу всіх органічних речовин. Карбон становить близько 18 % маси рослин і тварин. В організмі людини масова частка Карбону – 21 % (становить % маси м’язів і Уз маси кісткової тканини). Карбонати Кальцію і Магнію є основою зовнішнього і внутрішнього скелета багатьох видів тварин.
Фізичні властивості простих речовин
Існує кілька простих речовин, які складаються з атомів Карбону. їхня загальна хімічна назва – вуглець.
Карбон має властивість утворювати ланцюги, цикли, сітки, складні просторові фігури. Завдяки цьому Карбон – елемент з найбільшою кількістю алотропічних модифікацій: алмаз, лондедейліт, графіт, карбін, фулерен, нанотрубка і нановолокно, нанопіна тощо.
Алмаз – прозорий безбарвний (іноді з жовтим, коричневим, червоним, зеленим, синім відтінком, навіть до чорноти; штучний алмаз має чорний колір) дуже твердий кристал. Алмаз – найтвердіша3 природна речовина (до 1966 p.). Виняткова твердість алмазу пояснюється будовою його кристалічних граток: усі 4 електрони кожного атома Карбону в алмазі утворюють міцні ковалентні зв’язки з іншими атомами Карбону. Комірка атомних кристалічних граток має тетраедричну структуру. Відстані між атомами Карбону однакові. Алмаз не проводить електричного струму, оскільки в його кристалічних гратках немає вільних електронів. Огранені та відшліфовані кристали алмазу називають діамантами. За температури 1000 °С, якщо немає кисню, поступово перетворюється на графіт.
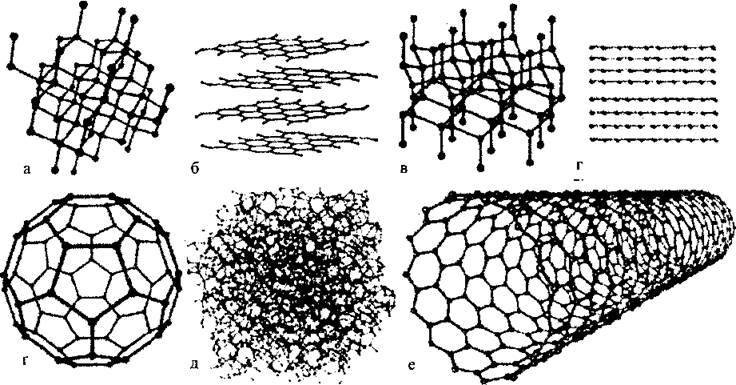
На малюнку зображено кристалічні структури алотропних модифікацій Карбону: а) алмазу, б) графіту, в) лонсдейліту, г) карбіну, т) фулерену С60, д) аморфного вуглецю, е) нанотрубки4.
Лонсдейліт (гексагональний алмаз)- алотропічна модифікація Карбону, відкрита 1966 року. Дещо відрізняється будовою від алмазу і на 58 % твердіший за нього (№ 11 за шкалою Мооса).
Графіт – мінерал із класу самородних елементів, темно-сіра кристалічна тугоплавка речовина з металічним блиском, має складну шарувату (лускоподібну) структуру. Зв’язки між атомами Карбону в одному шарі значно міцніші, ніж між атомами в різних шарах. Кожний атом Карбону в кристалічних гратках утворює три міцні ковалентні зв’язки з іншими атомами, які розміщені у тому ж шарі. Четвертий електрон кожного атома Карбону, що не бере участі в утворенні цих зв’язків, залишається вільним і зумовлює електропровідність графіту (напівметал, металоїд). Відстань між шарами значно більша, ніж відстань між атомами Карбону, що розміщуються в одному шарі.
Карбін – дрібнокристалічний порошок чорного кольору, за своїми властивостями подібний до графіту. Природний полімер (трапляється у вигляді мінералу чаоїту) з довгими лінійними молекулами. Ланцюжки з атомів Карбону складаються із фрагментів з подвійним (=С=С=С=С=) або потрійним (-С≡С-С≡С-) зв’язком. Напівпровідник, провідність збільшується при освітленні.
Карбон може утворювати кластери – структури, складніші за формою, ніж ланцюжки, цикли чи тетраедричний кристал: фулерени, графени, нанотрубки й астралени.
Фулерени були відкриті 1985 року. Молекули цієї речовини можуть складатися із 60, 70, 80, 90, 100 і більше атомів Карбону (С6о, С70, С8о-.-)> мають сферичну форму (нагадують за формою футбольний м’яч). Фулерит-60 – молекулярний кристал, у вузлах його граток розташовані молекули фулерена-60, майже удвічі твердіший за алмаз (№ 12 за шкалою Мооса).
Графен – штучно отримана гексагональна модифікація (2004 р.) з одноатомного шару Карбону. Його міцність на порядок вища за міцність будь-якої відомої науці речовини. Має надзвичайну електропровідність.
Аморфний вуглець – суміш дрібних, безладно розміщених кристалів графіту, з якої складаються технічний вуглець, сажа, кокс, вугілля викопне і деревне.
Технічний вуглець – чорний жирний на дотик порошок. Це продукт, який добувають у промислових умовах при термічному розкладанні вуглеводнів. Сажа утворюється при неконтрольованому згорянні органічних речовин (технологічно шкідливий побічний продукт).
Кокс – продукт коксування (нагрівання до температури 950-1100 °С без доступу повітря) кам’яного вугілля. Містить 96-98 % Карбону.
Деревне вугілля – тверда пориста речовина, продукт нагрівання (піролізу, 450-500 °С) деревини без доступу повітря. Щоб збільшити кількість пор (і відповідно збільшити поверхню поглинання), деревне вугілля обробляють гарячою водяною парою. Отримане в такий спосіб вугілля називають активованим. Залежно від вихідної речовини отримують тонко – (до 2 нм) чи грубо-пористий продукт (2-50 нм і більше). У пори можуть потрапляти молекули різних речовин і там утримуватися: у маленькі пори – малі молекули, у великі – великі молекули.
Здатність однієї речовини утримувати на своїй поверхні атоми, молекули, йони другої речовин називаю! адсорбцією. Речовину (тверду або рідку), яка здатна утримувати на своїй поверхні інші речовини (рідкі або газоподібні), називають адсорбентом.
Хімічні властивості вуглецю
Хімічна активність різних алотропних модифікацій неоднакова. За нормальних умов вуглець малоактивний. Алмаз і графіт можуть реагувати лише з чистим киснем за дуже високої температури. Усі реакції за участі вуглеці є окисно-відновними, у яких Карбон може виявляти властивості як відновника (більш характерні), так і окисника.
Як відновник вуглець реагує з простими речовинами неметалами (киснем, галогенами, сіркою), а також зі складними речовинами (вуглекислим газом, оксидами металічних елементів, водяними парами та кислотами-окисниками):
А) з простими речовинами:
– вуглець горить на повітрі, виділяючи значну кількість теплоти:
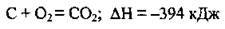
За умови нестачі кисню утворюється чадний газ СО:
2С + О2= 2СО
– сполучається із сіркою, хлором:
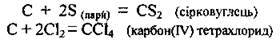
Б) зі складними речовинами:
– з водяними парами (за температури 1200 °С утворюється водяний газ – суміш чадного газу з воднем):
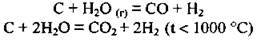
– з оксидами металічних і деяких неметалічних елементів:
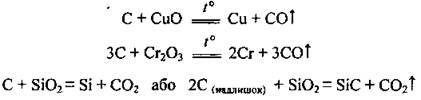
– з кислотами-окисниками:
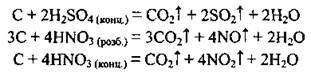
– з іншими речовинами:
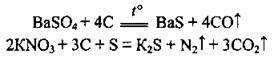
Як окисник:
– при нагріванні взаємодіє з простими речовинами (металами), утворюючи карбіди:
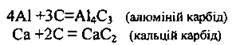
Карбіди розкладаються водою та мінеральними кислотами:
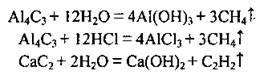
– з деякими неметалами:
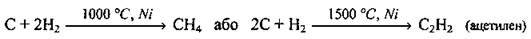
При взаємодії вуглецю із силіцієм утворюється силіцій(ІV) карбід. За твердістю він наближається до алмазу:
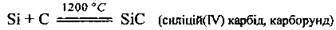
Застосування вуглецю
Алмаз використовують для виготовлення коштовних ювелірних прикрас (діамантів), штучні алмази – у промисловості для виготовлення абразивних та різальних інструментів, при бурінні свердловин.
Графіт застосовують в електротехніці для виготовлення електродів та електричних контактів; з нього виготовляють грифелі для олівців; подрібнений графіт вводять до складу фарб; у суміші з мінеральною олією використовують для виготовлення мастил для машин. Графітові стрижні застосовують як уповільнювач нейтронів в атомних реакторах.
Активоване вугілля використовують як адсорбент у медицині (при отруєннях), у харчовій промисловості, для очищення води, у протигазах.
Технічний вуглець застосовують для виробництва гуми, інших пластичних мас, уводять до складу друкарської фарби, копіювального паперу.
Кокс використовують у металургії як відновник.
Викопне вугілля застосовують в теплоенергетиці, для добування водяного газу (суміші СО та Н2), коксу.
Карбін використовують у фотоелементах.
Дослідження простих речовин Карбону тривають, це одна з найперспективніших галузей хімічної науки (а згодом і техніки).
_______________________________________________________________
1 Запропоновано 1946 р. американським фізико-хіміком Віллардом Ліббі (1908-1980), лауреатом Нобелівської премії з хімії 1960 р. Межа достовірності методу – близько 2000 р.
2 Вапняк, який складається з мушлів відмерлих молюсків, називають ракушняком.
3 Шкалу Мооса (мінералогічну шкалу твердості) запропонував 1811 року німецький мінералог Ф. Моос. За еталони взято е 10 природних мінералів, які розташовано в послідовності збільшення твердості від тальку (1) до алмазу (10).
4 Малюнки із сайтів en. wikipedia. org і him.1september. ru.
