Прості речовини метали й неметали. Оксиген. Кисень, склад його молекули
Тема 2
ПРОСТІ РЕЧОВИНИ МЕТАЛИ Й НЕМЕТАЛИ
Урок 25
Тема. Прості речовини метали й неметали. Оксиген. Кисень, склад його молекули
Цілі: повторити класифікацію речовин; закріпити знання учнів про елементи метали й неметали та прості речовини на прикладі Оксигену й кисню; дати поняття про Оксиген – хімічний елемент і кисень – просту речовину; ознайомити учнів з історією відкриття кисню, його поширенням у природі, фізіологічною дією.
Тип уроку: поглиблення і засвоєння знань.
Форма роботи: розповідь, фронтальна бесіда.
ХІД
I. Організація класу
II. Аналіз тематичного оцінювання з теми “Початкові хімічні поняття”
Учитель аналізує типові помилки, учні проводять роботу над помилками в зошиті. Виставляються оцінки за тему.
III. Актуалізація опорних знань і мотивація навчальної діяльності
Фронтальна бесіда
Навколо нас знаходиться велика кількість хімічних речовин з різними властивостями.
– Чому речовини розрізняються за властивостями? (Тому що мають різний склад)
– На які дві групи поділяються речовини за складом молекул? (На прості та складні)
Згадаймо визначення.
Прості речовини
Складні речовини – це…
– Наведіть приклади простих і складних речовин.
(Учитель записує на дошці у два стовпчики приклади учнів, коригує відповіді.)
– У природі хімічні елементи зустрічаються у вигляді простих речовин чи складних? (І тих і інших)
– А яких речовин більше в природі – простих чи складних? (Складних)
– Чому?
– Прості речовини, у свою чергу, також поділяються на групи за властивостями. Які це групи? (Метали й неметали)
– Відзначимо на дошці серед простих речовин ті, що утворені елементами-неметалами.
– Яких елементів у природі більше – металів чи неметалів? (Металів) Звертаємося до періодичної системи хімічних елементів і згадуємо розташування елементів металів і неметалів у таблиці.
– Які елементи – метали чи неметали – частіше зустрічаються в природі у вигляді простих речовин? Наведіть приклади.
N2, O2, H2, C, Si, S… – неметали.
Ag, Au, Pt – метали.
Порівняймо деякі фізичні властивості елементів металів і неметалів, використовуючи наш досвід і знання. (Заповнюємо таблицю.)
Прості речовини | Метали | Неметали |
1. Поширеність | ||
– у земній корі; | Al – 8,8 %; Na – 2,6 %; Fe – 4,7 %; K – 2,4 %; Ca – 3,4 %; Mg – 2,3 % | O – 47 %; Si – 27,6 % |
– у повітрі; | Домішки | Близько 100 % |
– у воді | У розчинених складних речовинах | У складі молекул води H2O, у розчинних речовинах |
2. Агрегатний стан | Hg, Ga – рідкі, решта – тверді | Газоподібні; рідкі; тверді |
3. Будова речовини | Немолекулярна | Молекулярна, немолекулярна |
4. Прості речовини | Атоми: Cu, Fe, Ag | Атоми й молекули: N2, O2, S, P |
5. Фізичні властивості | – Металевий блиск. – Висока електропровідність. – Теплопровідність. – Пластичність. – Тугоплавкість. – Ковкість | Немає загальних властивостей, характерних для всіх неметалів |
6. Хімічні властивості | Багато в чому подібні, є ряд активності металів | Особливі в кожного неметалу, загальних властивостей мало |
Прості речовини мають для людини важливе значення. Якщо вивчити склад і властивості простих речовин, то можна краще розібратися в будові та властивостях складних речовин.
Вивчення простих речовин ми починаємо з одного з найпоширеніших елементів-неметалів – Оксигену.
IV. Засвоєння нових знань
Розповідь учителя
Ми починаємо вивчати елемент Оксиген. У складі хімічних сполук він розповсюджений на земній поверхні так, як жоден інший елемент. Він становить близько 8/9 масових частин води (88,8 % масових). У твердому зовнішньому шарі Землі на частку Оксигену припадає 47 % масових, або 58 % за кількістю атомів. У повітрі поряд з азотом і незначною кількістю інших домішок міститься 23,15 % масових, або 21 % об’ємних.
Оксиген входить до складу таких біологічно важливих речовин, як вода, білки, жири, вуглеводи, нуклеїнові кислоти, до 50-85 % ваги живих і рослинних тканин.
– А яку роль відіграє кисень для людини?
Про роль кисню в природі написані тисячі книг. Усі тварини дихають киснем і в безкисневій атмосфері просто не можуть існувати. Лише деякі мікроорганізми – анаеробні бактерії, живуть без кисню.
Вдихуваний кисень окислює вуглеводи та інші речовини, і в цьому хімічному процесі виділяється та енергія, що витрачається на всі життєві процеси. Весь кисень виник і зберігається на планеті завдяки процесу фотосинтезу.
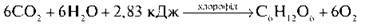
Поговоримо трохи про історію відкриття кисню.
Тривалий час у хімії існувала думка про повітря як про елемент. Світовий пріоритет у відкритті кисню належить китайському вченому Мао-хао (VIII століття), який виявив наявність у повітрі двох газів, один з яких підтримує дихання і горіння.
В Європі це відкриття сталося через 1000 років. Шведський учений Карл Шеєле, учень аптекаря, у вільний від роботи час займався хімічними дослідами з вивчення флогістону – пальної сутності речовини. Він спалював у закритій колбі фосфор, який миттєво згоряв, перетворюючись на “суху фосфорну кислоту” (P2O5). Потім занурював колбу в посудину з водою, і вона на 1/5 заповнювалася водою. Знову і знову вчений повторював дослід, спалюючи різні речовини, й одержував одне й те саме – зникала 1/5 частина повітря. Шеєле припустив, що повітря в колбі вже інше. Щоб перевірити свою гіпотезу, він досліджував повітря, що залишилося в колбі. Повітря виявилося мертвим: у ньому нічого не хотіло горіти, свічки стухали, немов їх задмухувала “невидимка”, розжарене вугілля остигало, палаюча скіпка миттєво гасла. Висновок був тільки один: повітря – неоднорідна речовина, одна частина якого підтримує дихання і горіння.
Після численних дослідів з розкладу селітри (KNO3, NaNO3) Шеєле одержав “вогненне повітря”, в якому скіпка, що ледь жевріла, загорялася яскравим полум’ям. Шеєле повторив дослід зі спалювання фосфору, але у “вогненному повітрі” після згоряння фосфору колба цілком заповнювалася водою.
Утім, таємниця вогню так і залишалася для вченого таємницею, тому що до кінця днів він залишався прихильником теорії “флогістону”.
“Вогненне повітря” було відкрите майже одночасно трьома вченими: К. Шеєле, Дж. Прістлі, А. Лавуазьє.
Англієць Джозеф Прістлі сонячним промінням нагрівав у пробірці меркурій(ІІ) оксид і одержував велику кількість газу, в якому свічка яскраво горіла.
2HgO 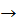 2Hg + O2
2Hg + O2
Першість у відкритті кисню належить Дж. Прістлі. Але з усіх трьох тільки Лавуазьє правильно оцінив істинне значення кисню в природі. Він уперше заявив, що ніякого флогістону не існує. Ця заява викликала бурю в ученому світі. Хіміки так звикли бачити всюди незримий флогістон, що ніяк не могли розстатися з ним. Але проти очевидного встояти важко, і наприкінці XVIII століття флогістон було остаточно вигнано з хімічної науки.
Тож.
Хімічний елемент: О – Оксиген.
Порядковий номер: 8.
Будова атома: +8)) np = 8, ne – = 8, nn = 8.
Відносна атомна маса: 16.
Валентність – II.
Проста речовина: O2 – кисень, O3 – озон.
Відносна молекулярна маса O2: 32.
V. Підбиття підсумків
Сьогодні ми познайомилися з історією відкриття неметалу – кисню, з його поширеністю в природі як простої речовини, так і хімічного елемента в складі складних сполук, з його фізіологічною роллю для живих організмів. А на наступних уроках ми маємо вивчити його фізичні та хімічні властивості.
VI. Домашнє завдання
Прочитати параграф, відповісти на запитання.
Творче завдання. Написати есе про значення кисню для людини.
