Реакції обміну між розчинами електролітів, умови їх протікання
Тема 1
РОЗЧИНИ
УРОК 14
Тема уроку. Реакції обміну між розчинами електролітів, умови їх протікання
Цілі уроку: показати процеси, що протікають у розчинах електролітів як реакції обміну між іонами; ознайомити з умовами їх протікання; формувати навички складання іонних рівнянь.
Тип уроку: формування вмінь і навичок та їх творчого застосування.
Форми роботи: розповідь учителя, демонстраційний експеримент, виконання тренувальних вправ.
Обладнання: таблиця розчинності, набір реактивів, лабораторне устаткування. Демонстрація
ХІД УРОКУ
I. Організація класу
II. Перевірка домашнього завдання.
Актуалізація опорних знань
1. Двоє учнів працюють біля дошки, решта – у зошитах виконують завдання.
Напишіть рівняння дисоціації запропонованих речовин.
Na2SО4
Na2CО3
Ва(ОН)2
Ca(ОH)2
HCl
LiОH
K2CО3
K3PО4
H3PО4
H2SО4
2. Фронтальне опитування (по ланцюжку)
Продовжте визначення.
Електроліти – це…
Ступінь дисоціації – це…
Кислота – це…
Основа – це…
Сіль – це…
Електролітична дисоціація – це…
ІІІ. Сприйняття
Демонстрація 4
Згадайте, які явища супроводжують хімічні реакції.
Ми з’ясували, що в розчині електроліти перебувають у формі іонів.
Дослід 1
Візьмемо два розчини: BaSО4 і Na2SО4.
Запишіть рівняння дисоціації цих солей:
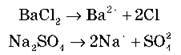
Змішуємо розчини. Що відбувається? Осад BaSО4 свідчить про протікання хімічної реакції.
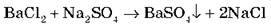
Оскільки в розчині BaCl2, Na2SО4 і NaCl перебувають у вигляді іонів, запишіть рівняння в іонній формі.
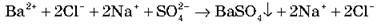
Розчинність BaSО4 настільки мала, що більша частина його в розчині перебуває у вигляді молекул BaSО4.
Отже, у розчині протікає реакція зв’язування іонів Ba2+ і SО24-, що описується рівнянням:
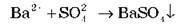
Дослід 2
Для наступної реакції візьмемо розчин натрій гідроксиду (з фенолфталеїном) і додамо по краплях хлоридну кислоту до зникнення малинового забарвлення. Ознака реакції – зникнення забарвлення індикатора:
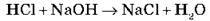
НCl, NaОН, NaCl – сильні електроліти, тобто в розчині перебувають у вигляді іонів.
Тоді запишемо рівняння реакції в іонній формі:
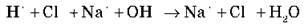
H2O – слабкий електроліт, ступінь дисоціації дорівнює 1,4 – 10-9. Тому практично протікає реакція:
H++ OH – 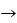 H2O
H2O
Дослід 3
До розчину Na2CO3 додамо розчин хлоридної кислоти. Ознака реакції – виділення вуглекислого газу:
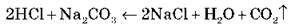
НО, Na2CО3, NaCl – сильні електроліти, тому в розчині перебувають у вигляді іонів.
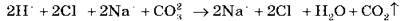
H2О і CО2 – слабкі електроліти, тому суть процесу описує рівняння:
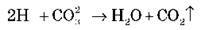
Отже, виділяють три умови незворотного протікання реакцій:
– утворення нерозчинної або малорозчинної речовини;
– утворення газоподібної речовини;
– утворення речовини, що дисоціює незначною мірою, наприклад H2О.
IV. Керована практика
Самостійна робота під керівництвом учителя.
Завдання 1
Запишіть рівняння в молекулярній повній та скороченій іонній формах.
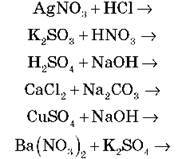
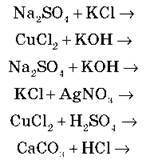
Завдання 2
Виберіть рівняння можливих реакцій.
V. Підбиття підсумків уроку, виставлення оцінок
VI. Домашнє завдання
Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи.
За таблицею розчинності підібрати три-чотири пари речовин, між якими можна записати іонні рівняння.




 (1 votes, average: 5.00 out of 5)
(1 votes, average: 5.00 out of 5)Related posts:
- Реакції іонного обміну – РОЗЧИНИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 5. РОЗЧИНИ. ТЕОРІЯ ЕЛЕКТРОЛІТИЧНОЇ ДИСОЦІАЦІЇ § 5.11. Реакції іонного обміну Згідно з теорією електролітичної дисоціації всі реакції у водних розчинах електролітів є реакціями між іонами. Вони називаються іонними реакціями, а рівняння цих реакцій – іонними рівняннями. Вони простіші, ніж рівняння реакцій, […]...
- РЕАКЦІЇ В РОЗЧИНАХ ЕЛЕКТРОЛІТІВ – ЕЛЕКТРОЛІТИ Хімія – універсальний довідник ЕЛЕКТРОЛІТИ РЕАКЦІЇ В РОЗЧИНАХ ЕЛЕКТРОЛІТІВ У розчинах електролітів у хімічну взаємодію вступають іони. З’ясуємо, у яких випадках це відбувається. Якщо змішати водні розчини кухонної солі (хлориду натрію) і вапняної води (розчину гідроксиду кальцію), то зовнішніх змін не спостерігається. Формально можна написати З огляду на те, що всі чотири речовини (хлорид і […]...
- Практична робота № 2. Реакції іонного обміну в розчинах електролітів Тема 1 РОЗЧИНИ Урок 16 Тема уроку. Практична робота № 2. Реакції іонного обміну в розчинах електролітів Цілі уроку: перевірити вміння використовувати практичні знання про електролітичну дисоціацію, навички дослідження розчинів, складання іонних рівнянь; уміння спостерігати, робити висновки. Тип уроку: практичного застосування знань, умінь і навичок. Форми роботи: самостійна практична робота. Обладнання: таблиця розчинності, набір хімічних […]...
- Реакції в розчинах електролітів. Складання молекулярних і йонно-молекулярних рівнянь ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 6. Суміші речовин. Розчини 6.10. Реакції в розчинах електролітів. Складання молекулярних і йонно-молекулярних рівнянь За нормальних умов тверді речовини зазвичай не вступають між собою в хімічні реакції. Хоч би один з реагентів повинен бути в газоподібному чи рідкому (розчиненому) стані. Отже, у хімії […]...
- Теорія електролітичної дисоціації. Іонні реакції I СЕМЕСТР ПОВТОРЕННЯ ОСНОВНИХ ПИТАНЬ КУРСУ ХІМІЇ ОСНОВНОЇ ШКОЛИ (4 год.) УРОК 3 Тема уроку. Теорія електролітичної дисоціації. Іонні реакції Цілі уроку: актуалізувати знання учнів про процеси, що протікають у розчинах; узагальнити знання про електролітичну дисоціацію речовин; удосконалювати вміння й навички складання повних і скорочених іонно-молекулярних рівнянь реакцій. Тип уроку: повторення й систематизації знань. Форми […]...
- Реакції сполучення, розкладу, заміщення й обміну Тема 2 ХІМІЧНІ РЕАКЦІЇ Урок 22 Тема уроку. Реакції сполучення, розкладу, заміщення й обміну Цілі уроку: розвивати навички й уміння складати рівняння хімічних реакцій; формувати навички розпізнавання типів реакцій теоретично – за рівняннями реакції, експериментально – за ознаками хімічних реакцій. Тип уроку: формування вмінь і навичок. Форми роботи: фронтальне опитування, демонстраційний експеримент, групова робота, самостійна […]...
- ОБОРОТНІ РЕАКЦІЇ – ЕЛЕКТРОЛІТИ Хімія – універсальний довідник ЕЛЕКТРОЛІТИ ОБОРОТНІ РЕАКЦІЇ Реакція дисоціації води, рівняння якої наведено у попередньому параграфі, протікає незначною мірою. З кожного мільярда молекул води в ній беруть участь лише дві, тому концентрація кожного з іонів, які утворюються, мізерно мала (10-7 моль/л). Коли кажуть, що вода – слабкий електроліт, то мають на увазі, що вона слабко […]...
- Гідроліз солей як окремий випадок реакцій йонного обміну у водних розчинах електролітів ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 6. Суміші речовин. Розчини 6.11. Гідроліз солей як окремий випадок реакцій йонного обміну у водних розчинах електролітів У хімії часто стикаються з явищем гідролізу1 – хімічної взаємодії речовин з водою. Найбільше практичне значення має гідроліз солей. Гідроліз солей – це хімічна взаємодія солей […]...
- Ступінь дисоціації. Сильні та слабкі електроліти Тема 1 РОЗЧИНИ Урок 13 Тема уроку. Ступінь дисоціації. Сильні та слабкі електроліти Цілі уроку: розширити знання учнів про електроліти; ознайомити з поняттями “сильні та слабкі електроліти”; показати кількісну характеристику процесу електролітичної дисоціації – ступінь дисоціації; закріпити навички складання рівнянь дисоціації кислот, основ і солей; визначити відмінності сильних і слабких електролітів. Тип уроку: комбінований урок […]...
- Електроліз водних розчинів електролітів – ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 7. ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ § 7.7. Електроліз водних розчинів електролітів Слід розрізняти електроліз розплавлених електролітів і їх розчинів. В останньому випадку в процесах можуть брати участь молекули води. Як приклад розглянемо електроліз концентрованого водного розчину хлориду натрію (електроди вугільні). В цьому […]...
- Сильні й слабкі електроліти – РОЗЧИНИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 5. РОЗЧИНИ. ТЕОРІЯ ЕЛЕКТРОЛІТИЧНОЇ ДИСОЦІАЦІЇ § 5.10. Сильні й слабкі електроліти Розрізняють сильні й слабкі електроліти. Сильні електроліти під час розчинення у воді повністю дисоціюють на іони. До них належать: 1) майже всі солі; 2) багато мінеральних кислот, наприклад H2SO4, HNO3, […]...
- РЕАКЦІЇ ОБМІНУ – ТИПИ ХІМІЧНИХ РЕАКЦІЙ Хімія – універсальний довідник ТИПИ ХІМІЧНИХ РЕАКЦІЙ РЕАКЦІЇ ОБМІНУ Реакції між складними хімічними речовинами, в результаті яких відбувається обмін між ними окремими атомами або групами атомів, називаються реакціями обміну. Наприклад: Реакції обміну (крім сильно екзотермічної реакції нейтралізації) зазвичай супроводжуються невеликим тепловим ефектом, тобто відбувається лише невелика зміна внутрішньої енергії системи, і вона не може бути […]...
- Ступінь дисоціації – РОЗЧИНИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 5. РОЗЧИНИ. ТЕОРІЯ ЕЛЕКТРОЛІТИЧНОЇ ДИСОЦІАЦІЇ § 5.9. Ступінь дисоціації Оскільки електролітична дисоціація – процес оборотний, то в розчинах електролітів поряд з їх іонами є й молекули. Тому розчини електролітів характеризуються ступенем дисоціації (позначається грецькою буквою “альфа” а). Ступінь дисоціації – це […]...
- Електролітична дисоціація – Розчини Хімія Загальна хімія Розчини Електролітична дисоціація Речовини, розчини або розплави яких проводять електричний струм, називаються електролітамИ. Речовини, розчини або розплави яких не проводять електричного струму, називаються неелектролітамИ. Розпад електролітів на йони під час їхнього розчинення у воді називається електролітичною дисоціацієЮ. Основні положення теорії електролітичної дисоціації 1) Електроліти під час розчинення у воді розпадаються (дисоціюють) на […]...
- Електролітична дисоціація кислот, основ, солей у водних розчинах Тема 1 РОЗЧИНИ Урок 12 Тема уроку. Електролітична дисоціація кислот, основ, солей у водних розчинах Цілі уроку: поглибити знання учнів про електролітичну дисоціацію на прикладі розчинів кислот, основ і солей; формувати навички складання рівнянь дисоціації на прикладі розчинних кислот, основ, солей; уточнити визначення кислот, основ і солей у світлі теорії електролітичної дисоціації. Тип уроку: засвоєння […]...
- Ступінь електролітичної дисоціації – Електролітична дисоціація ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 6. Суміші речовин. Розчини 6.6. Електролітична дисоціація 6.6.3. Ступінь електролітичної дисоціації Розчини можуть складатись із частинок розчинника, розчиненої речовини і продуктів їхньої взаємодії, а отже, у розчинах електролітів можуть дисоціювати не всі, а лише частина молекул. Кількісною характеристикою процесу дисоціації є ступінь дисоціації […]...
- Теорія електролітичної дисоціації – РОЗЧИНИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 5. РОЗЧИНИ. ТЕОРІЯ ЕЛЕКТРОЛІТИЧНОЇ ДИСОЦІАЦІЇ § 5.5. Теорія електролітичної дисоціації Для пояснення особливостей водних розчинів електролітів шведський учений С. Арреніус у 1887 р. запропонував теорію електролітичної дисоціації. Пізніше вона була розвинута багатьма вченими на основі вчення про будову атомів і хімічний […]...
- Механізм дисоціації – РОЗЧИНИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 5. РОЗЧИНИ. ТЕОРІЯ ЕЛЕКТРОЛІТИЧНОЇ ДИСОЦІАЦІЇ § 5.6. Механізм дисоціації Суттєвим є питання про механізм електролітичної дисоціації. І дійсно, чому електроліти дисоціюють на іони? Вчення про хімічний зв’язок атомів допомагає відповісти на це запитання. Найлегше дисоціюють речовини з іонним зв’язком. Як відомо, […]...
- СИЛЬНІ І СЛАБКІ ЕЛЕКТРОЛІТИ – ЕЛЕКТРОЛІТИ Хімія – універсальний довідник ЕЛЕКТРОЛІТИ СИЛЬНІ І СЛАБКІ ЕЛЕКТРОЛІТИ Якщо реакція речовини з водою, яка призводить до утворення іонів, не проходить до кінця і у розчині залишаються молекули вихідної речовини, тобто процес електролітичної дисоціації оборотний, то така речовина належить до слабких електролітів. Крім описаних у попередньому параграфі води й аміаку, до слабких електролітів належать майже […]...
- Оцінювання навчальних досягнень учнів з теми “Розчини” Тема 1 РОЗЧИНИ Урок 20 Тема уроку. Оцінювання навчальних досягнень учнів з теми “Розчини” Цілі уроку: узагальнити й систематизувати знання учнів з теми “Основні класи неорганічних сполук”; з’ясувати рівень навчальних досягнень учнів з теми, розуміння основних понять, уміння використовувати їх на практиці. Тип уроку: контролю й коригування знань, умінь і навичок. Форми роботи: письмова контрольна […]...
- РЕАКЦІЇ РОЗКЛАДУ – ТИПИ ХІМІЧНИХ РЕАКЦІЙ Хімія – універсальний довідник ТИПИ ХІМІЧНИХ РЕАКЦІЙ РЕАКЦІЇ РОЗКЛАДУ З назви “реакція розкладу” також випливає, про який тип реакцій іде мова. У реакції розкладу відбувається розкладання складної речовини на декілька речовин. Продуктами реакції можуть бути як прості, так і складні речовини. Наприклад: Майже всі вказані реакції, як і переважна більшість інших реакцій розкладу, ендотермічні. Для […]...
- Швидкість хімічної реакції – ХІМІЧНІ РЕАКЦІЇ ТА ЗАКОНОМІРНОСТІ ЇХ ПЕРЕБІГУ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЧНІ РЕАКЦІЇ ТА ЗАКОНОМІРНОСТІ ЇХ ПЕРЕБІГУ Швидкість хімічної реакції Хімічні реакції відрізняються одна від одної тривалістю їхнього протікання. Деякі хімічні реакції відбуваються миттєво (наприклад, вибух воднево-кисневої суміші, реакції обміну з утворенням осаду), інші – досить швидко (горіння речовин), треті – повільно (більшість реакцій […]...
- Швидкість хімічної реакції, залежність швидкості реакції від різних факторів Тема 2 ХІМІЧНІ РЕАКЦІЇ Урок 23 Тема уроку. Швидкість хімічної реакції, залежність швидкості реакції від різних факторів Цілі уроку: формувати уявлення учнів про швидкість хімічної реакції, вплив на неї різних факторів; показати залежність швидкості хімічної реакції від природи речовини, температури, концентрації; розвивати навички й уміння складати рівняння хімічних реакцій, розпізнавати типи реакцій за рівняннями реакції; […]...
- Хімічні властивості кислот. Реакції заміщення й обміну. Заходи безпеки під час роботи з кислотами. Використання кислот Тема 2 ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК УРОК 19 Тема. Хімічні властивості кислот. Реакції заміщення й обміну. Заходи безпеки під час роботи з кислотами. Використання кислот Цілі уроку: закріпити знання про хімічні властивості кислот на прикладі хлоридної кислоти; поглибити знання учнів про реакції заміщення й обміну на прикладі хімічних властивостей кислот; розвивати навички експериментальної роботи з […]...
- СОЛІ ЯК ЕЛЕКТРОЛІТИ – ЕЛЕКТРОЛІТИ Хімія – універсальний довідник ЕЛЕКТРОЛІТИ СОЛІ ЯК ЕЛЕКТРОЛІТИ При розчиненні у воді солі дисоціюють з утворенням позитивно заряджених іонів металу (або амонію NН4+) і негативно заряджених кислотних залишків. Ці іони і визначають поведінку солей у розчинах. Солі можуть взаємодіяти з кислотами: З лугами: З іншими солями: І тут, як і в усіх реакціях, які відбуваються […]...
- Електропровідність електролітів. Закони Фарадея ФІЗИКА Частина 3 ЕЛЕКТРИКА І МАГНЕТИЗМ Розділ 8 ЕЛЕКТРИКА 8.10. Електропровідність електролітів. Закони Фарадея Електроліти – розчини солей, кислот, лугів у рідинах – є добрими провідниками електричного струму. Струм у електролітах супроводжується електролізом – виділенням на електродах, занурених у розчин, складових частин електроліту. На відміну від металів, яким властива електронна провідність, струм в електролітах зумовлений […]...
- Сульфати. Якісна реакція на сульфат-іон. Розв’язання розрахункових задач з обчислення маси (об’єму, кількості речовини) продукту реакції, якщо один з реагентів узято в надлишку I СЕМЕСТР Тема 1. НЕМЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ (18 год.) УРОК 14 Тема уроку. Сульфати. Якісна реакція на сульфат-іон. Розв’язання розрахункових задач з обчислення маси (об’єму, кількості речовини) продукту реакції, якщо один з реагентів узято в надлишку Цілі уроку: розширити знання учнів про солі на прикладі властивостей сульфатів, їх застосування; ознайомити учнів з якісною […]...
- Тепловий ефект реакції. Екзотермічні й ендотермічні реакції. Термохімічні рівняння Тема 2 ХІМІЧНІ РЕАКЦІЇ Урок 24 Тема уроку. Тепловий ефект реакції. Екзотермічні й ендотермічні реакції. Термохімічні рівняння Цілі уроку: розширити уявлення про хімічні реакції на прикладі ендотермічних і екзотермічних реакцій; ознайомити учнів з поняттями “тепловий ефект хімічної реакції”, “термохімічні рівняння”; формувати навички й уміння складати термохімічні рівняння реакцій, розв’язувати задачі з їх використанням. Тип уроку: […]...
- Узагальнення й систематизація знань з теми “Розчини” Тема 1 РОЗЧИНИ Урок 19 Тема уроку. Узагальнення й систематизація знань з теми “Розчини” Цілі уроку: узагальнити, систематизувати та скоригувати знання учнів з теми “Розчини”; з’ясувати рівень засвоєння знань, умінь і навичок про процеси, що протікають у розчинах, рівень розуміння основних понять, умінь використовувати їх на практиці. Тип уроку: узагальнення й систематизації знань, умінь і […]...
- ЕЛЕКТРОЛІТИ І НЕЕЛЕКТРОЛІТИ – ЕЛЕКТРОЛІТИ Хімія – універсальний довідник ЕЛЕКТРОЛІТИ ЕЛЕКТРОЛІТИ І НЕЕЛЕКТРОЛІТИ Речовини, які мають іонну електропровідність, називаються електролітами. Усі інші речовини називаються неелектролітами. Електроліти – складні речовини, що складаються з іонів – позитивних і негативних, причому ці іони повинні володіти здатністю до переміщення в речовині. Таким чином, для того, щоб розпізнати, чи є дана рідина-неметал (тверда, рідка, розчин) […]...
- Порядок реакції – Вираження швидкості реакції ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ 3. Вираження швидкості реакції 3.2 . Порядок реакції На основі теорії зіткнення для різних типів молекулярних реакцій можна записати вирази для швидкості реакції: Константа k – константа швидкості реакції. Через спільний вплив різних чинників на швидкість реакції результати експериментів часто не відповідають теоретичним припущенням. Тому певна реакція описується експериментально виведеним рівнянням (виразом) […]...
- Іонні рівняння. Складання іонних рівнянь Тема 1 РОЗЧИНИ Урок 15 Тема уроку. Іонні рівняння. Складання іонних рівнянь Цілі уроку: закріпити навички й уміння складати іонні рівняння в розчинах електролітів; розвивати навички проведення хімічного експерименту на прикладі реакцій у розчинах електролітів. Тип уроку: застосування знань, умінь і навичок. Форми роботи: лабораторна робота, тренувальні вправи. Обладнання: таблиця розчинності, лабораторне устаткування й хімічні […]...
- Приклади розв’язування типових задач – Урок 7 ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 6. Суміші речовин. Розчини Приклади розв’язування типових задач Задача 1. Складіть молекулярне рівняння, що відповідає такому скороченому йонно-молекулярному рівнянню: Розв’язання Йонно-молекулярне рівняння реакції показує, що під час реакції відбулось зв’язування йонів Купруму Сu2+ і сульфід-іонів S2- в нерозчинну сполуку купрум(ІІ) сульфід CuS, тобто […]...
- Вплив середовища на характер перебігу реакцій – ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 7. ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ § 7.4. Вплив середовища на характер перебігу реакцій Реакції окиснення – відновлення можуть відбуватися в різних середовищах: у кислому (надлишок Н+-іонів), нейтральному (Н2О) і лужному (надлишок гідроксид-іонів ОН – ). Залежно від середовища може змінюватись і характер […]...
- ОКИСНО-ВІДНОВНІ РЕАКЦІЇ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС РЕАКЦІЇ ЗІ ЗМІНОЮ СТУПЕНІВ ОКИСНЕННЯ ЕЛЕМЕНТІВ ОКИСНО-ВІДНОВНІ РЕАКЦІЇ Окисно-відновні реакції проходять за рахунок переходу електронів або атомів від одних частинок до інших. У реакції Відбувається перехід електронів від атомів заліза (відновник) до іонів Купруму (окисник). В реакції Відбувається перехід атомів Оксигену від іонів СlO – (окисник) до йонів SO32- […]...
- Хімічні реакції. Окисно-відновні реакції I СЕМЕСТР ПОВТОРЕННЯ ОСНОВНИХ ПИТАНЬ КУРСУ ХІМІЇ ОСНОВНОЇ ШКОЛИ (4 год.) УРОК 4 Тема уроку. Хімічні реакції. Окисно-відновні реакції Цілі уроку: актуалізувати знання учнів про хімічні реакції; удосконалювати вміння й навички складання повних і скорочених іонно-молекулярних та окисно-відновних рівнянь реакції; узагальнити уявлення учнів про швидкість хімічної реакції, хімічну рівновагу й фактори, що впливають на швидкість […]...
- Електроліти і неелектроліти – РОЗЧИНИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 5. РОЗЧИНИ. ТЕОРІЯ ЕЛЕКТРОЛІТИЧНОЇ ДИСОЦІАЦІЇ § 5.4. Електроліти і неелектроліти Добре відомо, що одні речовини в розчиненому або розплавленому вигляді проводять електричний струм, інші за таких самих умов струм не проводять. Це можна простежити за допомогою простого приладу (рис. 5.4). Він […]...
- Іонні рівняння Тема 1 РОЗЧИНИ Урок 17 Тема уроку. Іонні рівняння Цілі уроку: закріпити вміння складати іонні рівняння реакцій; розвивати навички складання рівнянь хімічних реакцій на прикладі реакцій у розчинах електролітів; удосконалювати навички складання хімічних формул та іонних рівнянь. Тип уроку: творчого застосування знань, умінь і навичок. Форми роботи: фронтальна, групова, самостійна робота. Обладнання: таблиця розчинності, картки […]...
- Електроліз розчинів та розплавів електролітів – ОКИСНО-ВІДНОВНІ ПРОЦЕСИ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ОКИСНО-ВІДНОВНІ ПРОЦЕСИ Електроліз розчинів та розплавів електролітів Сукупність ОВР, які протікають на електродах у розчинах та розплавах електролітів при пропусканні через них електричного струму, називають електролізом. На підставі етимології слова можна сказати, що електроліз (від електро… і грец. лізіс – розклад) – це […]...
- РЕАКЦІЇ ПРОМІЖНОГО ОБМІНУ РЕЧОВИН, ЩО ВІДБУВАЮТЬСЯ В ЦИТОЗОЛІ, НА ПРИКЛАДІ ГЛІКОЛІЗУ ЦИТОПЛАЗМА, ЇЇ КОМПОНЕНТИ УРОК 21. РЕАКЦІЇ ПРОМІЖНОГО ОБМІНУ РЕЧОВИН, ЩО ВІДБУВАЮТЬСЯ В ЦИТОЗОЛІ, НА ПРИКЛАДІ ГЛІКОЛІЗУ Цілі уроку: розглянути особливості проміжного обміну речовин, проаналізувати механізми гліколізу та їх значення для життєдіяльності клітини. Обладнання й матеріали: таблиці або мультимедійна презентація “Будова рослинної клітини”, “Будова тваринної клітини”, “Гліколіз”. Базові поняття й терміни: проміжний обмін речовин, гліколіз, цитозоль, […]...