Солі амонію
РОЗДІЛ 2 НЕМЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХ СПОЛУКИ
ХІМІЧНІ ЕЛЕМЕНТИ VA ГРУПИ
§ 33. Солі амонію
Усвідомлення змісту цього параграфа дає змогу:
Характеризувати фізичні, загальні та специфічні хімічні властивості солей амонію, їх добування і застосування; експериментально розпізнавати солі амонію;
Складати рівняння та схеми електронного балансу відповідних хімічних реакцій.
Солі амонію мають йонну кристалічну гратку, у вузлах якої розміщуються катіони – йони амонію та аніони – кислотні залишки.
– Поміркуйте, який
Фізичні властивості. Солі амонію – це переважно безбарвні кристалічні речовини, добре розчинні у воді, термічно нестійкі на відміну від солей, утворених катіонами металічних елементів.
Хімічні властивості. Солі амонію належать до сильних електролітів, тому для них характерні загальні властивості солей. З багатоосновними кислотами утворюються солі двох видів: кислі, наприклад амоній гідрогенсульфат NH4HSO4, і середні – амоній сульфат (NH4)2SO4.
– Пригадайте загальні хімічні властивості
Як сильні електроліти солі амонію у водному розчині дисоціюють на йони амонію і йони кислотного залишку:
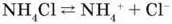
Цим визначаються їх загальні властивості, а саме взаємодія з: кислотами, якщо солі амонію утворені слабшими кислотами:
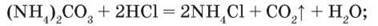
Лугами при нагріванні. Це якісна реакція на солі амонію:
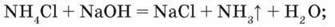
Іншими солями:
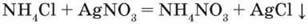
– Напишіть усі рівняння реакцій у йонних формах.
Коротко про головне
Солі амонію – сильні електроліти, у воді гідролізуються з утворенням кислого середовища. Для них характерні як загальні властивості солей, так і специфічні. Реакція з лугами є якісною на солі амонію. Ознака реакції – виділення амоніаку. При нагріванні солі амонію розкладаються, продукти реакції залежать від властивостей кислотного залишку. Застосування солей амонію визначається їх індивідуальними властивостями.
Для допитливих. Якщо нагрітий паяльник занурити в нашатир NH4Cl, то сіль розкладається (див. вище). Утворений хлороводень HCl взаємодіє з купрум(ІІ) оксидом СuO, що вкриває поверхню паяльника. Внаслідок цього утворюється купрум(ІІ) хлорид CuCl2, який сплавляється з надлишком нашатирю NH4Cl. Поверхня паяльника звільняється від оксидів, і розплавлене олово прилипає до очищеної міді.




 (1 votes, average: 5.00 out of 5)
(1 votes, average: 5.00 out of 5)Related posts:
- Солі амонію – Елементи VA групи ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 9. Неметалічні елементи та їхні сполуки. Неметали 9.4. Елементи VA групи 9.4.4. Солі амонію Солі амонію містять у своєму складі складний катіон NH4+. Це кристалічні речовини з йонним типом зв’язку, мають йонні кристалічні гратки, у вузлах яких розміщуються катіони (NH4+) та аніони (кислотні […]...
- Солі амонію – ПІДГРУПА НІТРОГЕНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 10. ПІДГРУПА НІТРОГЕНУ § 10.5. Солі амонію Солі амонію та їх властивості. Солі амонію складаються з катіона амонію та аніона кислоти. За будовою вони аналогічні відповідним солям однозарядних іонів металів. Солі амонію добувають при взаємодії аміаку або його водних розчинів з […]...
- Амоніак: властивості, використання. Солі амонію. Якісна реакція на іон амонію I СЕМЕСТР Тема 1. НЕМЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ (18 год.) УРОК 9 Тема уроку. Амоніак: властивості, використання. Солі амонію. Якісна реакція на іон амонію Цілі уроку: ознайомити зі складом, особливостями будови молекули й фізичними властивостями амоніаку, розчинністю амоніаку у воді й дією індикаторів на розчин, особливостями взаємодії амоніаку з водою й кислотами; формувати вміння […]...
- СПОЛУКИ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ З ГІДРОГЕНОМ. СОЛІ АМОНІЮ ТЕМА 1. НЕМЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ УРОК 5. СПОЛУКИ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ З ГІДРОГЕНОМ. СОЛІ АМОНІЮ Цілі: формувати знання про склад сполук неметалічних елементів з Гідрогеном, властивості та добування амоніаку і хлороводню, будову солей амонію, якісні реакції на іони амонію та хлорид-іони; формувати вміння складати формули сполук і рівняння реакцій, що характеризують властивості та способи […]...
- АМОНІАК І ХЛОРОВОДЕНЬ, ЇХ ВЛАСТИВОСТІ. СОЛІ АМОНІЮ ТЕМА 1. НЕМЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ УРОК 6. АМОНІАК І ХЛОРОВОДЕНЬ, ЇХ ВЛАСТИВОСТІ. СОЛІ АМОНІЮ Цілі: закріпити знання про амоніак і хлороводень, солі амонію, якісні реакції на іони амонію та хлорид-іони; формувати вміння складати формули сполук і рівняння реакцій, що характеризують властивості й способи добування сполук неметалічних елементів з Гідрогеном. Обладнання: роздавальний матеріал, мультимедійний […]...
- Солі ортофосфатної кислоти – Елементи VA групи ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 9. Неметалічні елементи та їхні сполуки. Неметали 9.4. Елементи VA групи 9.4.12. Солі ортофосфатної кислоти Як трьохосновна кислота Н3РO4 утворює три ряди солей: 1) середні (нормальні): К3РО4 – калій ортофосфат, Mg3(PO4)2-магній ортофосфат; І кислі: 2) однозаміщені: КН2РO4 – калій дигідрогенфосфат, Са(Н2РO4)2 – кальцій […]...
- Солі – НАЙВАЖЛИВІШІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 6. НАЙВАЖЛИВІШІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК § 6.4. Солі Визначення класу солей див. § 5.8. Рівняння їх дисоціації із урахуванням гідратації іонів слід записувати так: NaCl (к.) ⇆Na+ (водн.) + Сl – (водн.); К3РО4 (к.) ЗК+ (водн.) + РО3-4 (водн.). Залежно від […]...
- Солі (середні), їх склад і назви Тема 2 ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК УРОК 14 Тема. Солі (середні), їх склад і назви Цілі уроку: розширити знання про класифікацію неорганічних речовин і номенклатуру неорганічних речовин на прикладі солей; навчити називати солі, складати їхні формули за валентностями, розпізнавати з-поміж інших класів неорганічних сполук; розвивати вміння й навички складати формули за валентністю на прикладі солей, […]...
- СОЛІ ЯК ЕЛЕКТРОЛІТИ – ЕЛЕКТРОЛІТИ Хімія – універсальний довідник ЕЛЕКТРОЛІТИ СОЛІ ЯК ЕЛЕКТРОЛІТИ При розчиненні у воді солі дисоціюють з утворенням позитивно заряджених іонів металу (або амонію NН4+) і негативно заряджених кислотних залишків. Ці іони і визначають поведінку солей у розчинах. Солі можуть взаємодіяти з кислотами: З лугами: З іншими солями: І тут, як і в усіх реакціях, які відбуваються […]...
- Солі – ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК Солі Поняття про солі, їхній склад та назви Солі можна розглядати як продукти заміщення атомів Гідрогену в кислоті на атоми металічних елементів. Кухонну сіль, наприклад, можна добути з хлоридної кислоти за допомогою реакції заміщення. Солі – складні речовини, які […]...
- Властивості кислот, основ і солей з погляду теорії електролітичної дисоціації ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 6. Суміші речовин. Розчини 6.7. Властивості кислот, основ і солей з погляду теорії електролітичної дисоціації Згідно з теорією електролітичної дисоціації, кислоти – це сполуки, які дисоціюють на катіони Гідрогену1 та аніони кислотного залишку: Як уже згадувалось, багатоосновні кислоти дисоціюють ступінчасто. Основність кислоти визначається […]...
- Карбонатна кислота та її солі РОЗДІЛ 2 НЕМЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХ СПОЛУКИ ХІМІЧНІ ЕЛЕМЕНТИ IVA ГРУПИ § 48. Карбонатна кислота та її солі Усвідомлення змісту цього параграфа дає змогу: Називати солі карбонатної кислоти за хімічною і тривіальною номенклатурами; Характеризувати фізичні та хімічні властивості, способи добування, застосування карбонатної кислоти та її солей; Складати рівняння відповідних хімічних реакцій. Карбонатна кислота Н2СО3 відповідає […]...
- Сульфітна кислота та її солі – Елементи VIA групи ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 9. Неметалічні елементи та їхні сполуки. Неметали 9.3. Елементи VIA Групи 9.3.9. Сульфітна кислота та її солі Сульфітна кислота Н2SO3 – це слабка двохосновна кислота, існує лише в розбавлених розчинах1. Дисоціює двоступенево: Хімічні властивості Виявляє властивості кислот; при взаємодії з лугами може утворювати […]...
- Електролітична дисоціація – Розчини Хімія Загальна хімія Розчини Електролітична дисоціація Речовини, розчини або розплави яких проводять електричний струм, називаються електролітамИ. Речовини, розчини або розплави яких не проводять електричного струму, називаються неелектролітамИ. Розпад електролітів на йони під час їхнього розчинення у воді називається електролітичною дисоціацієЮ. Основні положення теорії електролітичної дисоціації 1) Електроліти під час розчинення у воді розпадаються (дисоціюють) на […]...
- Солі нітратної кислоти – ПІДГРУПА НІТРОГЕНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 10. ПІДГРУПА НІТРОГЕНУ § 10.9. Солі нітратної кислоти Одноосновна нітратна кислота утворює тільки середні солі, які називаються нітратами. Вони утворюються при дії кислоти на метали, їх оксиди і гідроксиди. Нітрати натрію, калію, амонію і кальцію називаються селітрами. NaNO3 – натрієва селітра, […]...
- Солі карбонатної кислоти – ПІДГРУПА КАРБОНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 11. ПІДГРУПА КАРБОНУ § 11.4. Солі карбонатної кислоти Карбонатна кислота утворює два ряди солей: середні – карбонати і кислі – гідрокарбонати. Вони виявляють загальні властивості солей. Карбонати і гідрокарбонати лужних металів та амонію добре розчиняються у воді. Солі карбонатної кислоти – […]...
- Сполуки Алюмінію РОЗДІЛ 3 МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХ СПОЛУКИ ХІМІЧНІ ЕЛЕМЕНТИ ІА – ІІІА ГРУП § 66. Сполуки Алюмінію Усвідомлення змісту цього параграфа дає змогу: Характеризувати фізичні та хімічні властивості оксиду, гідроксиду і солей Алюмінію; їх добування і застосування; Складати рівняння та схеми електронного балансу відповідних хімічних реакцій; Добувати експериментально алюміній гідроксид, доводити його амфотерні властивості. До […]...
- МІНЕРАЛЬНІ СОЛІ ТА ЙОНИ В ЖИВОМУ ОРГАНІЗМІ Розділ 2 Молекулярний рівень організації живої природи Тема 4 Неогранічні речовини живих організмів § 15. МІНЕРАЛЬНІ СОЛІ ТА ЙОНИ В ЖИВОМУ ОРГАНІЗМІ Терміни та поняття: буферність, тироксин, явище йонної асиметрії живого. Які мінеральні речовини та йони входять до складу живого. На солі неорганічних кислот, які ще називають мінеральними, припадає не більш як 1,5 % маси […]...
- Лужні метали. Натрій і Калій. Оксиди, гідроксиди, солі Натрію й Калію. Використання найважливіших сполук Натрію й Калію. Калійні добрива ІІ семестр Тема 2. МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ (13 годин) УРОК 28 Тема уроку. Лужні метали. Натрій і Калій. Оксиди, гідроксиди, солі Натрію й Калію. Використання найважливіших сполук Натрію й Калію. Калійні добрива Цілі уроку: поглибити й розширити знання про метали на прикладі лужних металів Натрію й Калію; вивчити зв’язок між властивостями оксидів, гідроксидів, […]...
- Солі сульфатної кислоти – ПІДГРУПА ОКСИГЕНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 9. ПІДГРУПА ОКСИГЕНУ § 9.8. Солі сульфатної кислоти Сульфатна кислота, як двохосновна, утворює два ряди солей: середні, що називаються сульфатами, і кислі, що називаються гідросульфатами. Сульфати утворюються при повній нейтралізації кислоти лугом (на один моль кислоти припадає два молі лугу), а […]...
- Солі Алюмінію – Алюміній ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 8. Металічні елементи та їхні сполуки. Метали 8.4. Алюміній 8.4.3. Солі Алюмінію Алюміній утворює солі всіх типів з відомими неорганічними кислотами. Зазначимо, що йон Аl3+ здатний до комплексоутворення завдяки великому заряду та наявності вакантних орбіталей: Середні Кислі Основні Подвійні (галуни) Комплексні АlСl3, Al2(SO4)3 […]...
- Гідроліз солей РОЗДІЛ 1 ПОВТОРЕННЯ ТА ПОГЛИБЛЕННЯ ТЕОРЕТИЧНИХ ПИТАНЬ КУРСУ ХІМІЇ ОСНОВНОЇ ШКОЛИ § 13. Гідроліз солей Усвідомлення змісту цього параграфа дає змогу: Пояснювати поняття “гідроліз солей” і суть цього процесу; характеризувати різні випадки гідролізу; Вміти наводити приклади гідролізу і складати рівняння відповідних реакцій; Прогнозувати реакцію середовища та експериментально її визначати. Пригадайте, які речовини називаються солями та […]...
- Солі натрію і калію – МЕТАЛИ ГОЛОВНИХ ПІДГРУП ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 13. МЕТАЛИ ГОЛОВНИХ ПІДГРУП § 13.4. Солі натрію і калію Натрій утворює солі з усіма кислотами. Майже всі його солі розчинні у воді. Найважливіші з них – хлорид натрію (кухонна сіль), сода і сульфат натрію. Хлорид натрію NaCl – необхідна приправа […]...
- Класифікація хімічних елементів і речовин. Властивості основних класів неорганічних сполук РОЗДІЛ 1 ПОВТОРЕННЯ ТА ПОГЛИБЛЕННЯ ТЕОРЕТИЧНИХ ПИТАНЬ КУРСУ ХІМІЇ ОСНОВНОЇ ШКОЛИ § 1. Класифікація хімічних елементів і речовин. Властивості основних класів неорганічних сполук Усвідомлення змісту цього параграфа дає змогу: класифікувати хімічні елементи та їх речовини; визначати властивості основних класів неорганічних сполук; називати хімічні елементи та їх сполуки; наводити приклади s-,p-, d-елементів; Складати рівняння хімічних реакцій, […]...
- Кальцій. Кальцій оксид і гідроксид. Солі Кальцію. Поняття про твердість води. Використання найважливіших сполук Кальцію ІІ семестр Тема 2. МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ (13 годин) УРОК 29 Тема уроку. Кальцій. Кальцій оксид і гідроксид. Солі Кальцію. Поняття про твердість води. Використання найважливіших сполук Кальцію Цілі уроку: розширити знання учнів про метали на прикладі лужноземельних металів; вивчити властивості лужноземельних металів, їхніх сполук, способи одержання й застосування на прикладі Кальцію; продовжити […]...
- Розв’язування типових задач Оксиди, кислоти, основи, солі – НАЙВАЖЛИВІШІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 6. НАЙВАЖЛИВІШІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК § 6.7. Розв’язування типових задач Оксиди, кислоти, основи, солі Задача 1. Напишіть рівняння реакцій, за допомогою яких можна здійснити такі перетворення; CuSO4 -> Сu -> СuО -> СuСl2 -> Сu(OН)2 -> Cu(OH)NO3 -> Сu(NO3)2. Розв’язання. 1) […]...
- Ферум. Ферум(ІІ) і ферум(ІІІ) оксиди, відповідні їм гідроксиди, їх амфотерність. Солі Феруму. Використання найважливіших сполук Феруму ІІ семестр Тема 2. МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ (13 годин) УРОК 31 Тема уроку. Ферум. Ферум(ІІ) і ферум(ІІІ) оксиди, відповідні їм гідроксиди, їх амфотерність. Солі Феруму. Використання найважливіших сполук Феруму Цілі уроку: поглибити й узагальнити знання учнів про метали побічних підгруп на прикладі Феруму; показати залежність будови та властивостей на прикладі сполук Феруму(ІІ) і […]...
- Тема 14. Солі – ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА ІІ ЗАВДАННЯ ДЛЯ ПЕРЕВІРКИ ЗНАНЬ ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК Тема 14. Солі Серед чотирьох наведених варіантів відповідей виберіть одну правильну 1. Вкажіть речовини, при взаємодії яких одна з одною виділяється осад: A. Купрум(ІІ) гідроксид та натрій гідроксид; Б. Аргентум нітрат та натрій хлорид; B. Кальцій карбонат […]...
- Солі кальцію – Металічні елементи головної підгрупи II групи ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 8. Металічні елементи та їхні сполуки. Метали 8.3. Металічні елементи головної підгрупи II групи1 8.3.8. Солі кальцію Якісне виявлення: іони Са2+ забарвлюють полум’я газового пальника в цегляно-червоний колір. Карбонат амонію осаджує з розчинів солей Кальцію білий осад СаСО3. Гіпс CaSО4 · 2Н2О при […]...
- Приклади розв’язування типових задач – Урок 7 ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 6. Суміші речовин. Розчини Приклади розв’язування типових задач Задача 1. Складіть молекулярне рівняння, що відповідає такому скороченому йонно-молекулярному рівнянню: Розв’язання Йонно-молекулярне рівняння реакції показує, що під час реакції відбулось зв’язування йонів Купруму Сu2+ і сульфід-іонів S2- в нерозчинну сполуку купрум(ІІ) сульфід CuS, тобто […]...
- Солі хлоридної кислоти – ВОДЕНЬ. ГАЛОГЕНИ-НЕОРГАНІЧНА ХІМІЯ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 8. ВОДЕНЬ. ГАЛОГЕНИ § 8.8. Солі хлоридної кислоти Нижче описано найважливіші солі хлоридної кислоти. Хлорид натрію (інші назви: кам’яна сіль, кухонна сіль, галіт) NaCl є приправою до їжі, сировиною для добування гідроксиду натрію, хлору, хлоридної кислоти, соди тощо; використовується для консервування […]...
- Розрахунки за рівняннями хімічних реакцій між розчином солі та металом РОЗДІЛ 3 МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХ СПОЛУКИ § 53. Розрахунки за рівняннями хімічних реакцій між розчином солі та металом Усвідомлення змісту цього параграфа дає змогу: Пояснювати суть і причини зміни маси пластинки в зазначених реакціях; Розв’язувати задачі “на пластинку”. Задачі такого типу засновані на закономірностях витискувального ряду металів. Як ви уже знаєте, показником порівняльної хімічної […]...
- Алюміній. Алюміній оксид, алюміній гідроксид, їх амфотерність. Солі Алюмінію. Використання найважливіших сполук Алюмінію ІІ семестр Тема 2. МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ (13 годин) УРОК 30 Тема уроку. Алюміній. Алюміній оксид, алюміній гідроксид, їх амфотерність. Солі Алюмінію. Використання найважливіших сполук Алюмінію Цілі уроку: розширити й поглибити знання учнів про метали на прикладі Алюмінію – представника головної підгрупи ІІІ групи; повторити поняття амфотерності на прикладі сполук Алюмінію, їх хімічних […]...
- Сполуки Натрію і Калію РОЗДІЛ 3 МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХ СПОЛУКИ ХІМІЧНІ ЕЛЕМЕНТИ ІА – ІІІА ГРУП § 59. Сполуки Натрію і Калію Усвідомлення змісту цього параграфа дає змогу: Характеризувати фізичні та хімічні властивості оксидів, гідроксидів і солей Натрію та Калію; Складати рівняння відповідних хімічних реакцій; обгрунтовувати застосування сполук їх властивостями; визначати експериментально йони Натрію та Калію у солях. […]...
- Нітрати – Елементи VA групи ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 9. Неметалічні елементи та їхні сполуки. Неметали 9.4. Елементи VA групи 9.4.7. Нітрати Солі нітратної кислоти називають нітратами. Нітрати – це тверді кристалічні речовини йонної будови. Усі нітрати добре розчинні у воді. При випарюванні їхніх розчинів здебільшого утворюються кристалогідрати: хром(ІІІ) нітрат нонагідрат Cr(NO3)3 […]...
- Неорганічні речовини: вода і мінеральні солі – Неорганічні речовини Біологія. Експерес-підготовка до ЗНО та ДПА ТЕОРЕТИЧНІ ВІДОМОСТІ РОЗДІЛ І. МОЛЕКУЛЯРНИЙ РІВЕНЬ ОРГАНІЗАЦІЇ ЖИТТЯ Тема 1. Неорганічні речовини Неорганічні речовини: вода і мінеральні солі Вода Молекула води (Н20) полярна. Її різні полюси мають частково позитивні й негативні заряди. У цілому молекула води електронейтральна. Сусідні молекули води можуть притягуватись одна до одної за рахунок сил електростатичної […]...
- Нітрити та нітрати РОЗДІЛ 2 НЕМЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХ СПОЛУКИ ХІМІЧНІ ЕЛЕМЕНТИ VA ГРУПИ § 37. Нітрити та нітрати Усвідомлення змісту цього параграфа дає змогу: Характеризувати фізичні та хімічні властивості нітритів і нітратів, їх застосування; Складати рівняння та схеми електронного балансу відповідних хімічних реакцій; Висловлювати судження про вміст нітратів і нітритів у харчових продуктах. Нітрити Ме(NO2)n є похідними […]...
- Генетичні зв’язки між класами неорганічних речовин – Основні класи неорганічних сполук ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 7. Основні класи неорганічних сполук 7.6. Генетичні зв’язки між класами неорганічних речовин Між класами речовин – простими (металами і неметалами) і складними (оксидами, кислотами, основами, солями) – існує зв’язок і можливість взаємного переходу: Зв’язки між класами неорганічних речовин, які грунтуються на одержанні речовин […]...
- КАРБОНАТНА КИСЛОТА ТА ЇЇ СОЛІ – ВУГЛЕЦЬ І ЙОГО СПОЛУКИ Хімія – універсальний довідник ВУГЛЕЦЬ І ЙОГО СПОЛУКИ КАРБОНАТНА КИСЛОТА ТА ЇЇ СОЛІ З хімічної точки зору оксид карбону (IV) – кислотний оксид із властивостями, характерними для даного класу неорганічних сполук. Йому відповідає карбонатна кислота Н2СО3. Це дуже нестійка сполука, у вільному вигляді не існує, та й у водних розчинах молекули карбонатної кислоти не виявляються. […]...
- Хімічні властивості оксидів – ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК Хімічні властивості оксидів Основні Амфотерні Кислотні Взаємодіють із кислотами з утворенням солі та води: СаО + 2НСl → СаСl2 + Н2O Взаємодіють із кислотами та основами з утворенням солі й води: ZnO + 2НСl → ZnCl2 + Н2O; ZnO […]...