Вуглеводи. Глюкоза. Будова глюкози як альдегідоспирту. Циклічна форма глюкози. Хімічні властивості глюкози: повне й часткове окиснення, відновлення, гідроліз, взаємодія з гідроксидами металевих елементів, бродіння, естерифікація
II Семестр
Тема 4. ОКСИГЕНОВМІСНІ ОРГАНІЧНІ СПОЛУКИ
Урок 44
Тема уроку. Вуглеводи. Глюкоза. Будова глюкози як альдегідоспирту. Циклічна форма глюкози. Хімічні властивості глюкози: повне й часткове окиснення, відновлення, гідроліз, взаємодія з гідроксидами металевих елементів, бродіння, естерифікація
Цілі уроку: ознайомити учнів із класифікацією вуглеводів, їхніми фізичними властивостями; дати уявлення про будову альдегідної та циклічної форм молекул глюкози; вивчити ізомерію моносахаридів, ознайомитися з фізичними й хімічними
Тип уроку: комбінований урок засвоєння знань, умінь і навичок і творчого застосування їх на практиці.
Форми роботи: евристична бесіда, навчальна лекція, лабораторна робота.
Лабораторний дослід 11. Взаємодія глюкози з купрум(ІІ) гідроксидом.
Демонстрація 11. Взаємодія глюкози з аргентум(І) оксидом.
Обладнання: схема будови глюкози та її ізомерів.
ХІД УРОКУ
I. Організація класу
II. Перевірка домашнього завдання.
Актуалізація опорних знань
Завдання для обговорення в класі записуються
1) З перелічених сполук виберіть ті, що можуть утворитися в результаті гідролізу жирів:
А) одноатомні спирти;
Б) гліцерин;
В) етиленгліколь;
Г) мурашина кислота;
Д) пальмітинова кислота.
2) Як зміниться температура плавлення жиру внаслідок збільшення вмісту ненасичених кислот?
3) Масляноізоаміловий естер має запах ананасів. Напишіть формулу цього естеру, запропонуйте спосіб його практичного використання.
4) Напишіть структурні формули двох можливих ізомерів жиру, до складу якого входять один залишок пальмітинової та два залишки стеаринової кислот.
5) Поясніть, чому після висихання розлитої рослинної олії вона не змивається водою та звичайними мийними засобами. Де використовується ця властивість рослинної олії?
6) Чому жири належать до біологічно активних речовин?
7) Які ще біологічно активні речовини ви знаєте з курсу біології?
III. Вивчення нового матеріалу
ВУГЛЕВОДИ: БУДОВА, ФІЗИЧНІ ВЛАСТИВОСТІ
1. Розповідь учителя
Поговоримо сьогодні про вуглеводи – складні оксигеновмісні органічні сполуки.
Вуглеводи – найважливіші природні сполуки, що характеризуються біологічною активністю, відіграють важливу роль у житті рослин, тварин, людини.
Свою назву вони одержали через перші уявлення про склад вуглеводів як сполуки Карбону з водою: Cx(H2O)y. Ця назва збереглася дотепер, хоча доведено складну будову вуглеводів.
Вуглеводи входять до складу клітин і тканин усіх рослинних і тваринних організмів і за масою становлять переважну частину органічної речовини на Землі. На частку вуглеводів припадає близько 80 % сухої речовини рослин і близько 20 % – тварин. їжа людини на 70 % складається з вуглеводів. Рослини синтезують вуглеводи з неорганічних сполук – вуглекислого газу й води (CO2 і H2O).
Вуглеводи мають загальну формулу Cn(H2O)m, звідки й виникла назва цих природних сполук.
Вуглеводи поділяються на прості цукри, або моносахариди (монози), і полімери цих простих цукрів, або полісахариди (поліози). Серед полісахаридів слід виокремити групу олігосахаридів, що містять у молекулі від двох до десяти моносахаридних залишків. До них належать, зокрема, дисахариди.
Моносахариди є гетерофункціональними сполуками. У їхніх молекулах одночасно містяться і карбонільна (альдегідна, або кетонна), і кілька гідроксильних груп, тобто моносахариди є полігідроксикарбонільними сполуками – полігідроксиальдегідами й полігідроксикетонами. Залежно від цього моносахариди поділяються на альдози (у моносахариді міститься альдегідна група) і кетози (наявна кетогрупа). Наприклад, глюкоза – це альдоза, а фруктоза – це кетоза.
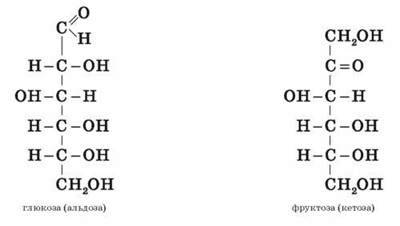
Залежно від числа атомів Карбону в молекулі моносахарид називається тетрозою, пентозою, гексозою тощо. Якщо об’єднати останні два типи класифікації, то глюкоза – це альдогексоза, а фруктоза – кетогексоза. Більшість наявних у природі моносахаридів – це пентози й гексози.
2. Класифікація вуглеводів
(Заповнюємо з учнями схему, учні самостійно наводять приклади, роблять висновки про застосування вуглеводів, повідомлення про поширення вуглеводів у природі.)
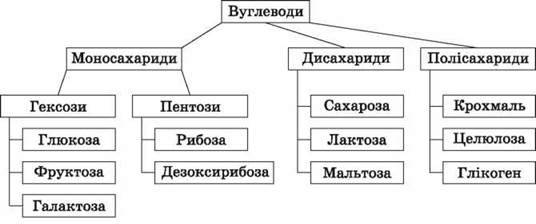
3. Розповідь учителя
Глюкоза
Найпростіший представник вуглеводів – глюкоза, її молекулярна формула – C6H12O6. За своєю будовою глюкоза – складна багатофункціональна сполука, що містить п’ять гідроксильних і одну альдегідну групу (-COH).
1) Демонстрація 11. Взаємодія глюкози з аргентум(І) оксидом
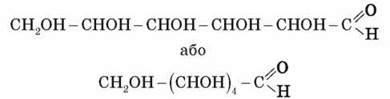
Як показали дослідження, у розчині глюкози містяться молекули лінійної та циклічної будов.
¦ До якого класу органічних сполук можна зарахувати глюкозу?
(Багатоатомні спирти, альдегіди)
Наявність функціональної групи – CHO дозволяє зарахувати глюкозу до класу альдегідів. Отже, глюкоза – альдегідоспирт.
Циклічні? – і?-форми глюкози є просторовими ізомерами, що відрізняються положенням півацетального гідроксилу відносно площини кільця. В?-глюкозі цей гідроксил перебуває в цис-положенні до гідроксилу біля атома C2, у?-глюкозі – у транс-положенні.
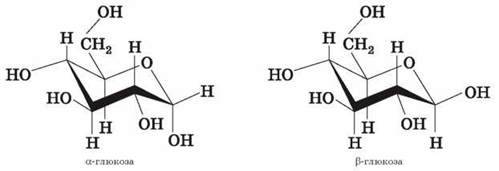
Розглянемо схему ізомеризації молекули глюкози:
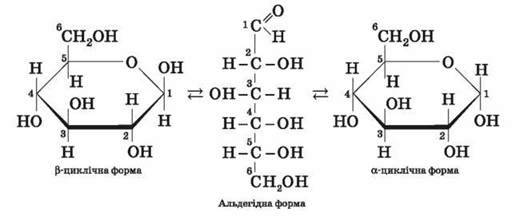
Глюкоза – цінна поживна речовина. Унаслідок її окиснення в тканинах вивільняється енергія, необхідна для нормальної життєдіяльності організмів. Реакцію окиснення можна описати сумарним рівнянням:
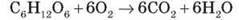
Глюкоза застосовується в медицині для приготування лікувальних препаратів, консервування крові, внутрішньовенного вливання та ін. Вона широко застосовується в кондитерському виробництві, у виробництві дзеркал та іграшок (сріблення).
¦ Як довести, що глюкоза має п’ять гідроксильних груп?
2) Лабораторний дослід 11. Взаємодія глюкози з купрум(П) гідроксидом
Приготуємо купрум(ІІ) гідроксид, додамо до одержаного осаду розчин глюкози. Що спостерігаємо? Про що свідчать розчинення та яскраво-синє забарвлення розчину? (Глюкоза – багатоатомний спирт) Тепер, дотримуючись правил нагрівання, підігріємо пробірку. Що спостерігаємо? Зміна забарвлення пов’язана з відновними властивостями альдегідної групи. Рівняння можна сумарно записати так:
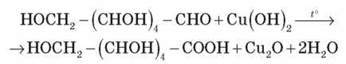
Купрум(І) оксид має яскраво-оранжевий колір. Цю реакцію використовують як якісну реакцію на глюкозу.
*Глюкоза, завдяки наявності альдегідної групи, окислюється амоніаковим розчином аргентум(І) оксиду (реакція “срібного дзеркала”) або купрум(ІІ) гідроксидом (якісні реакції):

Крім цього, глюкоза – як альдегід – вступає в реакції сполучення (відновлюється):

Важливе значення для життєдіяльності людини й тварин мають реакції бродіння глюкози.
Спиртове бродіння:
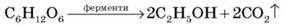
Молочнокисле бродіння:
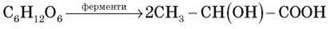
Маслянокисле бродіння:
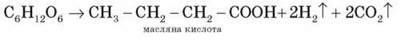
Згадані види бродіння, що спричиняються мікроорганізмами, мають велике практичне значення. Наприклад, спиртове використовується для одержання етилового спирту, у виноробстві, пивоварінні тощо, а молочнокисле – для виробництва молочної кислоти й кисломолочних продуктів.
4. Одержання глюкози
У вільній формі в природі поширена переважно глюкоза. Вона ж є структурною одиницею багатьох полісахаридів. Решта моносахаридів у вільному стані трапляються рідко коли й переважно відомі як компоненти оліго – й полісахаридів. У природі глюкоза утворюється в результаті реакції фотосинтезу:
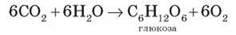
Уперше глюкозу одержав 1811 р. російський хімік Г. Е. Кірхгоф – у результаті гідролізу крохмалю. Згодом синтез моносахаридів з формальдегіду в лужному середовищі був запропонований О. М. Бутлеровим.
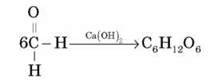
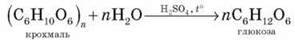
У промисловості глюкозу одержують шляхом гідролізу крохмалю в присутності сульфатної кислоти:
5. Фізичні властивості глюкози
Моносахариди – тверді речовини, легко розчинні у воді, погано – у спирті, і зовсім нерозчинні в етері. Водні розчини мають нейтральну реакцію на лакмус. Більшість моносахаридів мають солодкий смак, однак слабший, ніж буряковий цукор.
Глюкоза – це біла кристалічна речовина, добре розчинна у воді, має низьку температуру плавлення (t°пл = 146 °C).
IV. Первинне застосування одержаних знань
¦ Запишіть рівняння реакції горіння глюкози самостійно.
¦ Подумайте, де ми вже спостерігали таку реакцію? Ця реакція зворотна реакції фотосинтезу. Отже, через вуглеводи живі організми одержують енергію.
V. Підбиття підсумків уроку
Підбиваємо підсумки уроку, оцінюємо роботу учнів на уроці.
VI. Домашнє завдання
Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи.
Творче завдання: підготуйте повідомлення про поширення в природі й застосування моносахаридів (фруктози, рибози й дезоксирибози).
