Хімічні властивості спиртів: повне й часткове окиснення, дегідратація, взаємодія з лужними металами, гідрогенгалогенідами
II Семестр
Тема 4. ОКСИГЕНОВМІСНІ ОРГАНІЧНІ СПОЛУКИ
Урок 30
Тема уроку. Хімічні властивості спиртів: повне й часткове окиснення, дегідратація, взаємодія з лужними металами, гідрогенгалогенідами
Цілі уроку: вивчити хімічні властивості спиртів на прикладі насичених одноатомних спиртів – їх повного окиснення, взаємодії з металевим натрієм, гідроген хлоридом; показати зв’язок хімічних властивостей спиртів з наявністю функціональної гідроксильної групи; розвивати вміння й навички складати хімічні рівняння на прикладі хімічних
Тип уроку: комбінований урок засвоєння знань, умінь і навичок і творчого застосування їх на практиці.
Форми роботи: навчальна лекція, демонстраційний експеримент, самостійна робота.
Демонстрація 2. Взаємодія етанолу з натрієм.
Демонстрація 3. Взаємодія етанолу з гідроген бромідом.
ХІД УРОКУ
I. Організація класу
II. Перевірка домашнього завдання.
Мотивація навчальної діяльності
Біля дошки учні повторюють особливості будови спиртів, зумовлені наявністю ОН-групи.
¦ Чи відрізнятимуться властивості спиртів і вуглеводнів? Чому?
¦
III. Вивчення нового матеріалу
ХІМІЧНІ ВЛАСТИВОСТІ СПИРТІВ
1. Вступне слово вчителя
Спирти – речовини нейтральні. Незважаючи на наявність гідроксильної групи, спирти не змінюють забарвлення індикаторів, не вступають у хімічні реакції з водними розчинами лугів і розведених кислот. Лабораторні спиртівки заповнюють 98%-м спиртом. Який висновок можна зробити про горючість спиртів?
2. Хімічні властивості спиртів
У хімічних реакціях гідроксисполук можливе руйнування одного з двох зв’язків:
– C – OH з відщепленням ОН-групи;
– O – H з відщепленням Гідрогену.
Це можуть бути реакції заміщення, у яких відбувається заміна – OH або Н, або реакція відщеплення (елімінування), коли утворюється подвійний зв’язок.
Полярний характер зв’язків C – O й O – H сприяє гетеролітич – ному їх розриву й перебігу реакцій за іонним механізмом. У разі розриву зв’язку O – H з відщепленням протона H+ проявляються кислотні властивості гідроксисполуки, а у випадку розриву зв’язку C – O – властивості основи й нуклеофільного реагенту.
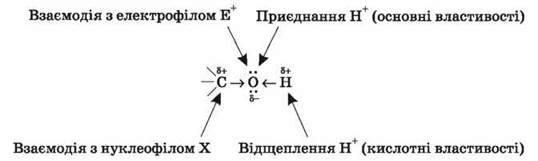
Реакції за зв’язком О-Н
До найбільш характерних реакцій гідроксисполук, що відбуваються з розривом зв’язку O – H, належать такі:
– реакції заміщення атома Гідрогену на метал (кислотні властивості);
– реакції заміщення атома Гідрогену на залишок кислоти (утворення естерів);
– реакції виділення водню в процесі окиснення й дегідрування. Легкість перебігу цих реакцій і будова продуктів, що утворюються, залежать від будови вуглеводневого радикала та взаємного впливу атомів.
Кислотні властивості спиртів
Одноатомні спирти реагують з активними металами (Na, K, Mg, Al та ін.), утворюючи солі – алкоголяти.
Демонстрація 2. Взаємодія етанолу з натрієм
2R – OH + 2Na 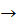 2RO – Na + H2
2RO – Na + H2
Запишіть рівняння реакції взаємодії етанолу з калієм:
2C2H5OH + 2K 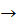 2C2H5O – K + H2
2C2H5O – K + H2
*Алкоголяти під дією води повністю гідролізуються з виділенням спирту й гідроксиду металу:
C2H5KR + H2O 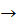 C2H5OH + KOH
C2H5OH + KOH
*Спирти – слабші кислоти, ніж вода, оскільки алкільний радикал збільшує електронну густину на атомі Оксигену та зменшує полярність зв’язку O – H. Тому в результаті взаємодії спиртів з лугами алкоголяти практично не утворюються:
C2H5OH + NaOH? C2H5ONa + H2O
(Рівновага цієї реакції зміщена ліворуч, оскільки солі спиртів у воді гідролізуються.)
Кислотність одноатомних спиртів зменшується в ряду:
CH3OH 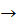 первинний
первинний 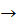 вторинний
вторинний 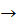 третинний.
третинний.
Утворення естерів
Спирти вступають у реакції з мінеральними й органічними кислотами, утворюючи естери. Реакція є оборотною (зворотний процес – гідроліз естерів).
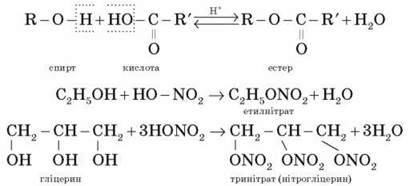
Реакційна здатність одноатомних спиртів у цих реакціях зменшується від первинних до третинних.
Окиснення
Часто використовуються окисники KMNO4, (K2Cr2O7 + H2SO4), (O2 + каталізатор). Легкість окиснення спиртів зменшується в ряду:
Первинні > вторинні >> третинні.
Первинні спирти внаслідок окиснення утворюють альдегіди, які потім легко окислюються до карбонових кислот.
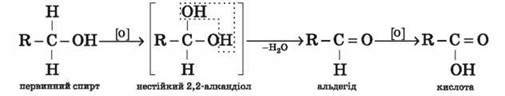
У результаті окиснення вторинних спиртів утворюються кетони.
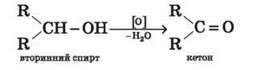
Третинні спирти більш стійкі до дії окисників. Вони окислюються лише за жорстких умов (кисле середовище, підвищена температура), що призводить до руйнування карбонового скелета молекули й утворення суміші продуктів (карбонових кислот і кетонів з меншою молекулярною масою).
Граничне окиснення спиртів до CO2 і H2O відбувається в результаті їх горіння, наприклад:
2CH3 + 3O2 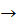 2CO2 + 4H2O
2CO2 + 4H2O
Повне окиснення метанолу відбувається за схемою:
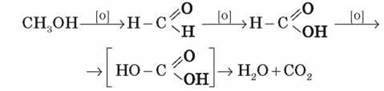
У процесі згоряння спиртів виділяється велика кількість тепла.
C2H5OH + 3O2 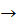 2CO2 + 3H2O +1370 кДж
2CO2 + 3H2O +1370 кДж
Через високу екзотермічність реакції горіння етанолу його вважають перспективним і екологічно чистим замінником бензинового палива у двигунах внутрішнього згоряння. У лабораторній практиці етанол застосовується як пальне для спиртівок.
Реакції заміщення ОН-групи
Заміщення гідроксилу – ОН на галоген відбувається в реакції спиртів з галогеноводнями в присутності каталізатора – сильної мінеральної кислоти (наприклад, концентрованої H2SO4). При цьому спирти проявляють властивості слабких основ.
Демонстрація 3. Взаємодія етанолу з гідроген бромідом
Ця реакція є одним зі способів одержання галогеноводнів.
Реакції дегідратації спиртів
Відщеплення води від молекул спирту (дегідратація спиртів) залежно від умов відбувається як внутрішньо-молекулярна або міжмолекулярна реакція.
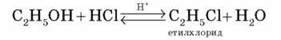
1. Внутрішньо-молекулярна дегідратація спиртів з утворенням алкенів перебігає в присутності концентрованої сульфатної кислоти за підвищеної температури.

У тих випадках, коли можливі два напрями реакції, наприклад:
Дегідратація відбувається переважно в напрямі I, тобто за правилом Зайцева – з утворенням більш заміщеного алкену (водень відщеплюється від менш гідрогенізованого атома Карбону).
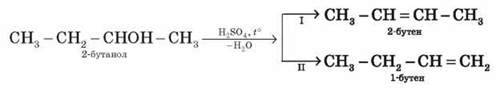
2. Міжмолекулярна дегідратація спиртів з утворенням етерів відбувається за більш низької температури, ніж внутрішньо-молекулярна реакція:
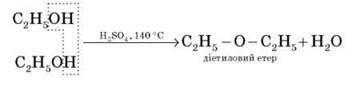
3. Одержання спиртів
1) У промисловості
Метанол синтезують із синтезу-газу на каталізаторі (Zn, Сu) за температури 250 °С і тиску 510 МПа:
CO + 2H2 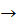 CH3OH
CH3OH
Раніше метанол одержували шляхом сухої перегонки деревини без доступу повітря.
Етанол одержують:
– гідратацією етилену (H3PO4, 280 °С, 8 МПа):
CH2 = CH2 + H2O 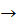 CH3 – CH2 – OH
CH3 – CH2 – OH
– бродіння крохмалю (або целюлози):

(Джерело крохмалю – зерно, картопля)
2) У лабораторії
– Гідратація алкенів (відповідно до правила Марковнікова):
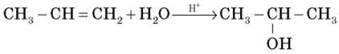
– Гідроліз галогенопохідних вуглеводнів:
CH3 – CH2 – Br + H2O 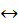 CH3 – CH2 – OH + HBr
CH3 – CH2 – OH + HBr
IV. Творче застосування одержаних знань
Складіть рівняння:
А) взаємодії 1-бутанолу з металевим натрієм і кальцієм;
Б) молекулярної дегідратації 2-пропанолу;
В) взаємодії 2-бутанолу з гідроген бромідом;
Г) внутрішньомолекулярної дегідратації 1-пентанолу;
Д) одержання пропанолу з 2-хлорпропану;
Е) одержання 1-пентанолу з 1-пентену.
V. оцінювання роботи учнів на уроці
VI. Домашнє завдання
Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи.
Творче завдання: підготувати повідомлення (презентації) про застосування спиртів.
