Загальні хімічні властивості металів – Загальні відомості про металічні елементи та метали
ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання
РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ
8. Металічні елементи та їхні сполуки. Метали
8.1. Загальні відомості про металічні елементи та метали
8.1.3. Загальні хімічні властивості металів
Найтиповіша ознака металічних елементів – це здатність відносно легко віддавати електрони:
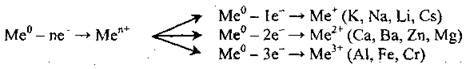
1. Взаємодія металів з простими речовинами (неметалами):
А) з галогенами. Утворюються відповідні солі – галогеніди:
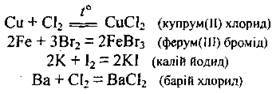
Б)
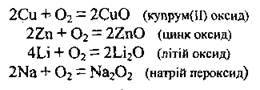
В) з азотом:
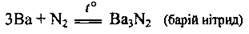
Г) з фосфором:
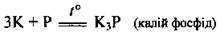
Г) із сіркою:
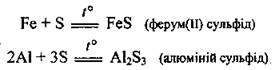
Д) з воднем. Найактивніші метали сполучаються з воднем, утворюючи гідриди:
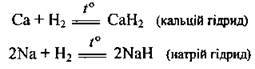
Е) з вуглецем. Утворюються карбіди:
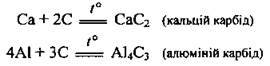
2. Реакції металів з водою. Хімічна активність металів у реакціях з водою визначається їхнім розміщенням у ряду активності металів. За звичайних умов з водою реагують лише найактивніші метали (лужні
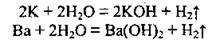
Зауважимо, що в аналогічні реакції можуть вступати магній (при нагріванні) і алюміній (після зняття оксидної плівки). За дуже високої температури з водою (водяною парою) взаємодіють деякі менш активні метали (цинк, залізо). Під час таких реакцій утворюються не гідроксиди, а оксиди:
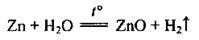
3. Реакції металів з кислотами. Хімічна активність металів у реакціях з розчинами кислот також визначається розміщенням металу у витискувальному ряді. Метали, які розміщені ліворуч від водню, взаємодіють з такими кислотами, як хлоридна НСl, фосфатна Н3РO4, сульфатна H2SO4 (розбавлена). Утворюється сіль і виділяється водень.
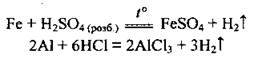
Ті ж метали, які розміщуються після водню, з наведеними кислотами не реагують.
Зауважимо, що розбавлена нітратна і концентрована сульфатна кислоти є сильними окисниками, а тому вони реагують з металами, які в ряду активності металів розміщені зліва і справа від водню, але водень у цих реакціях не виділяється:
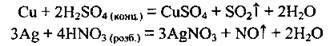
4. Взаємодія металів із солями. Для встановлення можливості реакції між металом і сіллю (розчин) також використовують ряд активності металів. Реакція відбувається, якщо метал-реагент є активнішим (тобто у ряду активності розміщується лівіше), ніж метал, який утворюється (продукт реакції):
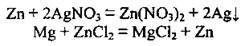
5. Взаємодія металів з лугами. З лугами взаємодіють лише ті метали, яким відповідають амфотерні оксиди і гідроксиди (алюміній Аl, цинк Zn, олово Sn…). Такі реакції можуть відбуватися з використанням не лише водного розчину, а й розплаву лугу:
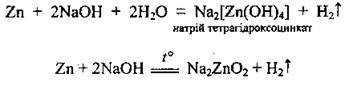




 (1 votes, average: 5.00 out of 5)
(1 votes, average: 5.00 out of 5)Related posts:
- Хімічні властивості металів – Метали Хімія Неорганічна хімія Метали Хімічні властивості металів Метали розрізняються між собою хімічною активністю, тобто здатністю вступати в хімічні реакції. Їх можна розташувати в ряд за зменшенням активності (див. таблицю). Метали – відновники. Отже, вони вступатимуть у хімічні реакції з окисниками. 1) Взаємодія з простими речовинами – неметалами (див. таблицю). 2) Взаємодія з кислотами. Метали, що […]...
- Загальні хімічні властивості металів – ЗАГАЛЬНА ХАРАКТЕРИСТИКА МЕТАЛІВ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ЗАГАЛЬНА ХАРАКТЕРИСТИКА МЕТАЛІВ Загальні хімічні властивості металів В атомах металів на зовнішній електронній оболонці утримується невелике число електронів. Ці електрони порівняно легко можуть відриватися від атомів. Така особливість металів є причиною не тільки їхніх фізичних, але й хімічних властивостей. Виходячи з того, що […]...
- ХІМІЧНІ ВЛАСТИВОСТІ ЛУЖНИХ МЕТАЛІВ – ЛУЖНІ МЕТАЛИ Хімія – універсальний довідник ЛУЖНІ МЕТАЛИ ХІМІЧНІ ВЛАСТИВОСТІ ЛУЖНИХ МЕТАЛІВ Лужні метали – хімічно дуже активні речовини. На повітрі вони швидко реагують з його складовими частинами. В результаті утвориться суміш речовин, що покривають поверхню металу товстим пухким шаром, тому лужні метали зберігають у рідинах, що не реагують з ними, наприклад, у гасі. Лужні метали бурхливо […]...
- Фізичні властивості металів – Загальні відомості про металічні елементи та метали ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 8. Металічні елементи та їхні сполуки. Метали 8.1. Загальні відомості про металічні елементи та метали 8.1.2. Фізичні властивості металів Особливості металічного зв’язку і кристалічних граток зумовлюють загальні фізичні властивості різних металів. 1. Агрегатний стан металів твердий (крім ртуті й, умовно, францію1). Температура плавлення […]...
- Загальні способи добування металів – Загальні відомості про металічні елементи та метали ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 8. Металічні елементи та їхні сполуки. Метали 8.1. Загальні відомості про металічні елементи та метали 8.1.5. Загальні способи добування металів У вигляді самородних металів трапляється незначна кількість малоактивних металів: золото, платина, срібло. Більшість металічних елементів трапляється в природі у вигляді сполук – оксидів, […]...
- Корозія металів – Загальні відомості про металічні елементи та метали ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 8. Металічні елементи та їхні сполуки. Метали 8.1. Загальні відомості про металічні елементи та метали 8.1.4. Корозія Металів Корозія (від лат. corrosio – роз’їдання) – це самовільний процес руйнування металів при взаємодії з навколишнім середовищем. Розрізняють кілька видів корозії, з яких найважливішими є […]...
- Хімічні властивості металів – ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 12. ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ § 12.3. Хімічні властивості металів Атоми металів порівняно легко віддають валентні електрони і перетворюються на позитивно заряджені іони. Тому метали є відновниками. В цьому, власне, і полягає їх головна і найзагальніша хімічна властивість. Рис. 12.2. Криві температур […]...
- ХІМІЧНІ ВЛАСТИВОСТІ ВОДИ – ВОДА. ВОДНІ РОЗЧИНИ Хімія – універсальний довідник ВОДА. ВОДНІ РОЗЧИНИ ХІМІЧНІ ВЛАСТИВОСТІ ВОДИ Вода реагує з багатьма металами. З найбільш активними металами (у таблиці Д. І. Менделєєва вони знаходяться в 1А і НА групах) відбуваються реакції типу: З менш активними металами вода реагує лише за високих температур (при цьому вона, зазвичай, знаходиться в газоподібному стані). У результаті реакції […]...
- Характерні хімічні властивості металів ІІ семестр Тема 2. МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ (13 годин) УРОК 24 Тема уроку. Характерні хімічні властивості металів Цілі уроку: ознайомити учнів із загальними хімічними властивостями металів, рядом активності металів; показати взаємозв’язок між хімічними властивостями металів та будовою їхніх атомів; розвивати навички складання рівнянь окисно-відновних реакцій і реакцій іонного обміну на прикладі хімічних властивостей […]...
- ЗАГАЛЬНІ ХІМІЧНІ ВЛАСТИВОСТІ МЕТАЛІВ. КОРОЗІЯ МЕТАЛІВ ТА ЇХ ЗАХИСТ ВІД КОРОЗІЇ ТЕМА 2. МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ УРОК 3. ЗАГАЛЬНІ ХІМІЧНІ ВЛАСТИВОСТІ МЕТАЛІВ. КОРОЗІЯ МЕТАЛІВ ТА ЇХ ЗАХИСТ ВІД КОРОЗІЇ Цілі: вивчити загальні хімічні властивості металів; мати уявлення про корозію металів і способи захисту металів від корозії; вміти складати рівняння хімічних реакцій, що ілюструють хімічні властивості металів і суть корозії металів, складати рівняння реакцій з […]...
- Сплави на основі заліза (чавун, сталь) – Загальні відомості про металічні елементи та метали ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 8. Металічні елементи та їхні сполуки. Метали 8.1. Загальні відомості про металічні елементи та метали 8.1.6. Сплави на основі заліза (чавун, сталь) Чавун і сталь – це сплави на основі заліза. Цикл чорної металургії включає в себе: – чавунно-доменне виробництво1; – виробництво сталі […]...
- Електронна будова атомів металічних елементів – Загальні відомості про металічні елементи та метали ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 8. Металічні елементи та їхні сполуки. Метали 8.1. Загальні відомості про металічні елементи та метали Металічних елементів більше, ніж неметалічних: зі 118 відомих на початок 2012 р. елементів понад 90 – металічні. Усі металічні елементи утворюють прості речовини – метали. 8.1.1. Електронна будова […]...
- ЗАГАЛЬНІ ФІЗИЧНІ ВЛАСТИВОСТІ МЕТАЛІВ. ПОШИРЕНІСТЬ МЕТАЛІЧНИХ ЕЛЕМЕНТІВ ТА ЇХНІХ СПОЛУК У ПРИРОДІ. МЕТАЛІЧНІ РУДИ. ЗАГАЛЬНІ МЕТОДИ ДОБУВАННЯ МЕТАЛІВ ТЕМА 2. МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ УРОК 2. ЗАГАЛЬНІ ФІЗИЧНІ ВЛАСТИВОСТІ МЕТАЛІВ. ПОШИРЕНІСТЬ МЕТАЛІЧНИХ ЕЛЕМЕНТІВ ТА ЇХНІХ СПОЛУК У ПРИРОДІ. МЕТАЛІЧНІ РУДИ. ЗАГАЛЬНІ МЕТОДИ ДОБУВАННЯ МЕТАЛІВ Цілі: вивчити загальні фізичні властивості металів; поширеність металічних елементів та їхніх сполук у природі; металічні руди й загальні методи добування металів; уміти пояснювати фізичні властивості металів з точки […]...
- Витискувальний ряд металів – ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК Витискувальний ряд металів Поняття про витискувальний ряд Металів У багатьох хімічних реакціях беруть участь прості речовини, зокрема метали. Однак різні метали проявляють різну активність у хімічних взаємодіях, і від цього залежить, буде протікати реакція чи ні. Чим більша активність […]...
- РЯД АКТИВНОСТІ МЕТАЛІВ – ХІМІЯ МЕТАЛІЧНИХ ЕЛЕМЕНТІВ Хімія – універсальний довідник ХІМІЯ МЕТАЛІЧНИХ ЕЛЕМЕНТІВ РЯД АКТИВНОСТІ МЕТАЛІВ За числовим значенням своєї відновної здатності всі метали можуть бути розташовані в ряд, який називається р я д о м активності мета л і в. Його називають ще електрохімічним рядом, підкреслюючи тим самим, що, вступаючи в хімічну реакцію, метал віддає електрони – носії електричного струму. […]...
- Метали та сплави в техніці – ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 12. ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ § 12.4. Метали та сплави в техніці Сплавами називаються системи, що складаються з двох і більше металів, а також металів і неметалів. Властивості сплавів дуже різноманітні і відрізняються від властивостей вихідних компонентів. Так, наприклад, сплав, що складається […]...
- Металічні елементи в природі. Загальні способи одержання металів. Виробництво чавуну та сталі ІІ семестр Тема 2. МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ (13 годин) УРОК 25 Тема уроку. Металічні елементи в природі. Загальні способи одержання металів. Виробництво чавуну та сталі Цілі уроку: ознайомити учнів з поширенням металів у природі, основними способами одержання металів, реакціями, покладеними в основу одержання металів; ознайомити з основними принципами доменного виробництва; показати взаємозв’язок між […]...
- Хімічні властивості оксидів – ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК Хімічні властивості оксидів Основні Амфотерні Кислотні Взаємодіють із кислотами з утворенням солі та води: СаО + 2НСl → СаСl2 + Н2O Взаємодіють із кислотами та основами з утворенням солі й води: ZnO + 2НСl → ZnCl2 + Н2O; ZnO […]...
- Основні способи добування металів – ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 12. ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ § 12.6. Основні способи добування металів Метали трапляються в природі як у вільному стані (самородні метали), так і, переважно, у вигляді хімічних сполук. У вигляді самородних металів перебувають найменш активні метали. Типовими їх представниками є золото і […]...
- Фізичні властивості металів – Метали Хімія Неорганічна хімія Метали Фізичні властивості металів Пластичність. Механічна дія на кристал із металічним зв’язком викликає зсув шарів атомів, але завдяки переміщенню валентних електронів по всьому зразку металу розриву зв’язків не відбувається. Найпластичніший метал – золото. Марганець і бісмут – крихкі метали. Металічний блиск, непрозорість. Вільні електрони взаємодіють із квантами світла, які падають на метал. […]...
- Ряд стандартних електродних потенціалів – ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 12. ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ § 12.5. Ряд стандартних електродних потенціалів У середній школі ви вивчаєте електрохімічний ряд напруг металів. Більш точна назва його – ряд стандартних електродних потенціалів металів. Для деяких металів він наведений у табл. 12.1. Як же складається такий […]...
- Натрій і Калій як представники лужних металів – Метали Хімія Неорганічна хімія Метали Натрій і Калій як представники лужних металів Лужні метали Розміщені в IА групі (у I групі головної підгрупи) Періодичної системи. На зовнішньому енергетичному рівні у лужних металів розміщений один неспарений електрон, який легко віддається окисникам. Ступінь окиснення лужних металів у сполуках дорівнює +1. Електронна конфігурація атома Натрію: Електронна конфігурація атома Калію: […]...
- Положення металів у періодичній системі елементів Д. І. Менделєєва – ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 12. ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ § 12.1. Положення металів у періодичній системі елементів Д. І. Менделєєва Якщо в періодичній системі елементів Д. І. Менделєєва провести діагональ від берилію до астату, то праворуч угорі від діагоналі будуть елементи-неметали (виключаючи елементи побічних підгруп), а […]...
- Ряд електрохімічних потенціалів металів ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 6. Суміші речовин. Розчини 6.12. Ряд електрохімічних потенціалів металів Порівняльну активність металів в окисно-відновних реакціях, які відбуваються у водних розчинах речовин, характеризує електрохімічний ряд напруг металів (ряд електрохімічних потенціалів, витискувальний ряд, ряд активності). Електрохімічний ряд напруг – це розташування металів у послідовності збільшення […]...
- ПРОСТІ РЕЧОВИНИ. МЕТАЛИ Й НЕМЕТАЛИ, МЕТАЛІЧНІ Й НЕМЕТАЛІЧНІ ЕЛЕМЕНТИ № 1. Прості речовини – це речовини, молекули яких складаються з елементів одного виду атомів. Залізо, алюміній, мідь, водень, кисень. № 2. Прості речовини поділяються на метали та неметали. До металів належать цинк Zn, калій К, кальцій Са, магній Mg, олово Sn, свинець Рb, мідь Сu, залізо Fe, алюміній Аl, срібло Ag, золото Аu. Прикладами […]...
- Загальні способи добування металів – ЗАГАЛЬНА ХАРАКТЕРИСТИКА МЕТАЛІВ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ЗАГАЛЬНА ХАРАКТЕРИСТИКА МЕТАЛІВ Загальні способи добування металів Лабораторні методи добування А) відновлення оксидів металів воднем; таким способом зазвичай добувають не дуже активні метали, які не взаємодіють із воднем: Б) розкладання оксидів важких металів: В) витіснення металів з їхніх солей більш активними металами: Добування […]...
- Тема 17. Загальні відомості про метали Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА ІІ ЗАВДАННЯ ДЛЯ ПЕРЕВІРКИ ЗНАНЬ НЕОРГАНІЧНА ХІМІЯ Тема 17. Загальні відомості про метали Серед чотирьох наведених варіантів відповідей виберіть одну правильну 1. Установіть послідовність зростання металічних властивостей елементів: A. Аргентум; Б. Стронцій; B. Йод; Г. Станум. 2. Позначте твердження, що характеризує більшість металів за звичайних умов: […]...
- Загальна характеристика лужних металів – ДЕЯКІ ПРЕДСТАВНИКИ МЕТАЛІВ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ДЕЯКІ ПРЕДСТАВНИКИ МЕТАЛІВ Загальна характеристика Лужних металів Будова атомів лужних металів У зовнішньому електронному шарі атоми лужних металів мають по одному електрону. У передзовнішньому електронному шарі в атома Літію 2 електрони, а в атомів інших металів по 8 електронів. Однакова будова не тільки […]...
- Фізичні й хімічні властивості кислот Тема 2 ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК УРОК 18 Тема. Фізичні й хімічні властивості кислот Цілі уроку: ознайомити учнів з фізичними й хімічними властивостями кислот; розширити знання учнів про реакції заміщення й обміну на прикладі хімічних властивостей кислот, їх взаємодії з металами, основними оксидами, основами й солями; розвивати навички складання рівнянь хімічних реакцій на прикладі хімічних […]...
- Корозія металів – ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 12. ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ § 12.7. Корозія металів Під час експлуатації виробів з металів та їх сплавів доводиться стикатися з явищем руйнування їх під дією навко яишнього середовища. Руйнування металів і сплавів внаслідок взаємодії їх з навколишнім середовищем називається корозією. Корозія […]...
- Загальні фізичні властивості металів – ЗАГАЛЬНА ХАРАКТЕРИСТИКА МЕТАЛІВ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ЗАГАЛЬНА ХАРАКТЕРИСТИКА МЕТАЛІВ Загальні фізичні властивості металів Металічні елементи займають в основному ліву нижню частину Періодичної системи хімічних елементів Д, І. Менделєєва. До металічних елементів належать ті елементи, в чиїх атомах на зовнішньому електронному рівні перебуває невелике (від одного до чотирьох) число електронів, […]...
- Фізичні властивості металів – ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 12. ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ § 12.2. Фізичні властивості металів Механічна дія на кристал з ковалентним зв’язком спричиняє зміщення окремих шарів атомів, внаслідок чого зв’язки розриваються і кристал руйнується (рис. 12.1, а). Така сама дія на кристал з металічним зв’язком також спричиняє […]...
- Контрольна робота з теми “Металічні елементи та їхні сполуки” ІІ семестр Тема 2. МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ (13 годин) УРОК 34 Контрольна робота з теми “Металічні елементи та їхні сполуки” Цілі уроку: узагальнити й систематизувати знання учнів з теми “Металічні елементи та їхні сполуки”; визначити рівень навчальних досягнень учнів з теми, розуміння основних понять, уміння використовувати їх на практиці. Тип уроку: контролю й […]...
- МЕТАЛІЧНІ ВЛАСТИВОСТІ – ХІМІЯ МЕТАЛІЧНИХ ЕЛЕМЕНТІВ Хімія – універсальний довідник ХІМІЯ МЕТАЛІЧНИХ ЕЛЕМЕНТІВ МЕТАЛІЧНІ ВЛАСТИВОСТІ Застосування металів як таких базується саме на їх металічних властивостях. Мова йде про металічні властивості речовин, на відміну від металічних властивостей хімічних елементів. Спільним у будові всіх речовин металів є атомна кристалічна гратка і, внаслідок незаповненості електронами зони зв’язуючих молекулярних орбіталей, здатність електронів сприймати і передавати […]...
- Елементи-метали в Періодичній системі – Метали Хімія Неорганічна хімія Метали Елементи-метали в Періодичній системі Якщо в Періодичній системі провести діагональ від Берилію до Астату, то зліва внизу розміщуватимуться елементи-метали (до них же належать елементи побічних підгруп). Атоми металів порівняно легко віддають електрони, перетворюючись на позитивно заряджені йони. Це пояснюється тим, що в атомів металів: – мале число електронів на зовнішньому енергетичному […]...
- Загальні хімічні властивості неметалів I СЕМЕСТР Тема 1. НЕМЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ (18 год.) УРОК 7 Тема уроку. Загальні хімічні властивості неметалів Цілі уроку: розвивати й поглиблювати знання учнів про неметали на прикладі їхніх хімічних властивостей (взаємодії з киснем, воднем, металами); розвивати навички й уміння порівнювати хімічні властивості різних речовин на прикладі сполук Сульфуру, Нітрогену, Фосфору, Карбону, Силіцію, […]...
- Загальні способи добування металів. Електроліз розплавів солей і лугів – Метали Хімія Неорганічна хімія Метали Загальні способи добування металів. Електроліз розплавів солей і лугів Металургія – це галузь промисловості, яка займається видобуванням металів із руд. Електроліз – окисно-відновний процес, що відбувається на електродах під час проходження електричного струму через розплав або розчин електроліту. Якщо в розплав електроліту, наприклад натрій хлориду, занурити інертні електроди й пропускати постійний […]...
- Тема 19. Лужні метали Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА ІІ ЗАВДАННЯ ДЛЯ ПЕРЕВІРКИ ЗНАНЬ НЕОРГАНІЧНА ХІМІЯ Тема 19. Лужні метали Серед чотирьох наведених варіантів відповідей виберіть одну правильну 1. Позначте номер групи періодичної системи, до якої входять лужні метали: A. І; Б. VI; B. VII; Г. IX. 2. Позначте кількість валентних електронів, що мають атоми […]...
- Лужні метали. Натрій і Калій РОЗДІЛ 3 МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХ СПОЛУКИ ХІМІЧНІ ЕЛЕМЕНТИ ІА – ІІІА ГРУП § 58. Лужні метали. Натрій і Калій Усвідомлення змісту цього параграфа дає змогу: Характеризувати фізичні та хімічні властивості, способи добування натрію і калію в промисловості; Складати рівняння реакцій, схеми електронного балансу відповідних хімічних реакцій; Обгрунтовувати застосування натрію та калію їх властивостями. Фізичні […]...
- ПРОСТІ РЕЧОВИНИ. МЕТАЛИ Й НЕМЕТАЛИ, МЕТАЛІЧНІ Й НЕМЕТАЛІЧНІ ЕЛЕМЕНТИ Тема 1 ПОЧАТКОВІ ХІМІЧНІ ПОНЯТТЯ & 14. ПРОСТІ РЕЧОВИНИ. МЕТАЛИ Й НЕМЕТАЛИ, МЕТАЛІЧНІ Й НЕМЕТАЛІЧНІ ЕЛЕМЕНТИ Вивчення параграфа допоможе вам: · наводити приклади простих речовин металів і неметалів; · розрізняти метали і неметали, металічні і неметалічні елементи; · користуватися періодичною системою як довідковою для визначення розміщення в ній деяких неметалічних і металічних хімічних елементів. ЯКІ […]...