Головна ⇒ 📌Довідник з хімії ⇒ ЕНЕРГІЯ ГІББСА – ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ
ЕНЕРГІЯ ГІББСА – ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ
Хімія – універсальний довідник
ХІМІЧНИЙ ПРОЦЕС
ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ
ЕНЕРГІЯ ГІББСА
Щоб однозначно оцінити можливість або неможливість здійснення реакції, необхідно враховувати як зміну ентальпії, так і зміну ентропії. Сумарну зміну ентальпії й ентропії для реакції при сталому тиску і температурі відображає зміна енергії Гіббса:
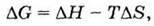
Де ΔG – зміна енергії Гіббса; Т – абсолютна температура.
У цьому рівнянні член ΔН характеризує ентальпійний фактор, а член ТΔS – ентропійний фактор проходження реакції.
Зменшення енергії Гіббса процесу (ΔG < 0) свідчить про його принципову можливість. Збільшення ж енергії Гіббса (ΔG > 0) вказує на неможливість самовільної реакції за даних умов.
Related posts:
- ЕНЕРГІЯ ГІББСА. УТВОРЕННЯ РЕЧОВИНИ – ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ ЕНЕРГІЯ ГІББСА. УТВОРЕННЯ РЕЧОВИНИ Стандартною молярною енергією Гіббса утворення речовини ΔG°УТB<298 називають зміну енергії Гіббса при утворенні 1 моль речовини з простих речовин у стандартних умовах. Стандартна молярна енергія Гіббса утворення простої речовини, стійкої у стандартних умовах, дорівнює нулю. Одиниця виміру енергії Гіббса утворення речовини – […]...
- ЕНТАЛЬПІЙНИЙ І ЕНТРОПІЙНИЙ ФАКТОРИ І НАПРЯМОК ХІМІЧНОЇ РЕАКЦІЇ – ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ ЕНТАЛЬПІЙНИЙ І ЕНТРОПІЙНИЙ ФАКТОРИ І НАПРЯМОК ХІМІЧНОЇ РЕАКЦІЇ Згідно з рівнянням Можливість реакції Визначає ентальпійний фактор: ΔH < 0. Можливість реакції Визначає ентропійний фактор: TΔS > 0. Реакція протікає за високої температури....
- ТЕПЛОВИЙ ЕФЕКТ РЕАКЦІЇ. ЕНТАЛЬПІЯ РЕАКЦІЇ – ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ ТЕПЛОВИЙ ЕФЕКТ РЕАКЦІЇ. ЕНТАЛЬПІЯ РЕАКЦІЇ Кількість теплоти Q, яку передали системі, йде на зміну її внутрішньої енергії ΔUі на здійснення системою роботи* W проти зовнішніх сил (зовнішнього тиску р) (рис. 32): Рис. 32. Робота, яку виконує хімічна система проти зовнішнього тиску (поршень невагомий). Вуглекислий газ, який […]...
- СУТНІСТЬ ХІМІЧНОГО ПЕРЕТВОРЕННЯ – ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ СУТНІСТЬ ХІМІЧНОГО ПЕРЕТВОРЕННЯ Хімія вивчає перетворення речовин, які супроводжуються зміною їх складу і (або) будови. Наприклад: Суть хімічної реакції – перегрупування атомів, яке супроводжується розривом хімічних зв’язків у вихідних речовинах і утворенням хімічних зв’язків у продуктах реакції. Хімічна реакція супроводжується енергетичними змінами, тому що під час […]...
- ВПЛИВ ТЕМПЕРАТУРИ НА НАПРЯМОК ХІМІЧНОЇ РЕАКЦІЇ – ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ ВПЛИВ ТЕМПЕРАТУРИ НА НАПРЯМОК ХІМІЧНОЇ РЕАКЦІЇ Згідно з рівнянням На значення ΔG великий вплив має температура. Цей вплив визначається знаком і величиною ΔS. При ΔS > 0 з підвищенням температури (збільшенням Т) негативне значення ΔG буде зменшуватися, а при ΔS < 0 – збільшуватися. Приклад реакції, […]...
- ЕНТРОПІЯ – ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ ЕНТРОПІЯ Ентропію можна охарактеризувати, як ступінь безладдя (невпорядкованості) системи. Ентропію речовини прийнято відносити до стандартних умов: до тиску р = 101 325 Па (1 атм) і, зазвичай, до температури 298 К (25 °С). Ентропія 1 моль речовини у стандартному стані називається стандартною молярною ентропією. Її позначають […]...
- ЗАКОН ГЕССА. РОЗРАХУНОК ЕНТАЛЬПІЇ ХІМІЧНОЇ РЕАКЦІЇ – ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ ЗАКОН ГЕССА. РОЗРАХУНОК ЕНТАЛЬПІЇ ХІМІЧНОЇ РЕАКЦІЇ Тепловий ефект реакції залежить від початкового і кінцевого станів системи і не залежить від шляху реакції (закон Гесса). Наприклад: Кількість теплоти, яка виділяється під час спалювання метану СН4, не залежить від того, протікає реакція за одну стадію чи за дві […]...
- Вільна енергія реакції Гіббса – Рушійна сила хімічних реакцій ЕНЕРГЕТИКА ХІМІЧНИХ РЕАКЦІЙ 3. Рушійна сила хімічних реакцій 3.4. Вільна енергія реакції Гіббса Кожна реакція характеризується двома тенденціями: – система речовин прагне перейти у стан з якомога меншою ентальпією; – система речовин прагне перейти в стан з якомога більшою ентропією. Тому реакція Проходить самочинно в той бік, де знижується ентальпія реакції і зростає її ентропія. […]...
- Енергетичний ефект хімічних реакцій Хімія Загальна хімія Хімічні реакції Енергетичний ефект хімічних реакцій Хімічні реакції завжди супроводжуються виділенням або поглинанням енергії. Кількість виділеної або поглиненої енергії називається тепловим ефектом хімічної реакції (Q). Реакції, що супроводжуються виділенням енергії, називаються екзотермічнимИ, поглинанням енергії, – ендотермічнимИ. Хімічні рівняння, в яких наводяться теплові ефекти хімічних реакцій, називаються ТермохімічнимИ, наприклад: У цьому рівнянні зазначені […]...
- Енергія активації ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 4. ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ. § 4.3. Енергія активації Значну зміну швидкості реакції зі зміною температури пояснює теорія активації. Згідно з цією теорією в хімічну взаємодію вступають тільки активні молекули (частинки), що мають енергію, достатню для здійснення даної реакції. Неактивні частинки можна […]...
- Ентропія реакції – Рушійна сила хімічних реакцій ЕНЕРГЕТИКА ХІМІЧНИХ РЕАКЦІЙ 3. Рушійна сила хімічних реакцій 3.3. Ентропія реакції У кожній реакції впорядкований стан системи змінюється і, отже, змінюється ентропія. Зміна ентропії реакції ∆SR, як і ентальпії реакції, визначається як різниця суми ентропій продуктів реакції і суми ентропій початкових речовин: Приклад. Під час реакції газоподібного гідроген хлориду з газоподібним амоніаком з двох “невпорядкованих” […]...
- ЕНЕРГІЯ (МІЦНІСТЬ) І ДОВЖИНА ХІМІЧНОГО ЗВ’ЯЗКУ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ ХІМІЧНИЙ ЗВ’ЯЗОК ЕНЕРГІЯ (МІЦНІСТЬ) І ДОВЖИНА ХІМІЧНОГО ЗВ’ЯЗКУ Енергія хімічного зв’язку – це енергія, необхідна для роз’єднання атомів і віддалення їх на таку відстань, на якій вони вже не відчувають сили притягування один до одного. Довжина зв’язку – відстань між ядрами атомів, що утворюють хімічний зв’язок....
- Внутрішня енергія кристалічних речовин – Зміна енергії при кристалізації і розчиненні ЕНЕРГЕТИКА ХІМІЧНИХ РЕАКЦІЙ 2 . Зміна енергії при кристалізації і розчиненні У твердому агрегатному стані речовини утворюють, як правило, гратку, в якій частинки впорядковано сполучені між собою. Взаємодія між іонами обумовлена кулонівськими силами, між молекулами – вандерваальсовими силами. 2.1. Внутрішня енергія кристалічних речовин Утворення кристалічної гратки зі складових частинок – це екзотермічний процес. Енергію, яка […]...
- Енергія в проміжних реакціях – Перетворення енергії в хімічних реакціях ЕНЕРГЕТИКА ХІМІЧНИХ РЕАКЦІЙ 1 . Перетворення енергії в хімічних реакціях 1.4 . Енергія в проміжних реакціях Часто зустрічаються реакції, зміну енергії яких експериментально важко або взагалі неможливо визначити. Проте непрямим шляхом ця проблема вирішується: – шукана реакція поділяється на низку проміжних стадій, ентальпія реакцій яких відома; – шукана реакція є однією з проміжних реакцій, сума […]...
- Ентальпія реакції – Перетворення енергії в хімічних реакціях ЕНЕРГЕТИКА ХІМІЧНИХ РЕАКЦІЙ 1 . Перетворення енергії в хімічних реакціях 1.3 . Ентальпія реакції Енергію, що виділилася або була поглинута в ході хімічної реакції, називають ентальпією реакції ∆HR або тепловим ефектом реакції. Значення цієї енергії легко визначити, якщо відомі ентальпії утворення ∆Hf відповідних речовин, що беруть участь у реакції. Тепловим ефектом реакції є різниця енергії […]...
- РЕАКЦІЇ ОБМІНУ – ТИПИ ХІМІЧНИХ РЕАКЦІЙ Хімія – універсальний довідник ТИПИ ХІМІЧНИХ РЕАКЦІЙ РЕАКЦІЇ ОБМІНУ Реакції між складними хімічними речовинами, в результаті яких відбувається обмін між ними окремими атомами або групами атомів, називаються реакціями обміну. Наприклад: Реакції обміну (крім сильно екзотермічної реакції нейтралізації) зазвичай супроводжуються невеликим тепловим ефектом, тобто відбувається лише невелика зміна внутрішньої енергії системи, і вона не може бути […]...
- Механічна енергія. Робота і енергія ЗАСТОСУВАННЯ ЗАКОНІВ ДИНАМІКИ Урок № 17 Тема. Механічна енергія. Робота і енергія Мета: розкрити учням сутність поняття енергії як фізичної величини, яка описує стан тіла і зміна якої визначає роботу. Тип уроку: комбінований. План уроку Контроль знань 15 хв. 1. Що таке переміщення? 2. Що таке сила? 3. Чи правильне твердження: переміщення тіла визначається тільки […]...
- Каталіз ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ 4. Каталіз Багато реакцій, які відповідно до енергетичних передумов повинні відбуватися спонтанно, не починаються або проходять дуже повільно. Приклад. Для процесу утворення газоподібної води з водню і кисню при 25 °С енергія Гіббса реакції ∆G°298 = -229 кДж/моль. Проте суміш водню і кисню може зберігатися як завгодно довго, реакція за цих умов […]...
- Внутрішня енергія тіл. Два способи зміни внутрішньої енергії ОСНОВИ ТЕРМОДИНАМІКИ * Урок № 1 Тема. Внутрішня енергія тіл. Два способи зміни внутрішньої енергії Мета: дати молекулярно-кінетичне трактування поняття внутрішньої енергії та способів зміни внутрішньої енергії; розвивати логічне мислення, вміння аналізувати, робити висновки. Тип уроку: урок вивчення нового матеріалу. Демонстрації: залежність між об’ємом, тиском і температурою; зміна внутрішньої енергії тіла внаслідок виконання роботи. ХІД […]...
- ЕНЕРГІЯ АКТИВАЦІЇ – ХІМІЧНА КІНЕТИКА. ШВИДКІСТЬ І МЕХАНІЗМ ХІМІЧНИХ РЕАКЦІЙ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ХІМІЧНА КІНЕТИКА. ШВИДКІСТЬ І МЕХАНІЗМ ХІМІЧНИХ РЕАКЦІЙ ЕНЕРГІЯ АКТИВАЦІЇ Енергія активації Еа – надлишкова енергія, яку повинні мати молекули, щоб у результаті їхнього зіткнення відбулася хімічна реакція. Хімічна реакція Здійснюється через утворення активованого комплексу А2 … В2, в якому відбувається перегрупування атомів (рис. 44): Рис. 44. Енергетична схема проходження […]...
- ЗАКОН ЗБЕРЕЖЕННЯ МАСИ Хімія – універсальний довідник КІЛЬКІСНІ ВІДНОШЕННЯ В ХІМІЇ ЗАКОН ЗБЕРЕЖЕННЯ МАСИ Рівняння хімічної реакції – це, фактично, рівняння матеріального балансу речовин, що вступили в реакцію, і продуктів реакції, тобто рівність їхніх мас. Дійсно, число атомів кожного елемента зліва і справа в рівнянні реакції те ж саме, адже атоми в хімічних реакціях не виникають і не […]...
- Енергія. Потенціальна і кінетична енергія РОЗДІЛ III МЕХАНІЧНА РОБОТА. ЕНЕРГІЯ УРОК № 8/42 Тема уроку. Енергія. Потенціальна і кінетична енергія Тип уроку: засвоєння нових знань. Мета уроку: ввести поняття про фундаментальну характеристику руху й взаємодію тіл – енергію; навчити описувати фізичні явища, використовуючи закони збереження; формувати вміння учнів спостерігати, аналізувати та описувати фізичні явища. Обладнання: гиря, встановлена на стиснутій пружині; […]...
- Умовні позначення, назви та одиниці фізичних величин ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ ДОДАТОК 1. Умовні позначення, назви та одиниці фізичних величин η – Вихід продукту (масова частка виходу) – Аr – Відносна атомна маса – Mr – Відносна молекулярна маса – DH2 – Відносна густина за воднем – Dn – Відносна густина за повітрям – Х – Відносна […]...
- Умови виникнення хімічного зв’язку Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЧНИЙ ЗВ’ЯЗОК І БУДОВА РЕЧОВИНИ Умови виникнення хімічного зв’язку Хімічний зв’язок – це взаємодія атомів, здійснювана шляхом обміну електронами або їхнім переходом від одного атома до іншого. Не всі атоми можуть взаємодіяти між собою. Буває так, що при зближенні атомів та перекриванні їхніх […]...
- ЕНЕРГІЯ. ЗАКОН ЗБЕРЕЖЕННЯ ЕНЕРГІЇ. ВИДИ ЕНЕРГІЇ Фізика підготовка до ЗНО комплексне видання МЕХАНІКА 3. ЗАКОНИ ЗБЕРЕЖЕННЯ В МЕХАНІЦІ 3.4. ЕНЕРГІЯ. ЗАКОН ЗБЕРЕЖЕННЯ ЕНЕРГІЇ. ВИДИ ЕНЕРГІЇ Енергія – це єдина міра різних форм руху матерії. Енергія – одна з характерних властивостей матерії. На практиці механічний рух частково чи повністю перетворюється в інші форми – тепловий, електромагнітний рух. Енергія характеризує рух системи, а […]...
- СПОЛУЧЕННЯ АТОМІВ МІЖ СОБОЮ. УТВОРЕННЯ ХІМІЧНОГО ЗВ’ЯЗКУ Хімія – універсальний довідник БУДОВА АТОМА СПОЛУЧЕННЯ АТОМІВ МІЖ СОБОЮ. УТВОРЕННЯ ХІМІЧНОГО ЗВ’ЯЗКУ Як і чому відбувається сполучення нейтральних атомів? Почнемо пояснення з найпростішого випадку. Нехай на деякій відстані один від одного (наприклад, 0,1нм) знаходяться два протони – два ядра атома Гідрогену. У чому полягатиме їх взаємодія? Звичайно, вони будуть відштовхуватися, тому що заряджені однойменно. […]...
- БІОСФЕРА. ФОТОСИНТЕЗ Хімія – універсальний довідник ХІМІЯ І ХІМІЧНА ТЕХНОЛОГІЯ ХІМІЯ НАВКОЛИШНЬОГО СЕРЕДОВИЩА. ХІМІЧНА ЕКОЛОГІЯ. БІОСФЕРА. ФОТОСИНТЕЗ У біосфері відбувається фотосинтез органічних речовин, наприклад: Процес синтезу дуже ендотермічний, здійснюється зі зменшенням ентропії, тому може проходити лише за рахунок зовнішнього потужного джерела енергії – Сонця. Фотосинтез глюкози здійснюється за участю хлорофілу. У процесі фотосинтезу хлорофіл поглинає світлову енергію […]...
- Енергія зв’язку АТОМНА І ЯДЕРНА ФІЗИКА УРОК 9/58 Тема. Енергія зв’язку Мета уроку: увести поняття про міцність атомних ядер; з’ясувати фізичний зміст поняття “дефект мас”. Тип уроку: урок вивчення нового матеріалу. ПЛАН УРОКУ Контроль знань 3 хв. 1. Що таке ядерної реакції? Наведіть два-три приклади ядерних реакцій. 2. Які умови перебігу ядерних реакцій? Вивчення нового матеріалу 30 […]...
- Визначення – Швидкість реакції ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ 2. Швидкість реакції У ході хімічної реакції кількість початкових речовин постійно зменшується, а кількість продуктів реакції відповідно збільшується. Зміну кількості початкових речовин чи продуктів реакції за певний проміжок часу називають швидкістю реакції. 2.1. Визначення Швидкість реакції v визначається як зміна кількості п речовини за певний проміжок часу: ∆n – зміна кількості речовини […]...
- ШВИДКІСТЬ ХІМІЧНОЇ РЕАКЦІЇ – ХІМІЧНА КІНЕТИКА. ШВИДКІСТЬ І МЕХАНІЗМ ХІМІЧНИХ РЕАКЦІЙ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ХІМІЧНА КІНЕТИКА. ШВИДКІСТЬ І МЕХАНІЗМ ХІМІЧНИХ РЕАКЦІЙ ШВИДКІСТЬ ХІМІЧНОЇ РЕАКЦІЇ Швидкість і механізм хімічної реакції вивчає хімічна кінетика. Швидкість хімічної реакції характеризується зміною концентрації однієї з вихідних речовин або кінцевих продуктів за одиницю часу. Середня швидкість реакції: Де с1 і с2 – початкова і кінцева концентрація речовини; τ1 і […]...