Головна ⇒ 📌Довідник з хімії ⇒ МОЛЕКУЛЯРНІ КРИСТАЛИ – КРИСТАЛИ
МОЛЕКУЛЯРНІ КРИСТАЛИ – КРИСТАЛИ
Хімія – універсальний довідник
БУДОВА РЕЧОВИНИ
КРИСТАЛИ
МОЛЕКУЛЯРНІ КРИСТАЛИ
Прикладами речовин з молекулярними кристалічними гратками є кристали аргону (рис. 22) та йоду (рис. 23).
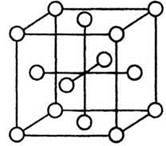
Рис. 22. Кристалічна гратка аргону (гранецентрований куб), що складається з одноатомних молекул.
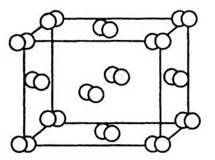
Рис. 23. Кристалічна гратка йоду(гранецентрований куб), утворена двоатомними молекулами.
Related posts:
- АТОМНО-МЕТАЛІЧНІ КРИСТАЛИ – КРИСТАЛИ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ КРИСТАЛИ АТОМНО-МЕТАЛІЧНІ КРИСТАЛИ Прикладами атомно-металічних кристалів є кристали натрію, калію, заліза, хрому, барію (рис.19), міді, алюмінію, свинцю (рис.20), цинку, кадмію, магнію (рис. 21). Рис. 19. Кубічна об’ємно-центрована кристалічна гратка. Рис. 20. Кубічна гранецентрована кристалічна гратка. Рис. 21. Гексагональна щільноупакована кристалічна гратка....
- АТОМНО-КОВАЛЕНТНІ КРИСТАЛИ – КРИСТАЛИ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ КРИСТАЛИ АТОМНО-КОВАЛЕНТНІ КРИСТАЛИ Прикладами атомно-ковалентних кристалів є кристали алмазу і кварцу. У кристалі алмазу кожен атом С утворює чотири σ-зв’язки з чотирма іншими (рис. 17). Рис. 17. Кристалічна гратка алмазу. У кристалі кварцу (оксиду силіцію SіO2) кожен атом Sі утворює чотири σ-зв’язки, кожен атом О – два σ-зв’язки (рис. […]...
- ІОННІ КРИСТАЛИ – КРИСТАЛИ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ КРИСТАЛИ ІОННІ КРИСТАЛИ Іонні кристали утворюються за рахунок електростатичної взаємодії протилежно заряджених іонів. Іонна модель кристала грунтується на тому, що енергетично найбільш вигідно, коли кожен іон оточений максимально можливою кількістю іонів із протилежним знаком. Співвідношення іонних радіусів для кристалів складу АВ визначає координаційні числа іонів. Відношення іонних радіусів Координаційні […]...
- МОЛЕКУЛЯРНІ КРИСТАЛИ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ МОЛЕКУЛЯРНІ КРИСТАЛИ Якщо проаналізувати фізичні властивості речовин, які складаються з молекул, можна дійти висновку, що речовини з молекулярною будовою мають неміцні гратки. Вони руйнуються вже за невисоких температур. Зі збільшенням молекулярної маси речовини енергія зв’язку між молекулами зростає, тому молекулярні речовини з малими молекулами плавляться (і киплять) при нижчих […]...
- ПОЛОЖЕННЯ ЕЛЕМЕНТІВ У ПЕРІОДИЧНІЙ СИСТЕМІ Д. І. МЕНДЕЛЄЄВА І СТРУКТУРА УТВОРЕННЯ НИМИ ПРОСТИХ РЕЧОВИН – КРИСТАЛИ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ КРИСТАЛИ ПОЛОЖЕННЯ ЕЛЕМЕНТІВ У ПЕРІОДИЧНІЙ СИСТЕМІ Д. І. МЕНДЕЛЄЄВА І СТРУКТУРА УТВОРЕННЯ НИМИ ПРОСТИХ РЕЧОВИН Будова простих речовин визначається числом валентних електронів (рис. 24). Рис. 24. Моделі будови простих речовин елементів третього періоду: Аргон Аr – молекула одноатомна; Хлор Сl2 – молекула двохатомна; Сірка S8 – молекула восьмиатомна; Сірка […]...
- КРИСТАЛІЧНИЙ СТАН РЕЧОВИНИ – КРИСТАЛИ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ КРИСТАЛИ КРИСТАЛІЧНИЙ СТАН РЕЧОВИНИ Кристали – тверді тіла, в яких атоми, іони або молекули утворюють впорядковану періодичну структуру. Кристалічні гратки – просторове періодичне розташування атомів, молекул або іонів у кристалі. Кристалічний стан характеризується дальнім порядком розташування частинок, що утворюють речовину. Рідина характеризується ближнім порядком, а газовий стан характеризується повного […]...
- ДЕФЕКТИ У КРИСТАЛАХ – СПОЛУКИ ЗМІННОГО СКЛАДУ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ СПОЛУКИ ЗМІННОГО СКЛАДУ ДЕФЕКТИ У КРИСТАЛАХ Сполуки сталого складу називають дальтонідами, а сполуки змінного складу – бертолідами. До сполук сталого складу належать речовини молекулярної будови, тому що склад молекул визначається будовою атомів, які їх утворюють. Кристалічні речовини атомної та іонної будови характеризуються більш-менш змінним складом (рис. 25, 26 і […]...
- IОННІ КРИСТАЛИ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ IОННІ КРИСТАЛИ Іонною будовою володіє більшість сполук металів із неметалами. У вузлах іонної кристалічної гратки можуть знаходитися не тільки прості, але і складні iони, що мають у своїй будові декілька атомів. Наприклад, кристал гідроксиду натрію NаОН складається з іонів Na+ і гідроксид-iонів ОН-. Іонними сполуками є більшість солей. Їх […]...
- ХІМІЧНИЙ ЗВ’ЯЗОК І ВЛАСТИВОСТІ КРИСТАЛІЧНИХ РЕЧОВИН – КРИСТАЛИ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ КРИСТАЛИ ХІМІЧНИЙ ЗВ’ЯЗОК І ВЛАСТИВОСТІ КРИСТАЛІЧНИХ РЕЧОВИН Властивості кристалічних речовин визначаються типом кристалічної гратки (табл. 5). Таблиця 5 Тип кристалічної гратки і властивості речовин Гратка Структурна частинка Зв’язок між частинками Температура плавлення Міцність Зв’язку Електропровідність Механічні властивості Молекулярна Молекула Міжмолекулярний Низька Мала Діелектрики Крихкість Атомно-ковалентна Атом Ковалентний Висока Велика […]...
- АТОМНІ КРИСТАЛИ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ АТОМНІ КРИСТАЛИ При побудові атомної кристалічної гратки і перекриванні АО утворюються МО, що належать усьому кристалу. Електрони на цих МО рухаються під впливом електричного поля всіх ядер кристала. Не можна сказати, якому атому належить той чи інший електрон, а тому можна говорити про делокалізацію електронів, про “газ вільних електронів”. […]...
- Кристалічні гратки. Атомні, молекулярні та іонні кристали Тема 4 ХІМІЧНИЙ ЗВ’ЯЗОК І БУДОВА РЕЧОВИНИ УРОК 59 Тема. Кристалічні гратки. Атомні, молекулярні та іонні кристали Цілі уроку: показати взаємозв’язок між будовою речовин та їх фізичними властивостями на підставі знань про типи хімічних зв’язків у неорганічних речовинах; ознайомити учнів з типами кристалічних граток (атомною, молекулярною, іонною, металевою); сформувати вміння характеризувати фізичні властивості речовин за […]...
- СПЛАВИ МЕТАЛІВ – КРИСТАЛИ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ КРИСТАЛИ СПЛАВИ МЕТАЛІВ У табл. 6 наведено найбільш поширені сплави металів. Таблиця 6 Деякі поширені сплави металів Основа Сплав Мас. частки основних компонентів Властивості Застосування Залізо Нержавіюча (хромиста) сталь 13-27% Сr Стійкість проти корозії Хімічне обладнання Залізо Нержавіюча (хромонікелева) Сталь 18% Сr, 9% Ni Стійкість проти корозії Столові прибори, […]...
- МОЛЕКУЛЯРНІ ОРБІТАЛІ. МОЛЕКУЛА Н2 Хімія – універсальний довідник БУДОВА РЕЧОВИНИ ХІМІЧНИЙ ЗВ’ЯЗОК МОЛЕКУЛЯРНІ ОРБІТАЛІ. МОЛЕКУЛА Н2 Для опису розподілу електронної густини в молекулі використовують уявлення про молекулярну орбіталь. Молекулярна орбіталь – ділянка простору в молекулі, в якій можливе перебування електрона. Знаходження електрона між атомними ядрами молекули описує зв’язуюча молекулярна орбіталь. Знаходження електрона в молекулі за атомними ядрами описує антизв’язуюча […]...
- КРИСТАЛІЧНА ГРАТКА Хімія – універсальний довідник БУДОВА РЕЧОВИНИ За даних умов речовина може знаходитися в одному з трьох агрегатних станів: твердому, рідкому або газоподібному. Існує, крім того, маловідомий, так званий рідкокристалічний стан речовини. Газоподібний стан речовини відзначається слабкою взаємодією між частинками, що утворюють газ – атомами (наприклад, у випадку інертних газів) або молекулами. КРИСТАЛІЧНА ГРАТКА Будь-яка хімічна […]...
- КРИСТАЛИ Розділ 2. БУДОВА РЕЧОВИНИ §12 . ТВЕРДІ ТІЛА 2. КРИСТАЛИ Є два типи твердих тіл – кристалічні та аморфні. Розглянемо спочатку кристалічні тіла, які часто називають кристалами. Прикладами кристалів є знайомі вам кухонна сіль і цукор. ПРОВЕДЕМО ДОСЛІД Розгляньте через збільшувальне скло кристалики солі або цукру: у них рівні, начебто спеціально зрізані, грані. Можна виростити […]...
- АЗОТ ЯК ПРОСТА РЕЧОВИНА – ХІМІЯ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ Хімія – універсальний довідник ХІМІЯ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ АЗОТ ЯК ПРОСТА РЕЧОВИНА Молекула N2 – найміцніша з усіх молекул відомих простих речовин, це – взагалі одна з найміцніших молекул (енергія хімічного зв’язку вища тільки в молекулі СО), тому у природі Нітроген знаходиться, в основному, у вигляді простої речовини N2 – однієї з основних складових частин повітря, […]...
- Рідкі кристали. Полімери 2-й семестр МОЛЕКУЛЯРНА ФІЗИКА Й ТЕРМОДИНАМІКА 1. Властивості газів, рідин, твердих тіл Урок 16/87 Тема. Рідкі кристали. Полімери Мета уроку: познайомити учнів з властивостями рідких кристалів і полімерів, розповісти про їх застосуваннях Тип уроку: вивчення нового матеріалу План уроку Контроль знань 4 хв. 1. Будова і властивість твердих тіл. 2. Кристалічні тіла. 3. Аморфні тіла. […]...
- СЕРЕДНЯ ШВИДКІСТЬ ТЕПЛОВОГО РУХУ ОДНОАТОМНИХ МОЛЕКУЛ. ДОСЛІД ШТЕРНА Фізика підготовка до ЗНО комплексне видання МОЛЕКУЛЯРНА ФІЗИКА І ТЕРМОДИНАМІКА 1. ОСНОВИ МОЛЕКУЛЯРНО-КІНЕТИЧНОЇ ТЕОРІЇ 1.7 СЕРЕДНЯ ШВИДКІСТЬ ТЕПЛОВОГО РУХУ ОДНОАТОМНИХ МОЛЕКУЛ. ДОСЛІД ШТЕРНА Середня швидкість теплового руху одноатомних молекул: – універсальна газова стала, що дорівнює добутку сталої Больцмана і сталої Авогадро: Дослід Штерна (1920) дає змогу визначити середню швидкість руху молекул експериментально за формулою Де […]...
- МОЛЕКУЛИ АЗОТУ N2, КИСНЮ O2 І ФТОРУ F2 Хімія – універсальний довідник БУДОВА РЕЧОВИНИ ХІМІЧНИЙ ЗВ’ЯЗОК МОЛЕКУЛИ АЗОТУ N2, КИСНЮ O2 І ФТОРУ F2 Енергетична діаграма орбіталей двохатомних молекул елементів другого періоду наведена на рис. 6. Рис. 6. Енергетична діаграма орбіталей двохатомних молекул s – і р-елементів. Користуючись рис. 6, можна скласти електронні конфігурації двохатомних s – і р-елементів. Електронна конфігурація Структурна Молекули […]...
- МОЛЕКУЛА МЕТАНУ СН4 І IОНА NH4+ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ ХІМІЧНИЙ ЗВ’ЯЗОК МОЛЕКУЛА МЕТАНУ СН4 І IОНА NH4+ Молекула метану має тетраедричну форму (рис. 7). Рис. 7. Взаємне розміщення атомів у молекулі метану СН4. Енергетичну діаграму орбіталей тетраедричних молекул і іонів без π-зв’язків наведено на рис.8. Рис. 8. Енергетична діаграма орбіталей тетраедричних молекул без π-зв’язків. Електронна конфігурація молекули СН4 […]...
- Молекулярні основи спадковості і мінливості Відповіді на питання до екзамену з курсу Основи біології та генетики Молекулярні основи спадковості і мінливості. Генетична інформація про ознаки організму міститься у геномі – наборі генів, що є ділянками молекул ДНК, які знаходяться в ядрах клітин. Різні види рибонуклеїнових кислот (і-РНК, т-РНК, р-РНК) забезпечують переміщення інформації в клітині, транспорт амінокислот, функціонування рибосом. Для багатьох […]...
- Відносні молекулярні маси деяких неорганічних речовин – ХІМІЯ Формули й таблиці ХІМІЯ Відносні молекулярні маси деяких неорганічних речовин H+ NH4+ Na+ K+ Ba2+ Ca2+ Mg2+ Al3+ Cr3+ Fe3+ Fe2+ Mn2+ Zn2+ Ag+ Cu2+ Pb2+ Sn2+ O2- 62 94 153 56 40 102 152 160 72 71 81 232 80 223 135 F- 20 37 42 58 175 78 62 84 109 113 94 […]...
- МОДЕЛЬ ГІБРИДИЗАЦІЇ ВАЛЕНТНИХ ОРБІТАЛЕЙ ЦЕНТРАЛЬНОГО АТОМА – ПРОСТОРОВА КОНФІГУРАЦІЯ МОЛЕКУЛ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ ПРОСТОРОВА КОНФІГУРАЦІЯ МОЛЕКУЛ МОДЕЛЬ ГІБРИДИЗАЦІЇ ВАЛЕНТНИХ ОРБІТАЛЕЙ ЦЕНТРАЛЬНОГО АТОМА Характер гібридизації валентних орбіталей центрального атома і їхнє просторове розташування визначають просторову конфігурацію молекул і комплексних іонів (рис. 11). Рис. 11. Гібридизація s – і р-валентних орбіталей. Відповідно до моделі гібридизації орбіталей центрального атома молекула СO2 має лінійну форму, іон […]...
- Відносні молекулярні маси деяких органічних речовин – ХІМІЯ Формули й таблиці ХІМІЯ Відносні молекулярні маси деяких органічних речовин -H -Сl -Вr -І -ОН -СОН -СООН -СООСН3 -СООС2Н5 -NH2 -H 2 36,5 81 128 18 ЗО 46 60 74 17 Насичені радикали -CnH2n+1 -CH3 16 50,5 95 142 32 44 60 74 88 31 -С2Н5 Зо 64,5 109 156 46 58 74 88 102 […]...
- УМОВИ ОДНОСТОРОННЬОГО ПЕРЕБІГУ РЕАКЦІЙ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ХІМІЧНА РІВНОВАГА УМОВИ ОДНОСТОРОННЬОГО ПЕРЕБІГУ РЕАКЦІЙ Зміщення хімічної рівноваги відбувається за рахунок утворення: Молекул слабких електролітів Летких сполук (виділення газу) Малорозчинних або нерозчинних сполук...
- ПРЕДМЕТ ОРГАНІЧНОЇ ХІМІЇ – ОРГАНІЧНІ СПОЛУКИ Хімія – універсальний довідник ОРГАНІЧНІ СПОЛУКИ ПРЕДМЕТ ОРГАНІЧНОЇ ХІМІЇ Органічна хімія – це хімія вуглеводнів і їх похідних. Вуглеводні – це, як випливає уже з назви, сполуки Карбону з Гідрогеном. Найпростішою з них є метан СН4. “Похідними” вуглеводнів називають речовини, які можна з них “зробити” (іноді лише думкою) шляхом заміни атомів Гідрогену на інші атоми […]...
- Фізичні властивості фенолу – СПИРТИ Й ФЕНОЛИ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ОРГАНІЧНА ХІМІЯ СПИРТИ Й ФЕНОЛИ Фізичні властивості фенолу Фенол являє собою безбарвні кристали (в ідеалі), при зберіганні набуває рожевуватого забарвлення внаслідок часткового окиснення. Має специфічний стійкий запах (так званий “запах карболки”). Отруйний! При потраплянні на шкіру викликає хімічні опіки. Температура плавлення +42 °С. […]...
- БУДОВА ВУГЛЕВОДНІВ. 2. ІЗОМЕРИ – ОРГАНІЧНІ СПОЛУКИ Хімія – універсальний довідник ОРГАНІЧНІ СПОЛУКИ БУДОВА ВУГЛЕВОДНІВ. 2. ІЗОМЕРИ Якщо у вуглеводневому ланцюгу більше трьох атомів Карбону, то вони можуть сполучатися по-різному, утворюючи ізомери – речовини з однаковим складом молекул, але різною будовою. Чим більше атомів Карбону в моле кулі, тим більше ізомерів має дана речовина....
- ВЗАЄМОДІЯ ГАЛОГЕНІВ З МЕТАЛАМИ Хімія – універсальний довідник ГАЛОГЕНИ ВЗАЄМОДІЯ ГАЛОГЕНІВ З МЕТАЛАМИ Хімічні властивості галогенів, тобто здатність вступати в реакції, утворювати ті або інші сполуки, визначаються їхнім місцем у періодичній системі. Кожен галоген практично завершує період, у якому він знаходиться. Розглянемо спочатку утворення сполуки одного з галогенів, а саме – Хлору з Натрієм. Електронна формула атома Натрію Він […]...
- ЕЛЕКТРОННА БУДОВА І ВЛАСТИВОСТІ АТОМІВ ХІМІЧНИХ ЕЛЕМЕНТІВ 3-ого ПЕРІОДУ Хімія – універсальний довідник ВІД НАТРІЮ ДО АРГОНУ ЕЛЕКТРОННА БУДОВА І ВЛАСТИВОСТІ АТОМІВ ХІМІЧНИХ ЕЛЕМЕНТІВ 3-ого ПЕРІОДУ Електронна будова атомів елементів 3-ого періоду визначається розподілом електронів на трьох енергетичних рівнях. При цьому перші два рівні, найближчі до ядра, заповнені цілком; їх будова описується електронною формулою 1s22s22р6. У періоді зліва направо відбувається поступове заповнення електронами зовнішнього, […]...
ЯНТАР »