Гідроген пероксид – ОКСИГЕН. СУЛЬФУР
Хімія підготовка до ЗНО та ДПА
Комплексне видання
ЧАСТИНА І
ЗАГАЛЬНА ХІМІЯ
ХІМІЯ ЕЛЕМЕНТІВ
ОКСИГЕН. СУЛЬФУР
Гідроген пероксид
Фізичні властивості гідроген пероксиду
Між молекулами Н2О2 виникають міцні водневі зв’язки, унаслідок чого речовина являє собою в’язку, важку (ρ = 1,44 г/см3) рідину блідо-голубого кольору з високою температурою кипіння (Тпл = +0,4 °С, Ткип = +150 °С).
Ця сполука змішується з водою в будь-яких співвідношеннях, за рахунок утворення нових водневих зв’язків.
Хімічні властивості гідроген
Гідроген пероксид може виступати як у ролі окисника, так і в ролі відновника, тому що атоми Оксигену в цій сполуці перебувають у проміжному ступені окиснення -1.
З більш сильними окисниками Н2О2 вступає в реакцію як відновник, тобто приймає електрони:
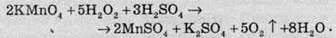
А з більш слабкими окисниками він виступає в ролі окисника:
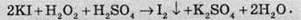
Однак гідроген пероксид дуже нестійка сполука. При зберіганні концентрованих розчинів або при дії опромінення Н2О2 розкладається на воду й кисень:
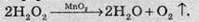
Каталізатором для цієї реакції є манган діоксид
,
Добування й застосування гідроген пероксиду
У промисловості Н2O2 добувають унаслідок дії концентрованої сульфатної кислоти на барій пероксид. У результаті цієї реакції барій сульфат утворює осад, а над ним залишається досить чистий гідроген пероксид:
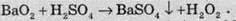
Застосовують в основному 3 % та 30 % водні розчини Н2О2. Використовують у текстильній промисловості для вибілювання тканин, а також як окисник ракетного палива. За рахунок бактерицидної дії гідроген пероксид використовують для знезаражування води та в медицині.
Related posts:
- Гідроген пероксид – Гідроген ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 9. Неметалічні елементи та їхні сполуки. Неметали 9.1. Гідроген 9.1.4. Гідроген пероксид Склад та будова молекули Формула гідроген пероксиду – Н2О2. Це ковалентна дуже полярна молекула: З водою змішується в будь-яких співвідношеннях. Розчин з масовою часткою Н2О2 30% називають пергідролем. Концентровані розчини гідроген […]...
- Сульфатна кислота – ОКСИГЕН. СУЛЬФУР Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЯ ЕЛЕМЕНТІВ ОКСИГЕН. СУЛЬФУР Сульфатна кислота Структурна формула сульфатної кислоти має такий вигляд: Фізичні властивості сульфатної кислоти Сульфатна кислота – це безбарвна, важка, масляниста рідина, яка замерзає при температурі +10 °С, а кипить при температурі +296 °С (кипить 98,3 % розчин, а надлишок […]...
- Прості речовини – ОКСИГЕН. СУЛЬФУР Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЯ ЕЛЕМЕНТІВ ОКСИГЕН. СУЛЬФУР Прості речовини Фізичні властивості речовин, утворених елементом Оксигеном Атоми Оксигену можуть утворювати два типи молекул: O2 – кисень та O3 – озон. Явище існування кількох простих речовин, утворених атомами одного хімічного елемента, називається алотропією. А прості речовини, утворені одним […]...
- ДОБУВАННЯ КИСНЮ З ГІДРОГЕН ПЕРОКСИДУ, ЗБИРАННЯ, ДОВЕДЕННЯ ЙОГО НАЯВНОСТІ ДОСЛІДЖУЄМО НА УРОЦІ ТА ВДОМА ПРАКТИЧНА РОБОТА № 4 Тема. Добування та збирання кисню. Мета роботи: освоїти одержання кисню лабораторним способом та навчитись виявляти його наявність. Речовини та обладнання: гідроген пероксид, пробірки, штатив для пробірок, пробка з газовідвідною трубкою, лабораторний штатив, напівзаповнений водою хімічний стакан чи плоскодонна колба, скляна чи виготовлена з іншого матеріалу, пластинка […]...
- Оксиди Сульфуру – ОКСИГЕН. СУЛЬФУР Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЯ ЕЛЕМЕНТІВ ОКСИГЕН. СУЛЬФУР Оксиди Сульфуру Фізичні властивості оксидів Сульфуру Сульфур(ІV) оксид, або сульфур діоксид, або сірчистий ангідрид, – це безбарвний газ із характерним різким запахом. Саме він створює запах при згоранні сірників. При температурі -10 °С він скраплюється в безбарвну рідину, а […]...
- Тема 23. Оксиген Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА ІІ ЗАВДАННЯ ДЛЯ ПЕРЕВІРКИ ЗНАНЬ НЕОРГАНІЧНА ХІМІЯ Тема 23. Оксиген Серед чотирьох наведених варіантів відповідей виберіть одну правильну 1. Виберіть властивості, що характерні для гідроген пероксиду: A. Окисні; Б. Відновні; B. Окисні і відновні; Г. Основні. 2. Укажіть вміст кисню в атмосфері Землі: A. 80 %; […]...
- Характеристика хімічних елементів – ОКСИГЕН. СУЛЬФУР Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЯ ЕЛЕМЕНТІВ ОКСИГЕН. СУЛЬФУР Характеристика хімічних елементів Властивості хімічних елементів Властивість Оксиген Сульфур Хімічний символ 0 S Порядковий номер 8 16 Атомна маса 15,9994 32,06 Місце в ПС 2 період; VI група 3 період; VI група Число електронів на енергетичних рівнях 2; 6 […]...
- Сульфати – ОКСИГЕН. СУЛЬФУР Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЯ ЕЛЕМЕНТІВ ОКСИГЕН. СУЛЬФУР Сульфати Солі сульфатної кислоти, сульфати, зазвичай являють собою кристалічні речовини, добре розчинні у воді (окрім PbSO4 та BaSO4). Безводні сульфати безбарвні, але деякі їхні сполуки з водою (кристалогідрати) мають колір: NiSO4 ∙ 7Н2O – інтенсивно зелений, FeSO4 ∙ 7Н2O […]...
- Сірководень – ОКСИГЕН. СУЛЬФУР Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЯ ЕЛЕМЕНТІВ ОКСИГЕН. СУЛЬФУР Сірководень Молекула сірководню складається з атома Сульфуру та двох атомів Гідрогену, сполучених полярним ковалентним зв’язком. Кут між зв’язками SH дорівнює 91°. Молекула сірководню полярна. Сірководень – природний компонент вулканічних і природних газів. Деякі мінеральні води містять розчинений сірководень, що […]...
- Оксиген, Сульфур. Алотропні модифікації. Сполуки оксигену та сульфуру – Неметали Хімія Неорганічна хімія Неметали Якщо в Періодичній системі умовно провести лінію по діагоналі від Бора до Астату, то праворуч угорі в головних підгрупах будуть розташовані елементи-неметалИ. До них належать: Гідроген, Гелій, Бор, Карбон, Нітроген, Оксиген, Флуор, Неон, Силіцій, Фосфор, Сульфур, Хлор, Аргон, Арсен, Селен, Бром, Криптон, Телур, Йод, Ксенон, Астат, Радон. Оксиген, Сульфур. Алотропні модифікації. […]...
- Оксиген. Кисень, його добування та фізичні властивості ТЕМА 2. ПРОСТІ РЕЧОВИНИ МЕТАЛИ І НЕМЕТАЛИ Урок 1. Оксиген. Кисень, його добування та фізичні властивості Цілі: вивчити характеристику кисню як простої речовини, його фізичні властивості, добування, способи збирання і виявлення; розкрити суть реакцій розкладу, суть поняття каталізатор. Обладнання: таблиці “Типи хімічних реакцій”, “Способи збирання газів”, штатив, пробірки, спиртівка, вата, пробка з газовідвідною трубкою, кристалізатор, […]...
- ГІДРОГЕН ЯК ХІМІЧНИЙ ЕЛЕМЕНТ – ВОДЕНЬ Хімія – універсальний довідник ВОДЕНЬ ГІДРОГЕН ЯК ХІМІЧНИЙ ЕЛЕМЕНТ У сполуках Гідроген одновалентний (його валентність прийнята за 1). Він утворює сполуки з переважною більшістю хімічних елементів (крім інертних газів і деяких металів В груп). У сполуках з Гідрогеном усі неметали проявляють свою нижчу валентність. Сполуки Гідрогену з металами називаються гідридами. Наприклад, NаН – гідрид натрію, […]...
- Приклади розв’язування типових задач (розрахунки за термохімічними рівняннями) – Хімічна реакція ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 4. Хімічна реакція Приклади розв’язування типових задач (розрахунки за термохімічними рівняннями) Задача 1. За наведеним термохімічним рівнянням добування аміаку Обчисліть: а) кількість теплоти, що виділяється під час утворення 5 моль аміаку; б) об’єм водню (н. у.), що прореагував, якщо під час реакції виділилось […]...
- Гідроген – ГІДРОГЕН. ВОДЕНЬ. ВОДА Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЯ ЕЛЕМЕНТІВ ГІДРОГЕН. ВОДЕНЬ. ВОДА Гідроген Характеристика хімічного елемента Гідроген – 1-й елемент Періодичної системи (заряд ядра 1), хімічний знак – Н, відносна атомна маса 1,008 (округлено 1). Валентність Гідрогену у сполуках дорівнює одиниці, найпоширеніший ступінь окиснення +1. Молекула водню Н2, молекулярна маса […]...
- Сірководень (гідроген сульфід). Сірководнева (сульфідна) кислота. Сульфіди – Елементи VIA групи ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 9. Неметалічні елементи та їхні сполуки. Неметали 9.3. Елементи VIA Групи 9.3.7. Сірководень (гідроген сульфід). Сірководнева (сульфідна) кислота. Сульфіди2 Сірководень та сірководнева кислота Сірководень, або гідроген сульфід H2S,- летка сполука Сульфуру з Гідрогеном. У молекулі сірководню атом Сульфуру утворює два ковалентні полярні зв’язки […]...
- Водень – Гідроген ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 9. Неметалічні елементи та їхні сполуки. Неметали Атоми неметалічних елементів мають у зовнішньому енергетичному рівні (окрім енергетичних елементів) значну кількість електронів (від чотирьох до семи) і здатні приєднувати певну кількість електронів, а саме стільки, скільки їх не вистачає до октету. Розгляньмо електронну будову […]...
- Гідроген хлорид. Хлоридна кислота ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 9. Неметалічні елементи та їхні сполуки. Неметали 9.2. Галогени 9.2.2. Гідроген хлорид. Хлоридна кислота Гідроген хлорид (хлороводень) Молекула хлороводню є ковалентною, лінійною, полярною, з одним a-зв’язком. Атом електронегативнішого Хлору зміщує у свій бік спільну електронну хмару: Кристалічні гратки твердого хлороводню молекулярні. Ступінь окиснення […]...
- Гідроген – ВОДЕНЬ. ГАЛОГЕНИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 8. ВОДЕНЬ. ГАЛОГЕНИ § 8.2. Гідроген Місце гідрогену в періодичній системі. Гідроген займає перше місце в періодичній системі (Z = 1). Він має найпростішу будову атома: ядро атома оточене електронною хмарою. Електронна конфігурація ls1. За одних умов гідроген виявляє металічні властивості […]...
- СУЛЬФУР – ХІМІЯ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ Хімія – універсальний довідник ХІМІЯ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ СУЛЬФУР Найважливішою сполукою Сульфуру є сульфатна кислота Н2SO4. У якості сировини для виробництва сульфатної кислоти використовуються самородна сірка, а також Сульфур, одержаний при очищенні від його сполук нафти і газу, а ще – сульфіди. Початкова стадія виробництва незалежно від сировини в принципі однакова – випалювання (нагрівання на повітрі): […]...
- Сульфур – Елементи VIA групи ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 9. Неметалічні елементи та їхні сполуки. Неметали 9.3. Елементи VIA Групи 9.3.5. Сульфур Сульфур – 16-й елемент періодичної таблиці, заряд ядра – +16. Хімічний символ – S, відносна атомна маса – 32. Відомо чотири стабільні природні ізотопи: 32S, 33S, 34S і 36S. Електронегативність […]...
- Очищення води – Гідроген ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 9. Неметалічні елементи та їхні сполуки. Неметали 9.1. Гідроген 9.1.3. Очищення води За даними 00Н сьогодні із 7 млрд. людей нашої планети більше 1,2 млрд. живуть в умовах постійного дефіциту прісної води, і ще близько 2 млрд. – страждають від нього регулярно. Отже, […]...
- Тема 24. Сульфур Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА ІІ ЗАВДАННЯ ДЛЯ ПЕРЕВІРКИ ЗНАНЬ НЕОРГАНІЧНА ХІМІЯ Тема 24. Сульфур Серед чотирьох наведених варіантів відповідей виберіть одну правильну 1. Виберіть властивості, характерні для сірководню: A. Окисні; Б. Відновні; B. Окисні і відновні; Г. Основні. 2. Укажіть речовину, яку можна використовувати для виявлення сульфат-іонів у розчині: A. […]...
- Вплив середовища на характер перебігу реакцій – ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 7. ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ § 7.4. Вплив середовища на характер перебігу реакцій Реакції окиснення – відновлення можуть відбуватися в різних середовищах: у кислому (надлишок Н+-іонів), нейтральному (Н2О) і лужному (надлишок гідроксид-іонів ОН – ). Залежно від середовища може змінюватись і характер […]...
- Сполуки неметалічних елементів з Гідрогеном. Гідроген хлорид. Хлоридна кислота I СЕМЕСТР Тема 1. НЕМЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ (18 год.) УРОК 8 Тема уроку. Сполуки неметалічних елементів з Гідрогеном. Гідроген хлорид. Хлоридна кислота Цілі уроку: розширити знання про хімічні властивості неметалів на прикладі їхніх сполук із Гідрогеном, знання про властивості кислот на прикладі гідроген хлориду та хлоридної кислоти, властивості хлоридів; продовжити формування практичних умінь […]...
- Хімічні властивості алкенів – АЛКЕНИ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ОРГАНІЧНА ХІМІЯ АЛКЕНИ Хімічні властивості алкенів Хімічні властивості алкенів визначаються наявністю в їхній молекулі подвійного зв’язку. При приєднанні полярних молекул типу НХ (X; Hаl, ОН, СN до несиметричних алкенів Гідроген переважно приєднується до більш гідрогенізованого атома Карбону, що примикає до подвійного зв’язку (правило […]...
- ОКСИГЕН ЯК ХІМІЧНИЙ ЕЛЕМЕНТ. ОКСИДИ – КИСЕНЬ Хімія – універсальний довідник КИСЕНЬ ОКСИГЕН ЯК ХІМІЧНИЙ ЕЛЕМЕНТ. ОКСИДИ Хімічний символ Оксигену – О. Його відносна атомна маса 15,9994 ≈ 16. Елемент О знаходиться в VIA групі періодичної системи, отже, можливі його валентності – вища 6 і нижча 2. Але правіше від Оксигену в таблиці розташований лише один елемент F, а вище – жодного. […]...
- Вода – Гідроген ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 9. Неметалічні елементи та їхні сполуки. Неметали 9.1. Гідроген 9.1.2. Вода Світовий океан вкриває близько 71 % земної поверхні. Маса гідросфери – 1,39 · 1018 т – складає 0,05 % маси планети (але це удесятеро менше, ніж міститься у мантії Землі). Багато води […]...
- Оксиген – Елементи VIA групи ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 9. Неметалічні елементи та їхні сполуки. Неметали 9.3. Елементи VIA Групи 9.3.2. Оксиген Оксиген – 8-й елемент періодичної таблиці, заряд ядра – +8. Хімічний символ – О. Відомо три стабільні природні ізотопи Оксигену: 16O,17O, 18O, серед яких найчастіше трапляється 16О (99,76 %). Оксиген […]...
- Сульфур та його властивості – ПІДГРУПА ОКСИГЕНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 9. ПІДГРУПА ОКСИГЕНУ § 9.3. Сульфур та його властивості Поширення в природі. Сульфур широко розповсюджений у природі. Він становить 0,05 % маси земної кори. У вільному стані (самородна сірка) у великих кількостях трапляється в Італії (острів Сицілія) і США. У Росії […]...
- Добування альдегідів – АЛЬДЕГІДИ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ОРГАНІЧНА ХІМІЯ АЛЬДЕГІДИ Добування альдегідів 1. Окиснення спиртів. Загальним способом добування альдегідів є реакція окиснення спиртів купрум(ІІ) оксидом: Іноді відзначають, що в реакції окиснення спиртів мідь є каталізатором унаслідок того, що отримана мідь потім окиснюється киснем повітря й знову вступає в реакцію окиснення. […]...