ГІДРОЛІЗ СОЛЕЙ – ВУГЛЕЦЬ І ЙОГО СПОЛУКИ
Хімія – універсальний довідник
ВУГЛЕЦЬ І ЙОГО СПОЛУКИ
ГІДРОЛІЗ СОЛЕЙ
У нейтральних розчинах, тобто за відсутності кислот і лугів, у результаті дисоціації (дуже слабкої) води утворюються однакові кількості іонів Н+ і ОН-:
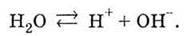
Додавання до води кислоти збільшує концентрацію іонів Н+ і, зміщуючи рівновагу дисоціації води вліво, знижує концентрацію іонів ОН-. Отже, кислий розчин містить більше іонів Гідрогену, ніж гідроксид-іонів.
Аналогічно додавання лугу, створюючи лужне середовище, зумовлює те, що
Таким чином, кислотність (лужність) розчину залежить від відносних кількостей іонів Н+ і ОН-. Якщо їх рівність порушується, розчин набуває певного середовища. Це може відбуватися не тільки при введенні в розчин кислот або лугів.
Якщо до складу солі входить іон слабкої кислоти, то він взаємодіє з водою, приєднуючи Іони Н+ і збільшуючи тим самим концентрацію іонів ОН-, тобто створюючи лужне середовище.
Наприклад, при розчиненні у воді соди Nа2СO3 у розчині з’являються іони Nа+ і СO32-:
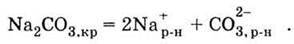
Іон СО32- взаємодіє з водою:
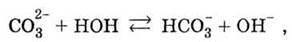
Оскільки карбонатна кислота Н2СО3 – слабкий електроліт; ще меншою мірою дисоціює гідрокарбонат-іон НСО3-.
Другий запис є скороченим іонним рівнянням реакції гідролізу карбонату натрію. Такий запис наочно показує зміну реакції (кисла або лужна) розчину.
Реакції гідролізу оборотні, тому що і серед реагентів, і серед продуктів є слабкі електроліти. А оскільки вода є одним з найслабших електролітів, у переважній більшості випадків рівновага гідролізу сильно зміщена вліво.
При взаємодії з водою солі, до складу якої входить катіон слабкої основи, останній взаємодіє з водою, утворюючи слабкий електроліт і зв’язуючи при цьому іони ОН-. Розчин такої солі – кислий. Наприклад, у водному розчині хлориду цинку відбуваються процеси:
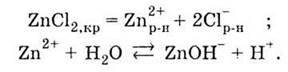
Таким чином, гідролізу піддаються ті іони солі, які входять до складу слабких кислот або слабких основ. Іншими словами, гідролізуються солі, утворені слабкою кислотою і сильною основою (тоді утворюється лужний розчин, наприклад, у випадку соди) або сильною кислотою і слабкою основою (тоді утворюється кислий розчин, як, наприклад, у випадку хлориду цинку).
Якщо сіль утворена слабкою основою і слабкою кислотою, то в реакцію з водою водночас вступають обидва іони солі, гідроліз стає необоротним, тобто сіль розкладається водою. Наприклад, сульфід алюмінію Аl2S3 – сіль, утворена слабкою основою Аl(ОН)3 і слабкою сульфідною кислотою Н2S, при сполученні з водою розкладається:
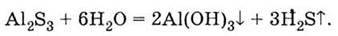
Щодо таких солей недоречне питання про їх розчинність у воді (у таблиці розчинності речовин у воді у відповідних місцях ви можете побачити прочерки).




 (1 votes, average: 5.00 out of 5)
(1 votes, average: 5.00 out of 5)Related posts:
- ГІДРОЛІЗ СОЛЕЙ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ХІМІЧНА РІВНОВАГА ГІДРОЛІЗ СОЛЕЙ Гідроліз солі – обмінна реакція між сіллю і водою. Схема гідролізу за катіоном: Гідролізу за катіоном підлягають солі слабкої основи і сильної кислоти: Чим більший заряд і менші розміри катіона, тим більший ступінь гідролізу. Схема гідролізу за аніоном: Чим більший негативний заряд і менший розмір […]...
- Гідроліз солей РОЗДІЛ 1 ПОВТОРЕННЯ ТА ПОГЛИБЛЕННЯ ТЕОРЕТИЧНИХ ПИТАНЬ КУРСУ ХІМІЇ ОСНОВНОЇ ШКОЛИ § 13. Гідроліз солей Усвідомлення змісту цього параграфа дає змогу: Пояснювати поняття “гідроліз солей” і суть цього процесу; характеризувати різні випадки гідролізу; Вміти наводити приклади гідролізу і складати рівняння відповідних реакцій; Прогнозувати реакцію середовища та експериментально її визначати. Пригадайте, які речовини називаються солями та […]...
- Гідроліз солей – НАЙВАЖЛИВІШІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 6. НАЙВАЖЛИВІШІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК § 6.5. Гідроліз солей Означення. Досвід показує, що розчини середніх солей мають лужну, кислу або нейтральну реакцію, хоча вони і не містять ні водневих, ні гідроксильних іонів. Пояснення цьому факту слід шукати у взаємодії солей з […]...
- Гідроліз солей як окремий випадок реакцій йонного обміну у водних розчинах електролітів ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 6. Суміші речовин. Розчини 6.11. Гідроліз солей як окремий випадок реакцій йонного обміну у водних розчинах електролітів У хімії часто стикаються з явищем гідролізу1 – хімічної взаємодії речовин з водою. Найбільше практичне значення має гідроліз солей. Гідроліз солей – це хімічна взаємодія солей […]...
- КАРБОНАТНА КИСЛОТА ТА ЇЇ СОЛІ – ВУГЛЕЦЬ І ЙОГО СПОЛУКИ Хімія – універсальний довідник ВУГЛЕЦЬ І ЙОГО СПОЛУКИ КАРБОНАТНА КИСЛОТА ТА ЇЇ СОЛІ З хімічної точки зору оксид карбону (IV) – кислотний оксид із властивостями, характерними для даного класу неорганічних сполук. Йому відповідає карбонатна кислота Н2СО3. Це дуже нестійка сполука, у вільному вигляді не існує, та й у водних розчинах молекули карбонатної кислоти не виявляються. […]...
- ВУГЛЕЦЬ ЯК ПРОСТА РЕЧОВИНА – ВУГЛЕЦЬ І ЙОГО СПОЛУКИ Хімія – універсальний довідник ВУГЛЕЦЬ І ЙОГО СПОЛУКИ ВУГЛЕЦЬ ЯК ПРОСТА РЕЧОВИНА В атомі Карбону на його зовнішніх чотирьох АО є чотири електрони, тому всі чотири АО беруть участь в утворенні хімічних зв’язків. Цим пояснюється різноманітність і багаточисельність сполук Карбону. Переважна більшість сполук Карбону належить до так званих органічних речовин. У цьому розділі розглядаються властивості […]...
- СИЛІЦІЙ І ЙОГО СПОЛУКИ – ВУГЛЕЦЬ І ЙОГО СПОЛУКИ Хімія – універсальний довідник ВУГЛЕЦЬ І ЙОГО СПОЛУКИ СИЛІЦІЙ І ЙОГО СПОЛУКИ Силіцій – хімічний аналог Карбону. Оксид SіO2, як і оксид карбону СO2, кислотний. Однак з водою він не взаємодіє, тому що відповідна йому силікатна кислота Н2SiO3 (або Н4SiO4) у воді нерозчинна. Аналогічний факт ми уже відзначали для основних оксидів металів: з водою взаємодіють […]...
- ОКСИДИ КАРБОНУ – ВУГЛЕЦЬ І ЙОГО СПОЛУКИ Хімія – універсальний довідник ВУГЛЕЦЬ І ЙОГО СПОЛУКИ ОКСИДИ КАРБОНУ Маючи чотири електрони на зовнішньому енергетичному рівні, Карбон у сполуці з Оксигеном, залежно від умов, проявляє ступені окиснення +2 і +4. Під час горіння карбоновмісних речовин (дрова, вугілля, природний газ метан, спирт та ін.) при температурі звичайного полум’я проходить реакція: Але якщо створити умови для […]...
- Водневий показник розчинів солей – Протолітична рівновага КИСЛОТИ Й ОСНОВИ 2. Протолітична рівновага 2.4. Водневий показник розчинів солей Багато сольових розчинів мають нейтральне середовище, деякі – кисле або лужне. За Бренстедом, вода при цьому виконує функцію основи або кислоти. Приклад. Натрій хлорид Іон Na+: не вступає в реакцію з водою. Іон Сl-: надзвичайно слабка основа, тому протоліз не відбувається. Розчин натрій хлориду […]...
- Розв’язування типових задач Оксиди, кислоти, основи, солі – НАЙВАЖЛИВІШІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 6. НАЙВАЖЛИВІШІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК § 6.7. Розв’язування типових задач Оксиди, кислоти, основи, солі Задача 1. Напишіть рівняння реакцій, за допомогою яких можна здійснити такі перетворення; CuSO4 -> Сu -> СuО -> СuСl2 -> Сu(OН)2 -> Cu(OH)NO3 -> Сu(NO3)2. Розв’язання. 1) […]...
- Добуток розчинності – Рівновага розчинності ХІМІЧНА РІВНОВАГА 3. Рівновага розчинності 3.2 . Добуток розчинності Якщо до насиченого розчину солі у воді ще додати цю ж сіль, то ця добавка випаде в нерозчинений осад. Якщо до нього додати сіль, що містить один з іонів розчиненої солі, то утвориться такий самий осад. Приклад. Якщо до насиченого розчину кальцій сульфату додати трохи кальцій […]...
- Дисоціація кислот, основ і солей у водних розчинах – РОЗЧИНИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 5. РОЗЧИНИ. ТЕОРІЯ ЕЛЕКТРОЛІТИЧНОЇ ДИСОЦІАЦІЇ § 5.8. Дисоціація кислот, основ і солей у водних розчинах За допомогою теорії електролітичної дисоціації дають означення й описують властивості кислот, основ і солей. Кислотами називаються електроліти, під час дисоціації яких як катіони утворюються тільки катіони […]...
- Амінокислоти – АЗОТОВМІСНІ ОРГАНІЧНІ СПОЛУКИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина III. ОРГАНІЧНА ХІМІЯ Розділ 18. АЗОТОВМІСНІ ОРГАНІЧНІ СПОЛУКИ § 18.4. Амінокислоти Амінокислотами називаються органічні сполуки, в молекулах яких містяться одночасно аміногрупа – NH2 і карбоксильна група – СООН. Їх можна розглядати як похідні карбонових кислот, які утворюються заміщенням одного або кількох атомів водню у вуглеводневому […]...
- ФОСФОР I ЙОГО СПОЛУКИ – ХІМІЯ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ Хімія – універсальний довідник ХІМІЯ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ ФОСФОР I ЙОГО СПОЛУКИ Радіус атома Фосфору майже у два рази більший, ніж Нітрогену. Це зумовлює суттєві відмінності у їхніх властивостях. Різниця в розмірах атомів позначається уже в будові простих речовин. Молекули азоту, утворені маленькими атомами, двохатомні. Збільшення розміру атомів веде до менш ефективного перекривання їх атомних орбіталей […]...
- Електролітична дисоціація кислот, основ, солей у водних розчинах Тема 1 РОЗЧИНИ Урок 12 Тема уроку. Електролітична дисоціація кислот, основ, солей у водних розчинах Цілі уроку: поглибити знання учнів про електролітичну дисоціацію на прикладі розчинів кислот, основ і солей; формувати навички складання рівнянь дисоціації на прикладі розчинних кислот, основ, солей; уточнити визначення кислот, основ і солей у світлі теорії електролітичної дисоціації. Тип уроку: засвоєння […]...
- Сполуки заліза – МЕТАЛИ ПОБІЧНИХ ПІДГРУП ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 14. МЕТАЛИ ПОБІЧНИХ ПІДГРУП § 14.7. Сполуки заліза Для заліза найбільш характерні два ряди сполук: сполуки феруму(ІІ) і феруму(ІІІ). Відома також незначна кількість сполук феруму(VІ) – ферати, наприклад ферат калію K3FeO4, ферат барію BaFeO4. Оксид ферум у (II) FeO – чорний […]...
- Складні ефіри (естери). Реакції етерифікації та омилення – КИСНЕВМІСНІ ОРГАНІЧНІ СПОЛУКИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина III. ОРГАНІЧНА ХІМІЯ Розділ 17. КИСНЕВМІСНІ ОРГАНІЧНІ СПОЛУКИ § 17.13. Складні ефіри (естери). Реакції етерифікації та омилення Добування складних ефірів. При взаємодії карбонових кислот зі спиртами утворюються складні ефіри. Наприклад, з оцтової кислоти й етилового спирту за наявності каталізатора(концентрованої сірчаної або соляної кислоти) добувають складний […]...
- НЕСТЕХІОМЕТРИЧНІ СПОЛУКИ – СПОЛУКИ ЗМІННОГО СКЛАДУ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ СПОЛУКИ ЗМІННОГО СКЛАДУ НЕСТЕХІОМЕТРИЧНІ СПОЛУКИ Сполуки сталого складу називають стехіометричними. Наприклад, оксид карбону (IV) СO2 і сульфід карбону (IV) СS2. У них співвідношення між числом атомів (іонів), що утворюють сполуку, виражається цілими числами (СO2, Н2O, HCl). Сполуки змінного складу називають нестехіометричними. Наприклад, оксид феруму (II) складу від Fе0,89О до […]...
- Мила і синтетичні мийні засоби – Естери. Жири – Оксигеновмісні органічні сполуки ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ III. ОРГАНІЧНА ХІМІЯ 12. Оксигеновмісні органічні сполуки 12.5. Естери. Жири 12.5.3. Мила і синтетичні мийні засоби Вищі насичені (жирні) карбонові кислоти у воді нерозчинні через наявність у молекулі великого вуглеводневого залишку. Однак вони добре розчинні в розчинах лугів унаслідок утворення солей: Натрієві і калієві солі вищих […]...
- Водневий показник – Протолітична рівновага КИСЛОТИ Й ОСНОВИ 2. Протолітична рівновага 2.2. Водневий показник У водних розчинах електролітів (кислот, основ) іонний добуток води залишається практично незмінним, поки їх концентрація не стане дуже великою. Отже, якщо концентрація с(Н3О+) у розчині більша, ніж у чистій воді, то с(ОН-) повинна бути менша, і навпаки. Приклад. Рівновага НСl + Н2O Н3O+ + Сl – […]...
- Сильні й слабкі електроліти – РОЗЧИНИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 5. РОЗЧИНИ. ТЕОРІЯ ЕЛЕКТРОЛІТИЧНОЇ ДИСОЦІАЦІЇ § 5.10. Сильні й слабкі електроліти Розрізняють сильні й слабкі електроліти. Сильні електроліти під час розчинення у воді повністю дисоціюють на іони. До них належать: 1) майже всі солі; 2) багато мінеральних кислот, наприклад H2SO4, HNO3, […]...
- Естери. Реакція естерифікації – Оксигеновмісні органічні сполуки Хімія Органічна хімія Оксигеновмісні органічні сполуки Естери. Реакція естерифікації Естери Естери Можна розглядати як похідні кислот, у яких Гідроген гідроксильної групи заміщений на вуглеводневий радикал спирту. Назви естерів утворюються від назв відповідних кислот і спиртів з додаванням слова естер. Наприклад, естер можна назвати етиловий естер оцтової кислотИ, за міжнародною систематичною номенклатурою – етилацетат (суфікс – […]...
- РОЗЧИН І ЙОГО КОМПОНЕНТИ: РОЗЧИННИК, РОЗЧИНЕНА РЕЧОВИНА ДОСЛІДЖУЄМО НА УРОЦІ ТА ВДОМА Дослід 1. Що робили Спостереження 1. Приготували розчин з води об’ємом 50 мл і кухонної солі масою 15 г налили його у чашку для випарювання. 2. Поставили чашку на кільце штатива. Скляну лійку закріпили на лабораторному штативі (розширеною частиною донизу над чашкою). 3. Нагріли над полум’ям спиртівки чашку з розчином, […]...
- СОЛІ ЯК ЕЛЕКТРОЛІТИ – ЕЛЕКТРОЛІТИ Хімія – універсальний довідник ЕЛЕКТРОЛІТИ СОЛІ ЯК ЕЛЕКТРОЛІТИ При розчиненні у воді солі дисоціюють з утворенням позитивно заряджених іонів металу (або амонію NН4+) і негативно заряджених кислотних залишків. Ці іони і визначають поведінку солей у розчинах. Солі можуть взаємодіяти з кислотами: З лугами: З іншими солями: І тут, як і в усіх реакціях, які відбуваються […]...
- ЗАЛІЗО І ЙОГО СПОЛУКИ – ХІМІЯ МЕТАЛІЧНИХ ЕЛЕМЕНТІВ Хімія – універсальний довідник ХІМІЯ МЕТАЛІЧНИХ ЕЛЕМЕНТІВ ЗАЛІЗО І ЙОГО СПОЛУКИ Проста речовина залізо – метал з усіма характерними для металічного стану властивостями: високими тепло – і електропровідністю, ковкістю, “металічним” блиском та ін.; здатний утворювати сплави з іншими металами, а також, що дуже важливо на практиці, і з вуглецем. Від більшості інших металів залізо відрізняється […]...
- Обмін води і мінеральних солей Відповіді на питання до екзамену з курсу Основи біології та генетики Обмін води і мінеральних солей. Вода та мінеральні солі переходять з травного каналу в кров у незмінному стані. В ході обміну речовин вони також не зазнають істотних змін і енергетичного значення в організмі не мають. Значення води та мінеральних солей полягає в іншому. Всі […]...
- Оцтова кислота – КИСНЕВМІСНІ ОРГАНІЧНІ СПОЛУКИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина III. ОРГАНІЧНА ХІМІЯ Розділ 17. КИСНЕВМІСНІ ОРГАНІЧНІ СПОЛУКИ § 17.12. Оцтова кислота Оцтова кислота при звичайній температурі – безбарвна рідина з різким характерним запахом. При температурі, нижчій за +16,6 °С, вона твердне у вигляді кристалів, схожих на лід, внаслідок чого дістала назву льодяної оцтової кислоти. […]...
- Проба розчином Фелінга – Виявлення альдегідів АНАЛІЗ ОРГАНІЧНИХ СПОЛУК 2 . Визначення властивостей речовин 2.2. Виявлення альдегідів Альдегіди в лужному розчині є сильними відновниками. При цьому карбонільна група окислюється в карбоксильну групу. Відновлення відповідних іонів металів є доказом наявності альдегідів. Проба розчином Фелінга Як реагент використовують розчин купрум(ІІ) сульфату. Іони Си(ІІ), що містяться в ньому, вступають у реакцію в лужному розчині […]...
- Розчинність основ і солей у воді ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ ДОДАТОК 2. Розчинність основ і солей у воді Катіони Аніони OH- F- Cl- Br- L- S2- SO2-3 SO2-4 NO-3 PO3-4 CO2-3 SіО2-3 СН3СОО NH+4 – P P P P – P P P P P – P Na+,K+ P P P P P P P P […]...
- Нейтралізація слабких кислот і основ – Нейтралізація КИСЛОТИ Й ОСНОВИ 3. Нейтралізація При змішуванні рівних об’ємів соляної кислоти і розчину їдкого натру однакових концентрацій, утворюється нейтральний розчин натрій хлориду, що має показник pH = 7. Таким чином, кислотні і лужні властивості початкових речовин нейтралізуються. Нейтралізація є реакцією взаємодії іонів гідроксонію і гідроксид-іонів з утворенням молекул води: Н3О+ + ОН – 2 Н2О. […]...
- Дія буферів – Буферні розчини – Протолітична рівновага КИСЛОТИ Й ОСНОВИ 2. Протолітична рівновага 2.5. Буферні розчини Дія буферів Використовуючи константу рівноваги процесу дисоціації кислоти, можна показати дію буфера: – Додавання кислоти, тобто збільшення с(Н3О+). Для збереження рівноваги додані іони гідроксонію реагуватимуть з відповідними іонами А-, утворюючи недисоційовану НА, практично не змінюючи концентрацію іонів гідроксонію. – Додавання лугу, тобто збільшення с(ОН-). Додані гідроксид-іони […]...
- Жири, їхній склад, хімічна будова. Гідроліз, гідрування жирів. Біологічна роль жирів II Семестр Тема 4. ОКСИГЕНОВМІСНІ ОРГАНІЧНІ СПОЛУКИ Урок 42 Тема уроку. Жири, їхній склад, хімічна будова. Гідроліз, гідрування жирів. Біологічна роль жирів Цілі уроку: формувати знання учнів про жири, їхній склад, утворення; вивчити будову жирів і властивості їх як естерів гліцерину й вищих карбонових кислот; ознайомити учнів з хімічними властивостями жирів на прикладі гідролізу й […]...
- Деякі сполуки галогенів – ГАЛОГЕНИ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЯ ЕЛЕМЕНТІВ ГАЛОГЕНИ Деякі сполуки галогенів Оксигеновмісні кислоти Хлору Характеристика оксигеновмісних кислот Хлору Формула кислоти Ступінь окиснення атома Хлору Назва кислоти Назва аніона Сила кислоти Стійкість кислоти HClO +1 Гіпохлоритна Гіпохлорит Дуже слабка Дуже нестійка HClO2 +3 Хлоритна Хлорит Середньої сили Існує тільки […]...
- Білки як високомолекулярні сполуки. Головні амінокислоти, що беруть участь в утворенні білків. Рівні структурної організації білків. Властивості білків: гідроліз, денатурація, кольорові реакції II Семестр Тема 5. НІТРОГЕНОВМІСНІ ОРГАНІЧНІ СПОЛУКИ Урок 54 Тема уроку. Білки як високомолекулярні сполуки. Головні амінокислоти, що беруть участь в утворенні білків. Рівні структурної організації білків. Властивості білків: гідроліз, денатурація, кольорові реакції Цілі уроку: формувати в учнів поняття про білки як природні високомолекулярні сполуки, первинну, вторинну, третинну й четвертинну структури білкових молекул; ознайомити з […]...
- Аміни – АЗОТОВМІСНІ ОРГАНІЧНІ СПОЛУКИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина III. ОРГАНІЧНА ХІМІЯ Розділ 18. АЗОТОВМІСНІ ОРГАНІЧНІ СПОЛУКИ § 18.2. Аміни Амінами називаються похідні аміаку, у якому один, два або всі три атоми водню заміщені органічними радикалами. Залежно від числа радикалів розрізняють аміни первинні (з одним радикалом), вторинні (з двома) і третинні (з трьома). Загальні […]...
- Контрольна робота № 3 з теми “Органічні сполуки. Органічні сполуки як основа сучасних матеріалів. Органічні сполуки і здоров’я людини” УРОК 27 Тема. Контрольна робота № 3 з теми “Органічні сполуки. Органічні сполуки як основа сучасних матеріалів. Органічні сполуки і здоров’я людини” Мета: перевірити рівень навчальних досягнень учнів з теми “Органічні сполуки. Органічні сполуки як основа сучасних матеріалів. Органічні сполуки і здоров’я людини”. Обладнання: роздавальний матеріал. Тип уроку: КОН. Форми роботи: тестово-текстові завдання по варіантах. […]...
- Сполуки Феруму РОЗДІЛ 3 МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХ СПОЛУКИ ХІМІЧНІ ЕЛЕМЕНТИ ІА – ІІІА ГРУП § 69. Сполуки Феруму Усвідомлення змісту цього параграфа дає змогу: Характеризувати фізичні та хімічні властивості оксидів, гідроксидів і солей Феруму(ІІ) і Феруму(ІІІ); порівнювати їх властивості; Складати йонні та окисно-відновні рівняння хімічних реакцій; експериментально визначити сполуки Феруму(ІІ) і Феруму(ІІІ). Ви вже знаєте, що […]...
- Електроліти і неелектроліти – РОЗЧИНИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 5. РОЗЧИНИ. ТЕОРІЯ ЕЛЕКТРОЛІТИЧНОЇ ДИСОЦІАЦІЇ § 5.4. Електроліти і неелектроліти Добре відомо, що одні речовини в розчиненому або розплавленому вигляді проводять електричний струм, інші за таких самих умов струм не проводять. Це можна простежити за допомогою простого приладу (рис. 5.4). Він […]...
- Загальні способи одержання оксидів, основ, кислот, солей Тема 2 ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК УРОК 34 Тема. Загальні способи одержання оксидів, основ, кислот, солей Цілі уроку: розвивати вміння й навички учнів у складанні рівнянь на прикладі одержання оксидів, основ, кислот, солей; систематизувати знання учнів про загальні способи одержання оксидів, основ, кислот і солей; показати їх взаємозв’язок з генетичним зв’язком класів неорганічних сполук. Тип […]...
- Розвиток понять “кислоти” й “основи” – Визначення кислот і основ КИСЛОТИ Й ОСНОВИ 1. Визначення кислот і основ Кислотами зазвичай вважають речовини, водні розчини яких мають такі властивості: – кислий смак; – розчиняють неблагородні метали, виділяючи водень; – розкладають карбонати (наприклад, вапняк) з виділенням карбон діоксиду; – змінюють забарвлення індикаторів. До основ відносяться речовини, водні розчини яких (луги) мають такі властивості: – мильні на дотик; […]...