ОРГАНІЧНІ СПОЛУКИ, ЩО ВХОДЯТЬ ДО СКЛАДУ КЛІТИНИ – ХІМІЧНИЙ СКЛАД КЛІТИНИ
Довідник з біології
ЗАГАЛЬНА БІОЛОГІЯ
ОСНОВИ ЦИТОЛОГІЇ
ХІМІЧНИЙ СКЛАД КЛІТИНИ
ОРГАНІЧНІ СПОЛУКИ, ЩО ВХОДЯТЬ ДО СКЛАДУ КЛІТИНИ.
Органічні сполуки складають близько 20-30 % маси живих клітин. До них відносяться біологічні полімери – білки, нуклеїнові кислоти і полісахариди, а також жири, гормони, пігменти, АТФ тощо.
Білки складають 10-18% від загальної маси клітини (50- 80% від сухої маси). Молекулярна маса білків коливається від десятків тисяч до багатьох мільйонів одиниць. Білки – це біополімери, мономерами яких є амінокислоти.
Кожна амінокислота складається з вуглеводневого радикала, сполученого з карбоксильною групою, що має кислотні властивості (-СООН), й аміногрупою (-NH2), яка має основні
Білки живих організмів складаються з сотень і тисяч амінокислот, тобто є макромолекулами. Різні властивості та функції білкових молекул визначаються послідовністю з’єднання амінокислот, яка закодована в ДНК. Цю послідовність називають первинною структурою молекули білка, від якої, у свою чергу, залежать подальші рівні просторової організації і біологічні властивості білків. Первинна структура білкової молекули зумовлена пептидними зв’язками.
Повторна структура білкової молекули досягається її спіралізацією, завдяки встановленню між атомами сусідніх витків спіралі водневих зв’язків. Вони слабкіше ковалентних, але, багато разів повторені, створюють досить міцну сполуку. Функціонування у вигляді закрученої спіралі характерне для деяких фібрилярних білків (колаген, фібриноген, міозин, актин тощо).
Більшість білкових молекул стають функціонально активними тільки після набуття глобулярної (третинної) структури. Вона формується шляхом багатократного згортання спіралі в тривимірне утворення – глобулу. Ця структура зшивається, як правило, ще більш слабкими дисульфідними (-S-S-) зв’язками. Глобулярну структуру має більшість білків (альбуміни, глобуліни тощо).
Для виконання деяких функцій потрібна участь білків з більш високим рівнем організації, при якому виникає об’єднання декількох глобулярних білкових молекул в єдину систему – четвертичну структуру (хімічні зв’язки можуть бути різні). Наприклад, молекула гемоглобіну складається з чотирьох різних глобул і гемінової групи, що містить іон заліза.
Втрата білковою молекулою своєї структурної організації називається денатурацією. Причиною її можуть бути різні хімічні (кислоти, луги, спирт, солі важких металів тощо) і фізичні (високі температура і тиск, іонізуюче випромінювання тощо) чинники. Спочатку руйнується дуже слабка – четвертична, потім третинна, вторинна, а за більш жорстких умов і первинна структура. Якщо під дією денатуруючого чинника не зачіпається первинна структура, то при поверненні білкових молекул у нормальні умови середовища їх структура повністю відновлюється, тобто відбувається ренатурація. Ця властивість білкових молекул широко використовується в медицині для приготування вакцин і сироваток і в харчовій промисловості для отримання харчових концентратів. При необоротній денатурації (руйнуванні первинної структури) білки втрачають свої властивості.
Білки виконують наступні функції: будівельну, каталітичну, транспортну, рухову, захисну, сигнальну, регуляторну й енергетичну.
Як будівельний матеріал білки входять до складу всіх клітинних мембран, гіалоплазми, органоїдів, ядерного соку, хромосом і ядерець.
Каталітичну (ферментативну) функцію виконують білки – ферменти, у десятки і сотні тисяч разів прискорюючи перебіг біохімічних реакцій у клітинах при нормальному тиску і температурі близько 37 °С. Кожний фермент може каталізувати тільки одну реакцію, тобто дія ферментів строго специфічна. Специфічність ферментів зумовлена наявністю одного або декількох активних центрів, в яких відбувається тісний контакт між молекулами ферменту і специфічної речовини (субстрату). Деякі ферменти застосовуються в медичній практиці і харчовій промисловості.
Транспортна функція білків полягає в перенесенні речовин, наприклад кисню (гемоглобін) і деяких біологічно активних речовин (гормонів).
Рухова функція білків полягає в тому, що всі види рухових реакцій клітин і організмів забезпечуються спеціальними скоротливими білками – актином і міозином. Вони містяться у всіх м’язах, віях і джгутиках. їх нитки здатні скорочуватися з використанням енергії АТФ.
Захисна функція білків пов’язана з виробленням лейкоцитами особливих білкових речовин – антитіл у відповідь на проникнення в організм чужорідних білків або мікроорганізмів. Антитіла зв’язують, нейтралізують і руйнують не властиві організму з’єднання. Прикладом захисної функції білків може бути перетворення фібриногену в фібрин при згортанні крові.
Сигнальна (рецепторна) функція здійснюється білками завдяки здатності їх молекул змінювати свою структуру під впливом хімічних і фізичних чинників, унаслідок чого клітина або організм сприймає ці зміни.
Регуляторна функція здійснюється гормонами, що мають білкову природу (наприклад, інсулін).
Енергетична функція білків полягає в їх здатності бути джерелом енергії в клітині (як правило, за відсутності інших). При повному ферментативному розщеплюванні 1 г білка виділяється 17,6 кДж енергії.
Вуглеводи. Вуглеводи, або сахариди, – органічні речовини із загальною формулою Сn(Н20)m. У більшості вуглеводів число атомів водню вдвічі перевищує кількість атомів кисню. Тому ці речовини і були названі вуглеводами. У тваринних клітинах вуглеводів небагато – 1-2, іноді до 5% (у клітинах печінки). Багаті на вуглеводи рослинні клітини, де їх зміст досягає 90% сухої маси (бульби картоплі).
Вуглеводи підрозділяють на прості і складні. Прості вуглеводи називаються моносахаридами. Залежно від числа атомів вуглецю в молекулі моносахариди називаються триозами (3 атоми), тетрозами (4 атоми), пентозами (5 атомів) або гексозами (6 атомів вуглецю).
Із шести-вуглецевих моносахаридів – гексоз – найбільш важливі глюкоза, фруктоза і галактоза. Глюкоза міститься в крові (0,1-0,12 %) і служить основним джерелом енергії для клітин і тканин організму. Пентози – рибоза і дезоксирибоза – входять до складу нуклеїнових кислот і АТФ. Якщо в одній молекулі об’єднуються два моносахариди, то таке з’єднання називають дисахаридом. До дисахариду відноситься харчовий цукор, який одержують з цукрової тростини або цукрового буряка. Він складається з однієї молекули глюкози і однієї молекули фруктози. Молочний цукор також є Димером і включає глюкозу і галактозу.
Складні вуглеводи, утворені багатьма моносахаридами багато кого, називаються полісахаридами. Мономером таких полісахаридів, як крохмаль, глікоген, целюлоза, є глюкоза.
Вуглеводи виконують дві основні функції: будівельну й енергетичну. Наприклад, целюлоза утворює стінки рослинних клітин; складний полісахарид хітин – головний структурний компонент зовнішнього скелета членистоногих. Будівельну функцію хітин виконує і у грибів. Вуглеводи відіграють роль основного джерела енергії в клітині. В процесі окислення 1 г вуглеводів звільняються 17,6 кДж енергії. Крохмаль у рослин і глікоген у тварин, відкладаючись у клітинах, служить енергетичним резервом.
Ліпіди (жири) і ліпоїди є обов’язковими компонентами всіх клітин. Жири є складними ефірами високомолекулярних жирних кислот і трьохатомного спирту гліцерину, а ліпоїди – жирних кислот з іншими спиртами. Ці сполуки нерозчинні у воді (гідрофобні). Ліпіди можуть утворювати складні комплекси із білками (ліпопротеїди), вуглеводами (гліколіпіди), залишками фосфорної кислоти (фосфоліпіди) тощо. Вміст жирів у клітині коливається від 5 до 15% маси сухої речовини, а в клітинах підшкірної жирової клітковини – до 90%.
Жири виконують будівельні/, енергетичну, запасаючу і захисну функції. Бімолекулярний шар ліпідів (переважно фосфоліпіди) утворює основу всіх біологічних мембран клітин. Ліпіди входять до складу оболонок нервових волокон. Жири є джерелом енергії: при повному розщеплюванні 1 г жиру вивільняється 38,9 кДж енергії. Вони служать джерелом води, що виділяється при їх окисленні. Жири є запасним джерелом енергії, нагромаджуючись у жировій тканині тварин і в плодах і насінні рослин. Вони захищають органи від механічних пошкоджень (наприклад, нирки оповиті м’яким жировим “футляром”). Нагромаджуючись у підшкірній жировій клітковині деяких тварин (кити, тюлені), жири виконують функцію теплоізоляції.
Нуклеїнові кислоти мають першорядне біологічне значення і є складними високомолекулярними біополімерами, мономерами яких є нуклеотиди. Вони вперше були знайдені в ядрах клітин, звідки і їх назва (nucleus – ядро).
Існують два типи нуклеїнових кислот: дезоксирибонуклеїнова (ДНК) і рибонуклеїнова (РНК). ДНК входить в основному в хроматин ядра, хоча невелика її кількість міститься і в деяких органоїдах (мітохондрії, пластиди). РНК міститься в ядерцях, рибосомах і в цитоплазмі клітини.
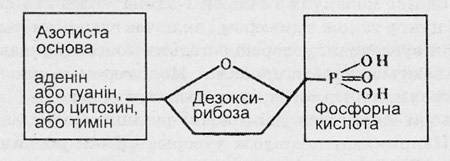
Рис. 127. Схема будови нуклеотиду.
Структура молекули ДНК була вперше розшифрована Дж. Уотсоном і Ф. Криком в 1953 р. Вона є двома полінуклеотидними ланцюгами, сполученими один з одним. Мономерами ДНК є нуклеотиди, в склад яких входять: п’ятивуглецевий цукор – дезоксирибоза, залишок фосфорної кислоти і азотна основа.
Нуклеотиди відрізняються один від одного тільки азотними основами. До складу нуклеотидів ДНК входять наступні азотні основи: аденін, гуанін, цитозин і тимін. Нуклеотиди з’єднуються в ланцюжок шляхом утворення ковалентних зв’язків між дезоксирибозою одного і залишком фосфорної кислоти сусіднього нуклеотиду. Обидва ланцюжки об’єднуються в одну молекулу водневими зв’язками, виникаючими між азотними основами різних ланцюжків, причому через певну просторову конфігурацію між аденіном і тиміном встановлюються два зв’язки, а між гуаніном і цитозином – три. Внаслідок цього нуклеотиди двох ланцюжків утворюють пари: А-Т, Г-Ц. Чітка відповідність нуклеотидів один одному в парних ланцюжках ДНК називається комплементарністю (додатковістю). Ця властивість лежить в основі реплікації (самоподвоєння) молекули ДНК, тобто утворення нової молекули на основі початкової.
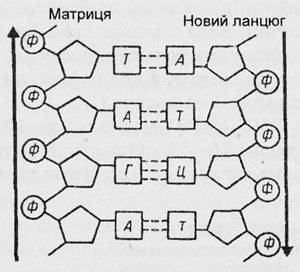
Рис. 128. Комплементарна сполука нуклеотидів і утворення дволанцюгової молекули ДНК.
Реплікація (від лат. replicatio – повторення) відбувається таким чином. Під дією спеціального ферменту (ДНК-полімерази) розриваються водневі зв’язки між нуклеотидами двох ланцюжків, і до зв’язків, що звільнилися, за принципом комплементарності приєднуються відповідні нуклеотиди ДНК (А-Т, Г-Ц). Отже, порядок нуклеотидів в “старому” ланцюжку ДНК визначає порядок нуклеотидів в “новому”, тобто “старий” ланцюжок ДНК є матрицею для синтезу “нового”. Такі реакції називаються реакціями матричного синтезу, вони характерні тільки для живого. Молекули ДНК можуть містити від 200 до 2×108 нуклеотидів. Beличезна різноманітність молекул ДНК досягається різними їх розмірами і різною послідовністю нуклеотидів.
Роль ДНК у клітині полягає в зберіганні, відтворенні і передачі генетичної інформації. Завдяки матричному синтезу спадкова інформація дочірніх клітин точно відповідає материнській.
РНК, як і ДНК, є полімером, побудованим з мономерів – нуклеотидів. Структура нуклеотидів РНК схожа з такою ДНК, але є наступні відмінності: замість дезоксирибози до складу нуклеотидів РНК входить п’яти вуглецевий цукор – рибоза, а замість азотної основи тиміна – урацил. Решта трьох азотних основ ті ж: аденін, гуанін і цитозин. У порівнянні з ДНК у склад РНК входить менше нуклеотидів і, отже, її молекулярна маса менше.
Відомі дво – і одноланцюжкові РНК. Дволанцюжкові РНК містяться в деяких вірусах, що виконуть (як і ДНК) роль охоронця і передавача спадкової інформації. У клітинах інших організмів зустрічаються одноланцюжкові РНК, які є копіями відповідних ділянок ДНК.
У клітинах існують три типи РНК: інформаційна, транспортна і рибосомальна. Інформаційна РНК (і-РНК) складається з 300-30 000 нуклеотидів і складає приблизно 5 % від всієї РНК, що міститься в клітині. Вона є копією певної ділянки ДНК (гена). Молекули і-РНК виконують роль переносників генетичної інформації від ДНК до місця синтезу білка (у рибосоми) і безпосередньо беруть участь у збиранні його молекул.
Транспортна РНК (т-РНК) складає до 10 % від всієї РНК клітини і складається з 75-85 нуклеотидів (рис. 129). Молекули т-РНК транспортують амінокислоти з цитоплазми в рибосоми.
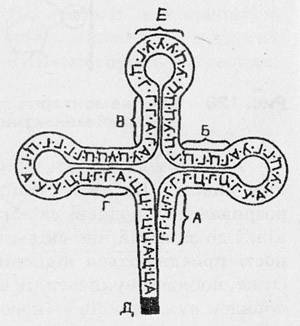
Рис. 129. Схема будови т-РНК. А, В, В, Г – ділянки комплементарної сполуки усередині одного ланцюжка РНК; Д – активний центр (ділянка сполуки з амінокислотою); Е – ділянка комплементарної сполуки з молекулою і РНК.
Основну частину РНК цитоплазми (близько 85 %) складає рибосомальна РНК (р-РНК). Вона входить до складу рибосом. Молекули р-РНК включають 3-5 тис.
Нуклеотидів. Вважають, що р-РНК забезпечує певне просторове взаєморозташування і-РНК і т-РНК.