Основні положення молекулярно-кінетичної теорії та їхнє дослідне обгрунтування
Розділ І ФІЗИКА ЯК ПРИ РОДНИЧА НАУКА. МЕТОДИ НАУКОВОГО ПІЗНАННЯ
&11. Основні положення молекулярно-кінетичної теорії та їхнє дослідне обгрунтування
✓ Як ви думаєте, чи можна побачити атоми речовини?
Молекулярно-кінетична теорія – це сучасне вчення про будову і властивості різних речовин. В основі цієї теорії лежать три основні положення:
1) усі тіла складаються з дрібних частинок – атомів та молекул;
2) атоми та молекули перебувають у безперервному безладному (хаотичному) русі;
3) між атомами та молекулами діють
Нижче будуть розглянуті експериментальні підтвердження цих положень.
1. Нині уже ніхто не сумнівається в існуванні атомів та молекул. У 70-х роках ХХ ст. за допомогою спеціального електронного мікроскопа, який дає збільшення у сотні тисяч і мільйони разів удалося розгледіти окремі атоми та молекули і навіть сфотографувати їх. До цього часу існували лише непрямі докази їхнього існування. На рис. 21 наведено фотографію вістря вольфрамової голки, зробленої за допомогою електронного мікроскопа. На цій фотографії круглі плями – це зображення окремих атомів Вольфраму.
2. Далі, розглянемо такий дослід. У мензурку наллємо розчин мідного купоросу. Цей розчин має темно-блакитний колір, він важчий за воду. Поверх нього обережно, щоб не змішати рідини, доливаємо шар чистої води, щоб між рідинами була чітка межа (рис. 22, а). Посудину залишимо у спокійному місці. Через два-три дні ми помітимо, що межа між рідинами розмивається (рис. 22, б). А через два-три тижні уся рідина у пробірці набуває блідо-блакитного кольору (рис. 22, в).
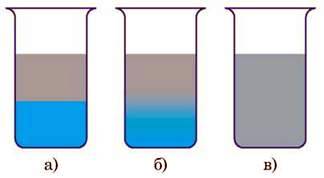
Рис. 22
У цьому досліді молекули мідного купоросу проникають у проміжки між молекулами води, а молекули води – у проміжки між молекулами мідного купоросу.
Явище самовільного взаємного проникнення контактуючих між собою речовин називається дифузією.
Дифузія є дослідним підтвердженням хаотичного руху молекул. Вона спостерігається і в газах. Якщо в кімнаті відкрити флакон з одеколоном, то через деякий час його запах пошириться по всій кімнаті. Це пояснюється тим, що молекули одеколону внаслідок свого хаотичного руху проникають у проміжки між молекулами повітря і навпаки. Дифузія в газах відбувається навіть швидше, ніж у рідинах.
Дифузія відбувається і в твердих тілах, хоча там вона відбувається дуже повільно, оскільки відстані між атомами твердих тіл значно менші, ніж у рідинах, а тим більше в газах. Було проведено такий дослід. Дві добре відполіровані плитки – свинцева і золота – притискали одна до одної і поміщали в піч з високою температурою, але нижчою, ніж температура плавлення свинцю. Приблизно через рік розглядали під мікроскопом шар на межі стикання плиток. У ньому було виявлено як наявність золота, так і наявність свинцю (рис. 23).
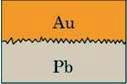
Рис. 23
Виникає запитання: від чого залежить швидкість дифузії? З наведених вище прикладів випливає, що дифузія залежить від агрегатного стану речовини: газ, рідина чи тверде тіло. Крім цього, виявляється, що вона істотно залежить і від температури: чим вища температура, тим швидше відбувається дифузія. Переконатися у цьому можна на такому досліді. Приготуймо дві посудини з розчином мідного купоросу і наллємо на нього шар чистої води, як описано вище. Одну посудину залишимо в кімнаті, а іншу поставимо у холодильник. Помітимо, що за той час, поки у посудині в кімнаті весь розчин набуде одноманітного забарвлення, у посудині в холодильнику рівень розчину купоросу ледве досягне половини посудини. Оскільки явище дифузії пов’язане з хаотичним рухом, то можна сказати, що температура – це фізична величина, яка характеризує інтенсивність теплового руху атомів чи молекул тіла. Чим температура вища, тим швидкість руху молекул більша і навпаки. Так, за кімнатної температури швидкість руху молекул газу складає сотні метрів за секунду.
У природі, техніці й побуті можна виявити чимало явищ, пов’язаних з дифузією: при фарбуванні тканини частинки фарби проникають у проміжки між частинками тканини, при склеюванні, паянні тощо. Дифузія відіграє важливу роль у житті рослин, тварин і людей. Так, кисень при диханні проникає в організм людини через поверхню легень, поживні речовини з кишківника дифундують у кров, поживні речовини з грунту через поверхню коренів надходять до рослин.
Підтвердженням існування та безперервного руху молекул є і так званий броунівський рух.

Роберт Броун
У 1827 р. англійський ботанік Р. Броун (1773-1858) спостерігав під мікроскопом рух спор у краплі води: вони безладно рухалися (рис. 24 – спора з положення 1 з часом переходить у положення 2). Рух спор довго пояснити не вдавалося. Сам Броун припускав, що спори рухаються тому, що вони живі. Але пізніше досліди були повторені з дрібно розмеленою фарбою і тушшю. І тільки згодом зрозуміли справжню причину броунівського руху. Ця причина – результат руху молекул води. Молекули води, в якій знаходиться броунівська частинка – спора чи частинка фарби – рухаються й ударяють її з різних боків. Причому з різних боків об частинку вдаряється не однакова кількість молекул і з різними швидкостями, що й призводить до хаотичного руху броунівської частинки.
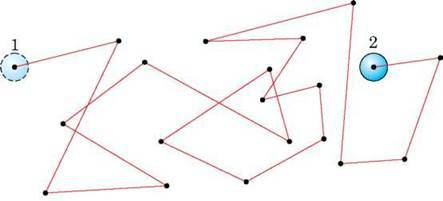
Рис. 24
Ми розглянули досліди, які підтверджують той факт, що молекули весь час перебувають у хаотичному русі. Проте особливості цього руху залежать від агрегатного стану речовини. У газах рух молекул цілком хаотичний. Тому гази не зберігають ні форми, ні об’єму, вони займають увесь об’єм посудини. Молекули рідини коливаються відносно деяких положень рівноваги і час від часу стрибкоподібно переміщаються у нові стабільні положення, відносно яких продовжують коливання. Тому рідина зберігає свій об’єм, але набуває форми посудини, в яку вона налита. У твердому тілі атоми (молекули, йони) настільки сильно взаємодіють між собою, що переважно коливаються відносно деяких положень рівноваги, а “перескакування” у нове положення відбувається дуже рідко. Тому тверді тіла зберігають і форму, і об’єм.
Спостереження показують, що тіла не розпадаються на окремі молекули, деякі з них трудно помітно розтягнути або стиснути. Як можна пояснити ці факти? Очевидно, що молекули притягуються одна до одної.
Проведемо такий дослід. Візьмемо два свинцеві циліндри, стиснемо їх основами, а потім відпустимо. Циліндри роз’єднаються. Далі, зачистимо основи циліндрів і дослід повторимо. Циліндри злипнуться. Вони не роз’єднаються, якщо навіть до нижнього циліндра підвісити вантаж масою у кілька кілограмів (рис. 25). Цей дослід можна пояснити так: циліндри утримуються разом унаслідок того, що між їхніми частинками діють сили притягання. Чому ці сили не проявлялися, поки ми циліндри не зачистили? Очевидно, поверхні циліндрів мали нерівності, які були усунуті при зачищенні, і до зачищення ми не змогли їх зблизити на малі відстані. Звідси можна зробити висновок, що сили притягання між атомами речовини проявляються тільки на малих відстанях.
Чому ж тоді, хоча між атомами й молекулами діють сили притягання, тіла не суцільні і між частинками існують проміжки? Чому тверді тіла й рідини трудно стиснути? Візьміть олівець або металевий стержень і попробуйте його помітно стиснути. Це зробити вам не вдасться. Причина – між частинками речовини, крім сил притягання, діють також сили відштовхування. Ці сили взаємно зрівноважуються, якщо на тіло не діють зовнішні сили. Взаємодія між атомами і молекулами – сили притягання і сили відштовхування – проявляються тільки на малих відстанях, приблизно таких, як розмір атома. Тому не можна, з’єднавши уламки розбитої чашки, отримати цілу чашку: відстані між уламками все одно будуть великими.

Рис. 25
Запитання для самоперевірки
1. Які основні положення молекулярно-кінетичної теорії?
2. Чи можна побачити окремі атоми та молекули?
3. Яке явище називається дифузією? Наведіть приклади дифузії.
4. Порівняйте швидкість дифузії в газах, рідинах і твердих тілах.
5. Чи пов’язана швидкість дифузії з температурою? Що характеризує температура?
6. Що таке броунівський рух?
7. Про що свідчать дифузія і броунівський рух?
8. Чому тіла самовільно не розпадаються на окремі атоми чи молекули?
9. Наведіть приклади дослідів, на яких можна спостерігати прояв сил притягання і сил відштовхування, що діють між частинками речовини.
10. Чому неможливо відновити розбиту чашку, якщо просто прикласти її уламки один до одного? Чому її можна склеїти?
Завдання 6
1. Чому дитячі повітряні кульки з часом зменшуються в об’ємі?
2. В якій воді – холодній чи гарячій – цукор розчиняється швидше? Чому?
3. Поясніть, чому частинки крейди, які залишилися на класній дошці після проведення записів, не відпадають від її поверхні.
4. Проведіть наступний дослід. Налийте воду у склянку і опустіть на дно кристалик марганцівки. Спостерігайте за процесом дифузії. Вимірюйте щодня висоту забарвленого стовпа води. Дані спостережень заносьте у зошит. Визначте, через який час забарвиться верхній шар води.
5. Проведіть спостереження дифузії у твердих тілах. Для цього візьміть невелику скляну пластинку, покладіть на неї кристалик марганцівки і покрийте його розплавленим парафіном. Помістіть пластинку в тепле місце і щодня спостерігайте за нею. Визначте, через який інтервал часу буде помітним результат дифузії.
