Питома теплоємність речовини
2-й семестр
ТЕПЛОВІ ЯВИЩА
4. Кількість теплоти. Теплові машини
Урок 7/49
Тема. Питома теплоємність речовини
Мета уроку: дати учням знання про питому теплоємність речовини, навчити розраховувати кількість теплоти в теплових процесах.
Тип уроку: урок вивчення нового матеріалу.
План уроку
Контроль знань | 5 хв. | 1. Що таке теплова рівновага? 2. Що можна сказати про температуру тіл, що перебувають у тепловій рівновазі? 3. На чому заснована дія газових і рідинних 4. Як треба користуватися термометром при вимірюванні температури? |
Демонстрації | 6 хв. | 1. Демонстрація на приладі “Теплоємність металів” виділення тілами рівної маси з різних речовин неоднакових кількостей теплоти під час їх охолодження. 2. Нагрівання рівних мас води й масла |
Вивчення нового матеріалу | 25 хв. | 1. Від чого залежить кількість теплоти, необхідна для нагрівання тіла? 2. Питома теплоємність речовини. 3. Порівняння питомих теплоємкостей різних речовин. 4. Рівняння теплового балансу |
Закріплення | 9 хв. | 1. Контрольні питання. 2. Навчаємося розв’язувати задачі. 3. Поміркуй і відповідай |
ВИВЧЕННЯ НОВОГО МАТЕРІАЛУ
1. Від чого залежить кількість теплоти, необхідна для нагрівання тіла?
Нам уже відомо, що внутрішня енергія тіла може змінюватися як шляхом виконання роботи, так і шляхом теплопередачі (без виконання роботи).
Енергію, яку одержує або втрачає тіло при теплопередачі, називають кількістю теплоти.
Познайомимося із приладом для кількісного вивчення теплових явищ. На рисунку ви бачите калориметр – прилад для вимірювання кількості теплоти. Найпростіший шкільний калориметр складається із двох склянок: внутрішнього алюмінієвого й зовнішнього пластмасового. Склянки розділені повітряним проміжком.
Як же підрахувати кількість теплоти Q, необхідну для нагрівання тіла?
По-перше, внутрішня енергія визначається швидкістю теплового руху частинок, з яких складається тіло, отже, кількість теплоти як міра зміни внутрішньої енергії пов’язана з температурою тіла. Якщо температура тіла зросла, то тіло одержало деяку кількість теплоти, якщо понизилася – то віддало. Таким чином, кількість теплоти залежить від зміни температури тіла:
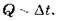
По-друге, кількість теплоти залежить також від маси тіла. Як показує досвід, чим більше маса тіла, тим більша кількість теплоти буде потрібна для нагрівання тіла до однієї й тієї самої температури. Звідси можна зробити висновок, що кількість теплоти пропорційна масі тіла:
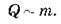
По-третє, маси молекул тіл різних речовин різні, тобто при однаковій зміні температури кількість теплоти, отримана або віддана цими тілами, буде різною. Таким чином, кількість теплоти Q залежить від роду речовини.
Кількість теплоти, передана тілу при нагріванні, залежить від роду речовини, з якої воно складається, від маси цього тіла й від зміни його температури.
2. Питома теплоємність речовини
Нагріємо на однакових пальниках дві посудини. Перша посудина містить воду, а друга – рослинне масло такої ж маси. Спостерігаючи за показаннями термометрів, ми побачимо, що масло нагрівається швидше. З’ясовуючи, чому це відбувається, ми приходимо до поняття питомої теплоємності речовини.
Питома теплоємність речовини показує, яка кількість теплоти необхідна, щоб змінити температуру 1 кг даної речовини на 1 °С.
Питома теплоємність позначається буквою с, її одиницею в СІ є 1 Дж/(кг-°С).
У різних речовин питома теплоємність має різні значення.
Так, наприклад, питома теплоємність цинку 400 Дж/(кг-°С).
Це означає, що для нагрівання цинку масою 1 кг на 1 °С необхідно затратити кількість теплоти, що дорівнює 400 Дж.
3. Порівняння питомих теплоємкостей різних речовин
Питома теплоємність – це характеристика речовини, й вона не залежить від маси тіла й зміни його температури.
Розглянемо таблицю питомих теплоємкостей деяких речовин.
Речовина | С, Дж/(кг-°С) | Речовина | С, Дж/(кг-°С) |
Золото | 130 | Алюміній | 920 |
Ртуть | 140 | Лід | 2100 |
Мідь | 400 | Спирт | 2500 |
Залізо | 460 | Вода | 4200 |
Вода, наприклад, має дуже велику питому теплоємність. Тому вода в морях й океанах, нагріваючись повільно, поглинає значну кількість теплоти. Завдяки цьому в тих місцях, які розташовані близько від великих водойм, улітку не буває так спекотно, як у місцях, віддалених від води.
Узимку вода, повільно остигаючи, віддає велику кількість теплоти, тому зима в цих умовах менш сувора. Саме завдяки великій питомій теплоємності вода широко використовується в системі водяного опалення, у побуті й медицині, наприклад у грілках.
Слід пам’ятати, що питома теплоємність речовини, що перебуває в різних агрегатних станах, різна.
Наприклад, ртуть у стані рідини має питому теплоємність 138 Дж/(кг-°С), а у твердому стані – 129 Дж/(кг-°С).
4. Рівняння теплового балансу.
Для розрахунку кількості теплоти, яку необхідно передати тілу масою т для нагрівання його від початкової температури t до кінцевої температури tп, можна скористатися формулою:
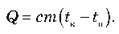
Наведене співвідношення справедливо й тоді, коли тіло не нагрівають, а охолоджують: у такому випадку кінцева температура tK нижче початкової температури tn й, отже, Q<0, тобто тіло віддає деяку кількість теплоти.
Розглянемо випадок, коли теплообмін відбувається тільки між двома тілами, тобто ні з якими іншими тілами вони теплом не обмінюються. Таку систему тіл називають теплоізольованою. Щоб зробити систему тіл теплоізольованою, тіла поміщають у калориметр.
Наллємо, наприклад, у калориметр воду й зануримо в неї мідний брусок, вийнятий з окропу. Між бруском і водою почнеться теплообмін, внаслідок якого незабаром установиться теплова рівновага: брусок і вода будуть мати однакову температуру – позначимо її t.
У процесі теплообміну вода одержить кількість теплоти, тому для води QB = cBmB(t – tп) > 0. Брусок же віддасть деяку кількість теплоти, тому для бруска QM = cMmM(t – tM) < 0. Систему “вода + брусок” ми вважаємо теплоізольованою, тому, відповідно до закону збереження енергії, QB + QM = 0, звідси одержуємо:
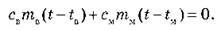
Це рівняння часто називають рівнянням теплового балансу.
Рівняння теплового балансу можна, звичайно, узагальнити на випадок декількох тіл: якщо система цих тіл теплоізольована, Q1 + Q2 + … + Qn = 0. Якщо тіло здобуває енергію при теплопередачі, то Q > 0. Якщо тіло віддає енергію при теплопередачі, то Q <с 0.
Питання до учнів у ході викладу нового матеріалу
Чому не можна тільки за зміною температури тіла судити про отриману ним кількість теплоти?
Від чого залежить кількість теплоти, яку необхідно передати тілу для нагрівання?
Питома теплоємність свинцю дорівнює 130 Дж/(кг-°С). Що це означає?
Що ефективніше використати як грілку – 2 кг води чи 2 кг піску за тієї ж температурі?
ЗАКРІПЛЕННЯ ВИВЧЕНОГО МАТЕРІАЛУ
1). Навчаємося розв’язувати задачі
1. Залізному тягарцеві масою 100 г передали 920 Дж теплоти. На скільки градусів нагрівся тягарець?
2. Яка питома теплоємність речовини, якщо для нагрівання 1 кг цієї речовини на 2 °С потрібна була кількість теплоти 1 кДж?
3. Для нагрівання цегельної печі масою 1,5 т витрачено 26,4 МДж теплоти. До якої температури нагріли піч, якщо початкова температура була 10 °С?
Розв’язок. Відповідно до визначення, Q = cm(t2 – t1). Звідси знаходимо кінцеву температуру печі:
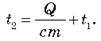
Перевіряємо одиниці величин:
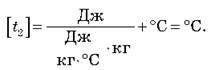
З таблиці знаходимо, що питома теплоємність цегли дорівнює 880 Дж/(кг-°С). Обчислюємо температуру печі:
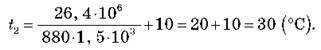
Відповідь: піч нагрілася до 30 °С.
2). Поміркуй і відповідай
1. Чим пояснюється, що в пустелях дуже великі добові перепади температур?
2. Які особливості клімату обумовлені великою питомою теплоємністю води?
3. У міських парках установлюють фонтани. Чому спекотного дня поблизу фонтану відчувається прохолода?
4. У якому випадку гаряча вода в склянці остудиться більше: якщо в склянку опустити срібну ложку чи таку саму алюмінієву? Чому?
5. Для охолодження інструментів, що нагріваються при роботі (різців, свердел), часто використовують воду. Чим можна пояснити цей факт?
Домашнє завдання-1
1. У-1: § 24.
2. Сб-1:
Рів1 – № 27.1, 27.2, 27.3, 27.9, 27.10.
Рів2 – № 27.15, 27.16, 27.21, 27.22, 27.23.
Рів3 – № 27.27, 27.28, 27.29, 27.32.
Домашнє завдання-2
1. У-2: § 39, 40.
2. Сб-2:
Рів1 – № 28.2, 28.3, 28.4, 28.5, 28.6.
Рів2 – № 28.7, 28.10, 28.11, 28.17, 28.19.
Рів3 – № 28.25, 28.26, 28.28, 28.31, 28.32.