Пояснення зміни агрегатних станів речовини на підставі атомно-молекулярного вчення
2-й семестр
ТЕПЛОВІ ЯВИЩА
4. Кількість теплоти. Теплові машини
Урок 19/61
Тема. Пояснення зміни агрегатних станів речовини на підставі атомно-молекулярного вчення
Мета уроку: узагальнити знання учнів про агрегатні стани речовини й пояснити їх на основі атомно-молекулярного вчення.
Тип уроку: урок узагальнення знань.
План уроку
Контроль знань | 5 хв. | Самостійна робота № 23 “Випаровування й конденсація. Кипіння” |
Вивчення нового матеріалу | 24 | Узагальнення й систематизація знань за темою “Зміна агрегатних станів речовини” |
Закріплення вивченого матеріалу | Хв. | Поміркуй і відповідай |
МЕТОДИЧНІ РЕКОМЕНДАЦІЇ
Урок доцільно побудувати за схемою узагальнення й систематизації знань. При вивченні агрегатних станів речовини головну увагу приділяють тій частині внутрішньої енергії, що залежить від енергії взаємодії частинок. Залежно від співвідношення між потенціальною енергією взаємодії й кінетичною енергією руху частинок речовина може перебувати в одному із трьох агрегатних
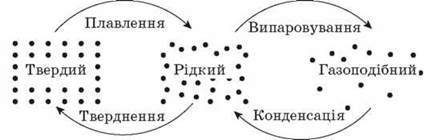
Молекулярно-кінетична теорія будови речовини – одне з найбільших досягнень фізичної науки – заснована на трьох твердженнях:
1) усяка речовина складається із частинок – молекул або атомів;
2) частинки здійснюють безладний тепловий рух;
3) частинки взаємодіють одна з одною.
Ця теорія дозволяє зрозуміти безліч найрізноманітніших явищ, у тому числі факт існування речовини в трьох агрегатних станах. Чому ж сукупності зовсім однакових частинок, наприклад молекул води, можуть утворити такі настільки не схожі одне на одного тіла, як лід, вода, водяна пара? “Винним” у цьому є третє з перерахованих вище тверджень, що лежать в основі МКТ, – твердження про те, що між молекулами діють сили. Однак існування різних агрегатних станів зручніше пояснювати, користуючись не “силовою”, а “енергетичною” мовою.
Тепловий рух молекул характеризується їх середньою кінетичною енергією. Вона, як відомо, визначає температуру тіл. Якби молекули мали тільки кінетичну енергію, вони розлетілися б в усіх напрямках (рух молекул хаотичний!) і речовина зайняла б весь доступний їй об’єм. Єдиним можливим станом речовини був би газоподібний стан.
Взаємодія молекул характеризується потенціальною енергією. Вона залежить від відстані між молекулами. Якби молекули мали тільки потенціальну енергію, вони зайняли б одна відносно одної такі положення, щоби сума сил, які діють на кожну молекулу з боку її сусідів, дорівнювала б нулю. При цьому потенціальна енергія взаємодії молекул була б мінімальною. Єдиним можливим станом речовини був би твердий стан.
Але молекули рухаються й взаємодіють одночасно, отже, вони володіють і кінетичною й потенціальною енергією. Тож чи бути тілу твердим, рідким або газоподібним, залежить від співвідношення обох видів енергії. А зміна цього співвідношення й призводить до переходу речовини з одного стану в інший.
1. Твердий стан – це стан, у якому абсолютне значення потенціальної енергії Еп взаємодії молекул надзвичайно велике порівняно з кінетичною Ек:
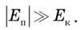
Як можна змінити це співвідношення? Наприклад, нагріваючи тверде тіло. При нагріванні збільшується кінетична енергія частинок тіла, а їхня потенціальна енергія при цьому практично не змінюється. Таким чином, можна досягти того, щоб кінетична енергія стала приблизно рівною потенціальній.
2. Тоді й відбудеться перехід із твердого стану в рідкий, для якого характерна наведена рівність:
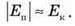
У цьому стані абсолютне значення потенціальної енергії ще досить велике, щоб молекули не могли розлетітися одна від одної, а кінетична енергія вже досить велика, щоб молекули набули певної рухливості, тобто можливості переміщатися усередині об’єму. Рідина зберігає свій об’єм, але стає текучою й тому не зберігає своєї форми.
3. Продовжуємо нагрівати рідину. Кінетична енергія молекул буде рости й у якийсь момент перевершить потенціальну енергію їх взаємодії настільки, що нею можна буде знехтувати:
|Еп| ” Ек.
Речовина перейде в газоподібний стан.
ЗАКРІПЛЕННЯ ВИВЧЕНОГО МАТЕРІАЛУ
Поміркуй і відповідай
1. Чому дощ охолоджує повітря? Чому фонтани зменшують спеку?
2. Чайник шумить перед закипанням води в ньому. Чому?
3. Поясніть принцип парового приготування їжі.
4. Холодильник час від часу доводиться вимикати й розморожувати. Чому?
Домашнє завдання-1
1. У-1: § 27.
2. Сб-1:
Рів1 – № 30.31, 30.32, 30.33, 30.36.
Рів2 – № 30.37, 30.38, 30.40, 30.45, 30.46.
Рів3 – № 30.56, 30.57, 30.58, 30.64.
Домашнє завдання-2
1. У-2: § 46 (п. 2).
2. Сб-2:
Рів1 – № 33.20, 33.34, 33.35.
Рів2 – № 33.23, 33.24, 33.25.
Рів3 – № 33.45, 33.47, 33.52, 33.53.