Середня і миттєва швидкість – Швидкість реакції
ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ
2. Швидкість реакції
2.2 . Середня і миттєва швидкість
У ході реакції її швидкість зазвичай зменшується. Тобто швидкість реакції непостійна. Наведені вище значення швидкості є лише середніми значеннями.
Математично середня швидкість у певному інтервалі часу між t1 і t2 визначається з нахилу січної на діаграмі залежності концентрації від часу.
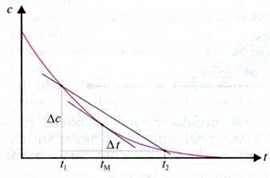
Увага: при експериментальному визначенні середньої швидкості реакції зазвичай виходять з часу, що минув між початком і завершенням реакції.
Швидкість реакції в певний момент часу tм – це миттєва швидкість. На діаграмі залежності концентрації від часу вона визначається з кута нахилу дотичної на графіку для t= tM.
Перехід від середньої швидкості до миттєвої визначається шляхом обчислення граничного значення для будь-якого короткого проміжку часу ∆t.
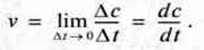
Related posts:
- ШВИДКІСТЬ ХІМІЧНОЇ РЕАКЦІЇ – ХІМІЧНА КІНЕТИКА. ШВИДКІСТЬ І МЕХАНІЗМ ХІМІЧНИХ РЕАКЦІЙ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ХІМІЧНА КІНЕТИКА. ШВИДКІСТЬ І МЕХАНІЗМ ХІМІЧНИХ РЕАКЦІЙ ШВИДКІСТЬ ХІМІЧНОЇ РЕАКЦІЇ Швидкість і механізм хімічної реакції вивчає хімічна кінетика. Швидкість хімічної реакції характеризується зміною концентрації однієї з вихідних речовин або кінцевих продуктів за одиницю часу. Середня швидкість реакції: Де с1 і с2 – початкова і кінцева концентрація речовини; τ1 і […]...
- Швидкість хімічної реакції – Хімічні реакції Хімія Загальна хімія Хімічні реакції Швидкість хімічної реакції Швидкість хімічної реакції Визначається кількістю речовини, що прореагувала за одиницю часу в одиниці об’єму. Формула середньої швидкості хімічної реакції: де – середня швидкість хімічної реакції, – зміна концентрації реагенту, – час. Чинники, що впливають на швидкість хімічної реакції 1) Природа реагуючих речовин. 2) Агрегатний стан реагуючих речовин. […]...
- Опис швидкості реакції – Швидкість реакції ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ 2. Швидкість реакції 2.3 . Опис швидкості реакції Швидкість реакції можна описати як зміну концентрації початкової речовини і як зміну продукту реакції за певний проміжок часу. І в одному і в іншому випадку за певний проміжок часу вона визначається за кутом нахилу січної відповідного графіка с(t). В один і той самий проміжок […]...
- Визначення – Швидкість реакції ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ 2. Швидкість реакції У ході хімічної реакції кількість початкових речовин постійно зменшується, а кількість продуктів реакції відповідно збільшується. Зміну кількості початкових речовин чи продуктів реакції за певний проміжок часу називають швидкістю реакції. 2.1. Визначення Швидкість реакції v визначається як зміна кількості п речовини за певний проміжок часу: ∆n – зміна кількості речовини […]...
- Чинники, що визначають швидкість реакції – Швидкість реакції ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ 2. Швидкість реакції 2.4 . Чинники, що визначають швидкість реакції Згідно з теорією зіткнення, реакція відбувається лише за певних умов: – частинки, які реагують між собою, повинні зіштовхнутися одна з одною; – частинки повинні зіштовхуватися в сприятливому для них положенні; – частинки повинні мати достатню кінетичну енергію, оскільки реакція проходить лише при […]...
- Швидкість хімічної реакції – ХІМІЧНІ РЕАКЦІЇ ТА ЗАКОНОМІРНОСТІ ЇХ ПЕРЕБІГУ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЧНІ РЕАКЦІЇ ТА ЗАКОНОМІРНОСТІ ЇХ ПЕРЕБІГУ Швидкість хімічної реакції Хімічні реакції відрізняються одна від одної тривалістю їхнього протікання. Деякі хімічні реакції відбуваються миттєво (наприклад, вибух воднево-кисневої суміші, реакції обміну з утворенням осаду), інші – досить швидко (горіння речовин), треті – повільно (більшість реакцій […]...
- Фактори, що впливають на швидкість реакції ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 4. ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ. § 4.2. Фактори, що впливають на швидкість реакції Швидкість хімічної реакції залежить від природи речовин, що реагують, і умов перебігу реакції: концентрації с, температури t, наявності каталізаторів, а також від деяких інших факторів (наприклад, від тиску – […]...
- Швидкість хімічної реакції – Приклади розв’язування типових задач – Урок 5 – Хімічна реакція ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 4. Хімічна реакція Приклади розв’язування типових задач І. Швидкість хімічної реакції Формули і поняття, які використовуються: Де v1 – швидкість прямої реакції, V2 – швидкість зворотної реакції, A, Б – реагенти реакції, B, Г – продукти реакції, С(А), с(Б) – концентрації реагентів, С(В), […]...
- Нерівномірний прямолінійний рух. Середня швидкість Розділ ІІ МЕХАНІЧНИЙ РУХ &18. Нерівномірний прямолінійний рух. Середня швидкість ✓ Який механічний рух називають рівномірним? ✓ Як визначити швидкість тіла під час рівномірного руху? 1. Рівномірний рух зустрічається в природі нечасто. Строго кажучи, ідеально рівномірно не може рухатися жодне тіло, але можна створити такі умови, за яких рух відбуватиметься практично рівномірно. Спробуйте уявити собі, […]...
- НЕРІВНОМІРНИЙ ПРЯМОЛІНІЙНИЙ РУХ. СЕРЕДНЯ ШВИДКІСТЬ НЕРІВНОМІРНОГО РУХУ Тип уроку: комбінований урок. Мета: ознайомити учнів з одним із видів механічного руху – нерівномірним прямолінійним рухом, увести поняття середньої швидкості. Показати учням практичну значущість набутих знань. Продовжувати формувати вміння грамотно оформлювати задачі. Обладнання та наочність: демонстрування нерівномірного руху, комп’ютерні презентації. Відеофрагмент: нерівномірний рух різних об’єктів (потяг, автомобіль, велосипедист). Хід уроку I. ОРГАНІЗАЦІЙНИЙ ЕТАП II. […]...
- Швидкість хімічної реакції, залежність швидкості реакції від різних факторів Тема 2 ХІМІЧНІ РЕАКЦІЇ Урок 23 Тема уроку. Швидкість хімічної реакції, залежність швидкості реакції від різних факторів Цілі уроку: формувати уявлення учнів про швидкість хімічної реакції, вплив на неї різних факторів; показати залежність швидкості хімічної реакції від природи речовини, температури, концентрації; розвивати навички й уміння складати рівняння хімічних реакцій, розпізнавати типи реакцій за рівняннями реакції; […]...
- Молекулярність реакції – Вираження швидкості реакції ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ 3. Вираження швидкості реакції Згідно з теорією зіткнення, збільшення вдвічі кількості частинок реагенту в певному об’ємі веде до збільшення кількості зіткнень вдвічі і, відповідно, до збільшення швидкості реакції вдвічі. При збільшенні втричі концентрації частинок відбувається збільшення швидкості реакції втричі і т. д. 3.1 . Молекулярність реакції Реакції, в яких від початкових речовин […]...
- Швидкість хімічної реакції. Каталізатор – Хімічна реакція ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 4. Хімічна реакція 4.8. Швидкість хімічної реакції. Каталізатор Розділ хімії, що вивчає швидкість хімічних реакцій, називають хімічною кінетикою. Розгляньмо зміст деяких понять, які використовують у цьому розділі. Швидкість хімічних реакцій характеризується зміною концентрації реагентів (або продуктів реакції) за одиницю часу. Якщо реакції відбуваються […]...
- Швидкість прямолінійного нерівномірного руху – Кінематика 5. Механіка 5.1. Кінематика 5.1.15. Швидкість прямолінійного нерівномірного руху Прямолінійний нерівномірний рух – це рух фізичного тіла (матеріальної точки), швидкість якого з часом змінюється, тобто тіло за рівні проміжки часу здійснює неоднакові переміщення. Середня швидкість – це векторна фізична величина, яка характеризує нерівномірний прямолінійний рух і чисельно дорівнює відношенню переміщення, здійсненого тілом (матеріальною точкою), до […]...
- НЕРІВНОМІРНИЙ РУХ. СЕРЕДНЯ ШВИДКІСТЬ НЕРІВНОМІРНОГО РУХУ Розділ 2 МЕХАНІЧНИЙ РУХ & 11. НЕРІВНОМІРНИЙ РУХ. СЕРЕДНЯ ШВИДКІСТЬ НЕРІВНОМІРНОГО РУХУ Напевне, вам траплялося їхати автобусом або потягом від одного міста до іншого. Згадайте: транспортний засіб час від часу гальмує, зупиняється, потім знову набирає швидкість… Стрілка спідометра весь час коливається і тільки іноді завмирає на місці. Чи можна назвати такий рух рівномірним? Звичайно, ні. […]...
- Нерівномірний рух. Середня швидкість РОЗДІЛ I МЕХАНІЧНИЙ РУХ УРОК № 5/5 Тема уроку. Нерівномірний рух. Середня швидкість Тип уроку: засвоєння нових знань. Мета уроку: навчати розрізняти види механічного руху за зміненням швидкості тіла; формувати навички розв’язування задач; увести поняття середньої швидкості. Обладнання: кулька, похилий жолоб. План уроку Етапи Час Прийоми і методи I. Перевірка домашнього завдання 5-7 хв. Записи […]...
- Швидкість хімічних реакцій ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 4. ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ. § 4.1. Швидкість хімічних реакцій Суть хімічних реакцій зводиться до розриву зв’язків у вихідних речовинах і виникнення нових зв’язків у продуктах реакції. При цьому загальне число атомів кожного елемента до і після реакції залишається сталим. Оскільки утворення […]...
- СЕРЕДНЯ ШВИДКІСТЬ ТЕПЛОВОГО РУХУ ОДНОАТОМНИХ МОЛЕКУЛ. ДОСЛІД ШТЕРНА Фізика підготовка до ЗНО комплексне видання МОЛЕКУЛЯРНА ФІЗИКА І ТЕРМОДИНАМІКА 1. ОСНОВИ МОЛЕКУЛЯРНО-КІНЕТИЧНОЇ ТЕОРІЇ 1.7 СЕРЕДНЯ ШВИДКІСТЬ ТЕПЛОВОГО РУХУ ОДНОАТОМНИХ МОЛЕКУЛ. ДОСЛІД ШТЕРНА Середня швидкість теплового руху одноатомних молекул: – універсальна газова стала, що дорівнює добутку сталої Больцмана і сталої Авогадро: Дослід Штерна (1920) дає змогу визначити середню швидкість руху молекул експериментально за формулою Де […]...
- НЕРІВНОМІРНИЙ ПРЯМОЛІНІЙНИЙ РУХ. СЕРЕДНЯ ШВИДКІСТЬ НЕРІВНОМІРНОГО РУХУ Розділ 2 МЕХАНІЧНИЙ РУХ & 20. НЕРІВНОМІРНИЙ ПРЯМОЛІНІЙНИЙ РУХ. СЕРЕДНЯ ШВИДКІСТЬ НЕРІВНОМІРНОГО РУХУ Нерівномірний рух. У живій та неживій природі є небагато тіл, які рухаються рівномірно протягом тривалого часу. Лише на прямій автостраді автомобіль може деякий час рухатися зі сталою швидкістю. На міських вулицях водію доводиться часто змінювати швидкість свого транспортного засобу: зупинятися перед світлофорами […]...
- ПРЯМОЛІНІЙНИЙ НЕРІВНОМІРНИЙ РУХ. СЕРЕДНЯ ШВИДКІСТЬ НЕРІВНОМІРНОГО РУХУ Роздiл 2 МЕХАНІЧНИЙ РУХ &19. ПРЯМОЛІНІЙНИЙ НЕРІВНОМІРНИЙ РУХ. СЕРЕДНЯ ШВИДКІСТЬ НЕРІВНОМІРНОГО РУХУ Більшість рухів у природі є нерівномірними. Наприклад, автобус, відходячи від зупинки, за однакові інтервали часу проїжджає дедалі більший шлях, а наближаючись до зупинки, – навпаки. Бігун, беручи участь у змаганнях, затрачає на подолання однакових за довжиною кіл різний час. Рух автобуса і бігуна […]...
- Порядок реакції – Вираження швидкості реакції ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ 3. Вираження швидкості реакції 3.2 . Порядок реакції На основі теорії зіткнення для різних типів молекулярних реакцій можна записати вирази для швидкості реакції: Константа k – константа швидкості реакції. Через спільний вплив різних чинників на швидкість реакції результати експериментів часто не відповідають теоретичним припущенням. Тому певна реакція описується експериментально виведеним рівнянням (виразом) […]...
- ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ – КИСЕНЬ Хімія – універсальний довідник КИСЕНЬ ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ Швидкість реакції – це кількість речовини, що реагує за одиницю часу. Залежно від умов одна і та ж реакція може протікати з різною швидкістю. Так, при збільшенні кількості речовини, що реагує в одиниці об’єму, тобто його концентрації, швидкість реакції зростає, тому що зростає число зіткнень частинок, що […]...
- КАТАЛІЗ – ХІМІЧНА КІНЕТИКА. ШВИДКІСТЬ І МЕХАНІЗМ ХІМІЧНИХ РЕАКЦІЙ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ХІМІЧНА КІНЕТИКА. ШВИДКІСТЬ І МЕХАНІЗМ ХІМІЧНИХ РЕАКЦІЙ КАТАЛІЗ Каталіз – це зміна швидкості хімічної реакції речовинами (каталізаторами), які беруть участь у реакції, але не входять до складу кінцевих продуктів. За участю каталізатора хімічна рівновага системи досягається швидше, ніж без нього. Вплив у каталізатора на швидкість реакції досягають за рахунок […]...
- РІВНОМІРНИЙ РУХ – ПРЯМОЛІНІЙНИЙ РУХ Фізика підготовка до ЗНО комплексне видання МЕХАНІКА 1. ОСНОВИ КІНЕМАТИКИ 1.4. ПРЯМОЛІНІЙНИЙ РУХ 1.4.1. РІВНОМІРНИЙ РУХ Прямолінійним рівномірним рухом називають рух, при якому тіло (матеріальна точка) за будь-які рівні проміжки часу здійснює однакове переміщення, або рух зі сталою швидкістю вздовж прямої: Рівняння рівномірного прямолінійного руху тіла Рівняння руху в скалярному вигляді: Якщо тіло рухається вздовж […]...
- ТЕПЛОВИЙ ЕФЕКТ РЕАКЦІЇ. ЕНТАЛЬПІЯ РЕАКЦІЇ – ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ ТЕПЛОВИЙ ЕФЕКТ РЕАКЦІЇ. ЕНТАЛЬПІЯ РЕАКЦІЇ Кількість теплоти Q, яку передали системі, йде на зміну її внутрішньої енергії ΔUі на здійснення системою роботи* W проти зовнішніх сил (зовнішнього тиску р) (рис. 32): Рис. 32. Робота, яку виконує хімічна система проти зовнішнього тиску (поршень невагомий). Вуглекислий газ, який […]...
- Швидкість – Кінематика 5. Механіка 5.1. Кінематика 5.1.10. Швидкість Швидкість – векторна величина, яка дорівнює відношенню переміщення точки за будь-який інтервал часу до значення цього інтервалу. Вона характеризує швидкоплинність будь-якого процесу. При рівномірному русі вона чисельно дорівнює відношенню пройденого шляху s до проміжку часу t, за який цей шлях пройдено Вектор швидкості спрямований по дотичній до траєкторії. Швидкість […]...
- Рівномірний прямолінійний рух. Швидкість рівномірного прямолінійного руху МЕХАНІКА РОЗДІЛ 2. МЕХАНІЧНИЙ РУХ § 17. Рівномірний прямолінійний рух. Швидкість рівномірного прямолінійного руху Запитання до вивченого 1. Рівномірним рухом називають такий рух, під час якого тіло за будь-які однакові інтервали часу проходить однаковий шлях. Прикладом рівномірного руху є рух точки земної поверхні під час обертання Землі навколо своєї осі. За рівномірний рух можна прийняти […]...
- РІВНЯННЯ РУХУ. ГРАФІКИ РІВНОМІРНОГО ПРЯМОЛІНІЙНОГО РУХУ Роздiл 2 МЕХАНІЧНИЙ РУХ &18. РІВНЯННЯ РУХУ. ГРАФІКИ РІВНОМІРНОГО ПРЯМОЛІНІЙНОГО РУХУ Рівномірний прямолінійний рух тіла дуже зручно представляти і вивчати у вигляді графіків залежності шляху, пройденого тілом, від часу його руху (графік руху) і залежності швидкості тіла від часу його руху (графік швидкості). Розглянемо приклад. Нехай автомобіль рухається з Києва до Одеси зі швидкістю 100 […]...
- Хімічна рівновага – Хімічні реакції Хімія Загальна хімія Хімічні реакції Хімічна рівновага Хімічні реакції, які за одних і тих самих умов можуть іти в протилежних напрямах, називаються оборотнимИ. У випадку, якщо за даних умов реагенти повністю перетворюються на продукти реакції, реакції називаються НеоборотнимИ. Умови необоротності хімічних реакцій 1) Продукти, що утворюються, виводяться зі сфери реакції – випадають у вигляді осаду, […]...
- Тепловий ефект реакції. Екзотермічні й ендотермічні реакції. Термохімічні рівняння Тема 2 ХІМІЧНІ РЕАКЦІЇ Урок 24 Тема уроку. Тепловий ефект реакції. Екзотермічні й ендотермічні реакції. Термохімічні рівняння Цілі уроку: розширити уявлення про хімічні реакції на прикладі ендотермічних і екзотермічних реакцій; ознайомити учнів з поняттями “тепловий ефект хімічної реакції”, “термохімічні рівняння”; формувати навички й уміння складати термохімічні рівняння реакцій, розв’язувати задачі з їх використанням. Тип уроку: […]...