Теплова рівновага. Температура
2-й семестр
МОЛЕКУЛЯРНА ФІЗИКА Й ТЕРМОДИНАМІКА
2. Основи термодинаміки
– Теплові явища
– Внутрішня енергія тіл
– Перший закон термодинаміки
– Теплові двигуни
Тематичне планування
№ п/п | Тема уроку | Дата проведення |
1 | Теплова рівновага. Температура | |
2 | Внутрішня енергія | |
3 | Робота в термодинаміці | |
4 | Перший закон термодинаміки | |
5 | Наслідки | |
6 | Теплові машини | |
7 | Незворотність теплових процесів | |
8 | Тематичне оцінювання з теми “Основи термодинаміки” |
Урок 1/90
Тема. Теплова рівновага. Температура
Мета уроку: ознайомити учнів з умовою теплової рівноваги, поглибити і розширити поняття про температуру
Тип уроку: вивчення нового матеріалу
План уроку
Демонстрації | 4 хв. | Вимірювання температури |
Вивчення нового матеріалу | 31 | 1. Теплова рівновага. 2. Температура. 3. Вимірювання температури. |
Закріплення вивченого матеріалу | 10 хв. | 1. Тренуємося розв’язувати задачі. 2. Контрольні питання. |
ВИВЧЕННЯ НОВОГО МАТЕРІАЛУ
1. Теплова рівновага
Щодня ми стикаємося з тілами, що знаходяться в різних станах, для яких характерні певні параметри. Наприклад, шматок льоду, принесений в кімнату взимку, і повітря в кімнаті мають різну температуру. Через деякий час у результаті теплообміну між льодом і повітрям температура льоду підвищиться, а повітря знизиться, лід розтане, вода, що утворилася з нього нагріється, температура води та повітря в кімнаті буде однаковою.
Кажуть, що між водою і повітрям встановилася теплова, або термодинамічна рівновага, а макроскопічні системи являють собою термодинамічну систему.
O Термодинамічна система – сукупність макроскопічних систем, які можуть обмінюватися енергією між собою та з зовнішніми тілами. Термодинамічну систему, яка не бере участі в теплообміні з навколишніми тілами, називають теплоізольованою.
Теплоізольована термодинамічна система з плином часу завжди приходить в стан теплової рівноваги, з якої сама вийти не може. Це твердження розкриває зміст закону термодинамічної рівноваги.
Рівноважний стан характеризується незмінністю в часі всіх термодинамічних параметрів стану теплоізольованої системи. Наприклад, якщо налити в склянку гарячу воду і залишити її в кімнаті, то через деякий час склянка і вода в ній прийдуть у стан термодинамічної рівноваги з повітрям і предметами, що знаходяться в кімнаті. При цьому температура, тиск і об’єм залишаться незмінними, як завгодно довго за відсутності зовнішніх впливів.
2. Температура
У повсякденному житті температура – величина, яка відрізняє “гаряче” від “холодного”. І перші уявлення про температуру виникли з відчуттям тепла і холоду. Температура характеризує ступінь нагрітого тіла.
Про відмінність ступенів нагрітості тіл судять з процесу теплопередачі, що виникає під час теплового контакту тіл.
Основна властивість температури полягає в наступному: якщо привести в зіткнення два тіла – холодне і гаряче, то холодне тіло почне нагріватися, а гаряче – охолоджуватись. Температура кожного з тіл буде змінюватися з плином часу доти, поки температури тіл не стануть однаковими. Ми говоримо, що тіла прийдуть в стан теплової рівноваги.
Отже, температура характеризує стан теплової рівноваги: всі тіла, що знаходяться в тепловій рівновазі, мають однакову температуру.
Ця властивість відрізняє температуру від інших параметрів стану, наприклад об’єму або тиску. їх значення в стані теплової рівноваги з часом також не змінюються, але не є однаковими в усіх частинах системи рівноваги.
3. Вимірювання температури
Для вимірювання температури слід взяти до уваги, що під час зміни температури тіла змінюються і його властивості. Змінюються, відповідно, величини, що характеризують ці властивості. Тому для створення приладу, що вимірює температуру, тобто термометра, обирають будь-яку речовину (термометричну речовину) і визначають величину, яка характеризує властивість речовини (термометричну величину).
У медичних термометрах, наприклад, термометричною речовиною є ртуть, а термометричною величиною – довжина ртутного стовпчика.
Найчастіше на практиці використовують залежність об’єму рідини (ртуті або спирту) від температури. Для вимірювання температури можна скористатися залежністю будь-якої макроскопічної величини від температури: об’єму, тиску, електричного опору і т. д.
При визначенні температурної шкали в якості “опорних точок” використовують температуру танення льоду і температуру кипіння води при атмосферному тиску. Шкалу між точками 0 і 100 ділять на 100 рівних частин, які називають градусами. Переміщення стовпчика рідини на одну поділку відповідає зміні температури на 1 °С.
Побудована таким чином шкала є досить зручною для практичних цілей, хоча вона має ряд недоліків. По-перше, опорні точки вибрані довільно, так само як довільним є і поділ інтервалу між ними на 100 частин. По-друге, при побудові шкали вважають, що об’єм термометричного тіла під час зміни температури змінюється рівномірно на всьому температурному інтервалі, проте, це не так.
Термодинамічна (абсолютна) шкала температур будується наступним чином. Обирається одна постійна точка – потрійна точка води, тобто температура, за якої вода, лід і пара існують одночасно. Температура потрійної точки води становить 0,01 °С, а тиск, при якому вона існує, 609 Па. За нуль термодинамічної шкали температур прийнято вважати температуру -273 °С. Цю температуру називають абсолютним нулем температур.
Було встановлено, що при постійному об’ємі і температурі тиск газу прямо пропорційний його концентрації: р = nkT, де k – коефіцієнт пропорційності – постійна Больцмана. Постійна Больцмана зв’язує температуру з середньою кінетичної енергії руху молекул в речовині.
Згадаємо основне рівняння молекулярно-кінетичної теорії ідеального газу: 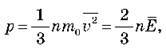 де
де 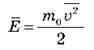 – середня кінетична енергія поступального руху молекули.
– середня кінетична енергія поступального руху молекули.
З виразів для тиску можна отримати: 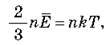 звідки
звідки 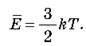 Отже,
Отже,
O абсолютна температура є мірою середньої кінетичної енергії руху молекул.
Цей висновок доводить правильність експериментальних даних, які показують збільшення швидкості частинок речовини зі зростанням температури.
Питання до учнів під час викладення нового матеріалу
1. Що розуміють під тепловою рівновагою тіл?
2. Який стан називають станом теплової рівноваги?
3. Чим температура як параметр стану теплової рівноваги відрізняється від інших параметрів?
4. Як пов’язана середня кінетична енергія руху молекул з термодинамічною температурою?
ЗАКРІПЛЕННЯ ВИВЧЕНОГО МАТЕРІАЛУ
1). Тренуємося розв’язувати задачі
1. Нормальна температура людського тіла близько 37 °С. Чому ж нам не холодно за температури повітря 25 °С і дуже жарко за 37 °С?
Розв’язок
Тіло людини безперервно виділяє тепло, яке віддається навколишньому повітрю. За температури повітря, близької до 37 °С, процес тепловіддачі сповільнюється, і в тілі накопичується надмірна внутрішня енергія.
2. Тіло А знаходиться в тепловій рівновазі з тілом Б, а тіло Б – з тілом В. Що можна сказати про температури тіл А і В?
3. Мідний кубик А має температуру 200 °С, такі ж мідні кубики В і С мають температуру 0 °С. Шляхом теплообміну між ними треба охолодити кубик А до температури 50 °С і нагріти за рахунок цього кубики В і С до температури 75 °С. Чи можливо це? Теплообміном між кубиками і повітрям можна знехтувати.
Розв’язок
Так, можливо. При контакті кубиків А і В, ми зможемо вирівняти їх температури. Отримаємо:
А – 100 °С, В – 100 °С, С – 0 °С.
Вчинивши аналогічно з кубиками А і С, маємо:
А – 50 °С, В – 100 °С, С – 50 °С.
Нарешті, виробляючи теплообмін між кубиками В і С, остаточно отримаємо:
А – 50 °С, В – 75 °С, С – 75 °С.
4. Визначте температуру газу, якщо середня кінетична енергія теплового руху його молекул 8,1-10-21 Дж.
2). Контрольні запитання
1. Чому не завжди можна довіряти визначенням температури на дотик?
2. Для вимірювання температури медичним термометром необхідно не менше 3-5 хв. Чому?
3. Які властивості тіл використовуються в термометрі?
4. Чи існує в природі як завгодно низька і як завгодно висока температура тіл? Чому?
Що ми дізнались на уроці
– Термодинамічна система – сукупність макроскопічних систем, які можуть обмінюватися енергією між собою та з зовнішніми тілами.
– Термодинамічна система, яка не бере участі у теплообміні з оточуючими тілами, називають теплоізольованою.
– Температура характеризує стан теплової рівноваги: всі тіла, що знаходяться в тепловій рівновазі, мають однакову температуру.
– Абсолютна температура є мірою середньої кінетичної енергії руху молекул:
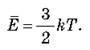
Домашнє завдання
1. Конспект.
2. Розв’язування задач:
1). На якій підставі можна припускати існування зв’язку між температурою і кінетичною енергією молекул?
2). За якої температури середня кінетична енергія поступального руху молекул газу дорівнює 6,21-10-21 Дж?
3). На скільки відсотків збільшується середня кінетична енергія молекул газу під час збільшення його температури від 7 до 35 °С?
4). Знайдіть температуру газу, коли тиск – 100 кПа і концентрація молекул – 1025 м-3.