Визначення валентності за формулами хімічних сполук
Хімія підготовка до ЗНО та ДПА
Комплексне видання
ЧАСТИНА І
ЗАГАЛЬНА ХІМІЯ
ОСНОВНІ ЗАКОНИ Й ПОНЯТТЯ ХІМІЇ
Визначення валентності за формулами хімічних сполук
Знаючи валентність одного хімічного елемента, можна визначити валентність інших атомів у сполуці. Якщо атоми Гідрогену завжди одновалентні, то в молекулі хлороводню НСl валентність атомів Хлору також дорівнює одиниці, тому що атом Хлору зв’язаний тільки з атомом Гідрогену й не може утворювати з ним більше одного зв’язку. У молекулі амоніаку NH3 атом Нітрогену
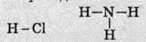
Для позначення валентності використовують римські цифри й записують їх над символом відповідного елемента в хімічній формулі:
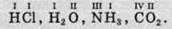
Для визначення валентності елементів не обов’язково складати структурні формули. Зверніть увагу на те, що сумарне число зв’язків атомів одного елемента завжди дорівнює сумарному числу зв’язків усіх атомів іншого елемента,
Загальне число одиниць валентності всіх атомів одного елемента в сполуці дорівнює загальному числу одиниць валентностей усіх атомів іншого елемента.
На підставі цього можна визначати валентності елементів у будь-якій сполуці, яка складається з двох хімічних елементів (ці сполуки називають бінарними). Для цього можна використати такий алгоритм:
1. Указуємо валентність елемента з постійною валентністю.
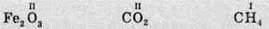
2. Множимо число атомів цього елемента на його валентність.
3 ∙ II = 6 2 ∙ II = 4 4 ∙ I = 4
3. Ділимо отримане значення на число атомів іншого елемента.
6 : 2 = III 4 : 1 = IV 4 : 1 = IV
4. Записуємо значення валентності над символом цього елемента.
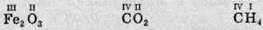
Як ми вже згадували, деякі елементи в сполуках проявляють постійну валентність, тобто, незалежно від сполуки, у цих елементів може бути тільки одне значення валентності. Ці елементи та їхню валентність треба запам’ятати. Інші елементи можуть проявляти різні валентності, залежно від різних умов.
Для більшості хімічних елементів, особливо для елементів зі змінною валентністю, можна визначити вищу (максимальну) валентність за Періодичною системою. Вища валентність хімічного елемента в переважній більшості випадків дорівнює номеру групи Періодичної системи, в якій перебуває цей елемент. За допомогою Періодичної системи можна також визначити й можливі валентності для хімічних елементів: для цього треба від вищої валентності відняти 2.
Визначення валентності за Періодичною системою1*
Група ПС | I | II | III | IV | V | VI | VII |
Вища валентність | І | II | III | IV | V | VI | VII |
Можливі валентності | II | III | II, IV | І, III, V |
Наведений принцип не є законом, тобто він не проявляється в абсолютно всіх випадках. Наприклад, Оксиген, що перебуває в VI групі, проявляє тільки валентність II, а для Феруму (VIII група) характерні валентності II та III. Однак для більшості елементів, з якими ви зустрічаєтесь у шкільному курсі, він справедливий. Докладніше визначення валентності для кожного елемента описано в другій частині цього посібника.
__________________________________________________
1* Для короткого варіанта Періодичної системи. При використанні довгого варіанта від номера групи треба додатково відняти 10.