ЯК ВИВЧАЮТЬ ЖИТТЯ НА МОЛЕКУЛЯРНОМУ РІВНІ
Розділ 2 Молекулярний рівень організації живої природи
Тема. 3 Елементний склад біологічних систем
§ 10. ЯК ВИВЧАЮТЬ ЖИТТЯ НА МОЛЕКУЛЯРНОМУ РІВНІ
Терміни та поняття: проба, об’ємно-ваговий аналіз, титрування, оптичні методи (спектральний і люмінесцентний аналізи, хроматографія), електрофорез, ультрацентрифугування, радіоактивне мічення, ізотопи, математичний аналіз, моделювання.
Матеріал для біохімічних досліджень. Зазвичай біохімічні дослідження проводять на спеціально дібраному матеріалі, який отримують від тварин, рослин,
Одним з надійних фіксаторів є етиловий спирт. (З курсу хімії пригадайте його формулу, властивості.) Саме спирт використовують для тривалого зберігання проб і подальшого дослідження структури ДНК.
Виділення необхідних речовин. Найважливішою біохімічною процедурою є виділення потрібної для аналізу речовини. Цей процес дуже кропіткий, оскільки в будь-якій клітині, тканині або органі одночасно містяться сотні й тисячі різних сполук. Багато в чому розвиток біохімічних досліджень пов’язаний саме з розробкою методик виділення з біологічних об’єктів речовин та їх очищення. Для того щоб процес виділення був ефективнішим, використовують ті види організмів або частини тіла, у яких концентрація досліджуваної речовини максимальна. (Пригадайте, звідки вперше була виділена сахароза, а звідки – глюкоза й фруктоза.) Виділення певних речовин грунтується на особливостях їх фізичних або хімічних властивостей – відмінності в молекулярній масі, формах, розмірах і зарядах молекул, розчинності у воді й інших розчинниках, специфічні реакції з певними речовинами таін. Найпоширенішими методами розділення сумішей речовин, що використовують у біохімії, є випарювання, фільтрація, діаліз (від грец. діалізіс – розкладання, відділення), який заснований на здатності речовин дифундувати через спеціальну напівпроникну мембрану, перегонка – випарювання рідини при заданій температурі з наступною конденсацією, екстракція й кристалізація. (Пригадайте, як поводяться насичені розчини солей.)
Методи дослідження в біохімії. Основне завдання, що постає перед біохіміками, – визначення присутності конкретної речовини у пробі й оцінка її кількості. У випадку, якщо виявлена речовина раніше не була відома науці, то встановлюють її формулу, просторову структуру, хімічні та фізичні властивості, функції в організмі. Для того щоб розв’язати ці завдання, вчені мають у своєму розпорядженні арсенал прийомів, які представляють собою сукупність спеціально розроблених методів та методик.
Об’ємно-ваговий аналіз заснований на кількісному визначенні обсягу або маси виділених речовин. Якщо аналізують рідку речовину або розчин солей, то кількісна оцінка речовини проводиться шляхом титрування (від фр. титр – характеристика). Наприклад, у лужний розчин спочатку додають індикатор фенолфталеїн до появи малинового забарвлення, а потім спеціальними піпетками – краплями кислоту. В момент нейтралізації, коли зникає забарвлення, фіксують кількість витраченої кислоти, що і є кількісним показником аналізованої речовини.
Кількісне визначення сухої речовини проводиться шляхом зважування, для цього можуть використовуватися ваги з різним рівнем роздільної здатності від 1 г до 1 мг. Наприклад, перед дослідником поставлено завдання: визначити масу нерозчинної у воді речовини, що містять ся у пробі молока. Для цього молоко фільтрують, отриманий осад промивають, рідину випарюють, а отриману речовину сушать або прожарюють до сталої маси. Потім суху речовину зважують.
Оптичні методи. Це найбільш чутливі з біохімічних методів, які дозволяють визначити вміст речовини у пробі в концентрації менше тисячної мг. Крім того, ці методи мають високу специфічність і точність. Оптичні методи засновані на властивостях хімічних сполук забарвлювати розчин і таким чином робити його непрозорим. У результаті залежно від концентрації барвника змінюється інтенсивність поглинання світлової енергії, що фіксується спеціальними приладами. Розрізняють кілька груп оптичних методів.
Спектральний аналіз дозволяє визначити склад молекул і атомів у пробах на підставі визначення спектрів поглинання й випромінювання світлової енергії. Зви – чайно за допомогою цього методу у пробах визначають склад хімічних елементів.
Люмінесцентний аналіз має особливо високу чутливість. Він грунтується на явищі люмінесценції – світінні речовини, що виникає після поглинання нею енергії збудження. На досліджуваний біологічний об’єкт діють ультрафіолетовим світлом і за кольором люмінесценції визначають присутність певної речовини.
Інші методи. Хроматографія (від грец. хрома – колір і графія – письмо) – метод розділення й аналізу сумішей речовин, заснований на розподілі їх компонентів між двома фазами – не рухливою, що виконує роль сита, яке з різною швидкістю пропускає молекули залежно від їх фізичних та хімічних властивостей, і рухливою, що протікає через не рухливу. В результаті суміші речовини поділяються на групи – фракції, наприклад на прості та складні білки.
Електрофорез (від лат. електро і грец. форез – переносити). Оскільки макромолекули різняться між собою зарядом, то в електричному полі вони рухаються з різною швидкістю (мал. 82). Якщо, наприклад, підготовлену пробу крові помістити на спеціальний папір, просочений сольовим розчином – буфером, який має стале значення рН, а потім до одного боку паперу підвести анод, а до іншого – катод, то білки крові з різною швидкістю почнуть мігрувати від катода до анода. Якщо через якийсь час струм вимкнути, а папір пофарбувати спеціальним барвником, то можна виявити групи білків, що різняться зарядом, які відповідно мають різну електрофоретичну рухливість. У сучасній біохімії для електрофорезу застосовують спеціальні гелі – желеподобні речовини, що мають мікропори, через які білки, що рухаються в електричному полі, або молекули нуклеїнових кислот ніби фільтруються.
У біохімії білків і нуклеїнових кислот незамінним є метод ультрацентрифугування. Метод заснований на тому, що окремі частини молекули ДНК відрізняються за розмірами і масою, а тому будуть із різною швидкістю осідати в розчині під впливом відцентрової сили. Причому більші за розмірами молекули розташовуватимуться на периферії, а з меншою питомою вагою – ближче до осі обертання. Ультрацентрифугування проводиться у спеціальних центрифугах, що здійснюють до 50 тис. обертів за хвилину. В результаті під час тривалого центрифугування проб, поміщених у дуже міцні пробірки, вдається не просто розділити фракції ДНК, але й виділити їх у достатній кількості.
Дуже популярним у біохімії є метод радіоактивного мічення. Для цього використовують ся радіоактивні ізотопи (від грец. ізос – однаковий і топос – місце). (Вам уже відомо, що ізотопи – це атоми одного хімічного елемента, які відрізняються числом нейтронів.) Один з основних елементів живого Карбон існує в природі у вигляді кількох ізотопів, серед яких радіоактивним є поширений у довкіллі ізотоп 14С. Якщо у склянку з водою, де утримуються одноклітинні водорості, додати небагато карбонатної кислоти з 14С, а потім поставити її на сонце, то через деякий час завдяки фотосинтезу частина СО2, що утворюється при розкладанні цієї кислоти, виявиться включеною до складу клітини. Профільтрувавши вміст склянки і провівши вимір радіоактивності фільтра, у якому затрималися водорості, можна визначити швидкість накопичення Карбону, що і буде відповідати інтенсивності фотосинтезу та метаболізму водоростей. Розглянутий метод дослідження дістав назву радіокарбонового аналізу.
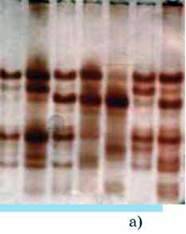
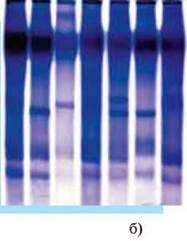
Мал. 82.Електрофореграми білків: а – ферменту неспецифічних естераз дощових червів; б – транспортних білків крові – трансферинів карася. Кожний трек відповідає окремій особині
Подібні дослідження можна проводити і з тваринами, й навіть з окремими клітинами.
Ви, напевно, чули про радіокарбоновий аналіз, за допомогою якого можна визначити вік будь-яких викопних решток. Виявляється, в живому організмі 14C перебуває в рівновазі з навколишнім середовищем і його концентрація залишається сталою. Після загибелі вміст 14C починає повільно зменшуватися (період напіврозпаду становить 5,7 тис. років). Таким чином, за зменшенням концентрації цього ізотопу можна чітко визначити, скільки минуло часу з моменту загибелі організму.
Математичний аналіз даних. Отримані результати вимірювань називають первинними даними. Їх спочатку заносять у лабораторний журнал, а вже потім формують електронну базу даних і піддають математичній обробці, яка дозволяє визначити надійність і вірогідність отриманих результатів за допомогою алгоритмів. При цьому зазвичай обчислюється середнє значення, наприклад, вмісту жирів у молоці, отримане в серії дослідів, і статистична помилка цього середнього значення. Якщо помилка незначна, то можна стверджувати, що отримані результати вірогідні, а не є наслідком випадкових збігів. За допомогою алгоритмів біометрії (пригадайте, що це за наука) можна проводити й більш складні розрахунки – визначати вірогідність тенденцій або швидкості зміни різних процесів. Для цього проводиться моделювання з подальшим зіставленням отриманої моделі з реально існуючим об’єктом чи процесом, що дозволяє з тим або іншим рівнем імовірності затверджувати вірогідність відмінностей у результатах спостережуваних і очікуваних процесів, які відбуваються в організмі.
Результати узагальнюються у вигляді таблиць, графіків і діаграм – спеціальних графічних зображень, що унаочнюють числові співвідношення. Для цього використовують відповідні комп’ютерні програми.
Сучасна біохімія – це наука, розвиток якої тісно пов’язаний з розробкою методів виявлення, кількісного аналізу й виділення різних речовин, що містяться в організмі або утворюються в результаті життєдіяльності. У створенні цих методів використовуються не тільки досягнення хімії та фізики, але й математичні алгоритми й інформаційні технології.