ЗАКОН ЗБЕРЕЖЕННЯ МАСИ РЕЧОВИН ПІД ЧАС ХІМІЧНИХ РЕАКЦІЙ
№ 1. Помилка попередників М. В. Ломоносова щодо прожарювання речовин полягала в тому, що перед проведенням дослідів реторту (з уміщеним у неї свинцем) зважували і запаювали. По завершенні дослідів реторту відкривали і повторювали зважування, виявляли збільшення маси. Про те, що у реторті, крім металу, було повітря, а в ньому кисень, який вступав у хімічну реакцію з металом, вчені не могли знати. А у відкриту репорту (замість кисню) надходила нова порція повітря.
№ 2. М. В. Ломоносов вніс зміни у проведення дослідів з прожарювання речовин та змінив
№ 3. М. В. Ломоносов у 1748 році відкрив закон збереження маси речовин.
Маса речовин, що вступають у хімічну реакцію, дорівнює масі речовин, що утворюються внаслідок реакції,
№ 4. Маса запаяної реторти після прожарювання в ній металу залишилась незмінною
№ 5. Не суперечить закону збереження маси речовин тому, що при горінні багаття відділюється вуглекислий газ і вода, яка випаровувається.
№ 6. Маса мідної пластинки після прожарювання у полум’ї спиртівки збільшиться, тому що мідь вступить у взаємодію з киснем повітря.
№ 9.
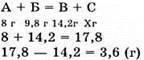
Відповідь: 3,6 г.
Related posts:
- ЗАКОН ЗБЕРЕЖЕННЯ МАСИ РЕЧОВИН ПІД ЧАС ХІМІЧНИХ РЕАКЦІЙ Тема 2 КИСЕНЬ & 23. ЗАКОН ЗБЕРЕЖЕННЯ МАСИ РЕЧОВИН ПІД ЧАС ХІМІЧНИХ РЕАКЦІЙ Вивчення параграфа допоможе вам: · пізнати сутність одного з основних законів хімії – закону збереження маси речовин; · пояснювати сутність закону збереження маси речовин Ви вже знаєте, що хімічні явища супроводжуються утворенням нових речовин. Відбувається це з атомів тих самих елементів, що […]...
- Рівняння хімічних реакцій. Закон збереження маси речовин у хімічних реакціях Контрольні запитання № 1. Маси речовин, що вступають у реакцію, дорівнюють масі утворених речовин, про що свідчить закон збереження маси в хімічних реакціях. Цей закон підкріплений тим, що атоми в хімічних реакціях не зникають, а просто переходять з одних речовин до складу інших. За допомогою хімічних символів і знаків закон збереження маси відображають рівнянням хімічної […]...
- Закон збереження маси речовин. Хімічні рівняння Тема 2 Кисень & 16. Закон збереження маси речовин. Хімічні рівняння Опанувавши цю тему, ви зможете: – знати, які знання називають законом; – розрізняти схему реакції та хімічне рівняння; – розуміти поняття “хімічне рівняння”; – формулювати закон збереження маси речовин; – пояснювати сутність закону збереження маси речовин і рівнянь реакцій; – уміти складати рівняння хімічних […]...
- ЗАКОН ЗБЕРЕЖЕННЯ МАСИ Хімія – універсальний довідник КІЛЬКІСНІ ВІДНОШЕННЯ В ХІМІЇ ЗАКОН ЗБЕРЕЖЕННЯ МАСИ Рівняння хімічної реакції – це, фактично, рівняння матеріального балансу речовин, що вступили в реакцію, і продуктів реакції, тобто рівність їхніх мас. Дійсно, число атомів кожного елемента зліва і справа в рівнянні реакції те ж саме, адже атоми в хімічних реакціях не виникають і не […]...
- Атомно-молекулярне вчення. Закони збереження маси речовин, сталості складу речовин – Хімічна реакція ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 4. Хімічна реакція 4.2. Атомно-молекулярне вчення. Закони збереження маси речовин, сталості складу речовин Атомно-молекулярне вчення – це сукупність аксіом і законів, що розглядають речовину, яка складається з атомів. Ось основні його положення: – усі речовини складаються з атомів. Молекули простих речовин складаються з […]...
- Схема хімічної реакції. Закон збереження маси речовин під час хімічної реакції. Хімічне рівняння Розділ 2 Кисень 19 Схема хімічної реакції. Закон збереження маси речовин під час хімічної реакції. Хімічне рівняння Матеріал параграфа допоможе вам: > з’ясувати, що таке схема хімічної реакції; > зрозуміти суть закону збереження маси речовин під час хімічної реакції; > навчитися перетворювати схеми реакцій на хімічні рівняння. Схема хімічної реакції. Існує кілька способів запису хімічних […]...
- Закон як форма наукових знань. Закон збереження маси Тема 1 ПОЧАТКОВІ ХІМІЧНІ ПОНЯТТЯ Урок 21 Тема. Закон як форма наукових знань. Закон збереження маси Цілі: пояснити закон збереження маси речовини як один з основних законів; показати роль учених-хіміків А. Лавуазьє, М. В. Ломоносова у відкритті цього закону; пояснити значення закону збереження маси речовини в хімії як однієї з форм наукових знань про природу; […]...
- Закон збереження маси речовини ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 1. ОСНОВНІ ПОНЯТТЯ І ЗАКОНИ ХІМІЇ § 1.9. Закон збереження маси речовини Розглянемо в світлі атомно-молекулярного вчення основні закони хімії: збереження маси речовини, сталості складу, об’ємних відношень і закон Авогадро. Ці закони підтверджують атомно-молекулярне вчення – основу нової хімії. У свою […]...
- Закон збереження речовин. Хімічні рівняння ТЕМА 1. ПОЧАТКОВІ ХІМІЧНІ ПОНЯТТЯ Урок 17. Закон збереження речовин. Хімічні рівняння Цілі: пояснити та сформулювати закон збереження маси речовин; дати поняття про рівняння хімічних реакції, коефіцієнт, реагент, продукт реакції; на основі закону збереження маси речовин сформувати вміння складати рівняння хімічних реакцій, добирати коефіцієнти. Обладнання та реактиви: терези з різновагами, пробірки, розчини барій хлориду й […]...
- Тема 2. Закон збереження маси. Кількість речовини – ОСНОВНІ ПОНЯТТЯ, ЗАКОНИ І ЗАКОНОМІРНОСТІ В ХІМІЇ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА ІІ ЗАВДАННЯ ДЛЯ ПЕРЕВІРКИ ЗНАНЬ ОСНОВНІ ПОНЯТТЯ, ЗАКОНИ І ЗАКОНОМІРНОСТІ В ХІМІЇ Тема 2. Закон збереження маси. Кількість речовини Серед чотирьох наведених варіантів відповідей виберіть одну правильну 1. Позначте прізвище вченого, ім’ям якого названо число частинок, що міститься в 1 моль будь-якої речовини: A. Менделєєв; Б. […]...
- Розрахунки за рівняннями хімічних реакцій між розчином солі та металом РОЗДІЛ 3 МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХ СПОЛУКИ § 53. Розрахунки за рівняннями хімічних реакцій між розчином солі та металом Усвідомлення змісту цього параграфа дає змогу: Пояснювати суть і причини зміни маси пластинки в зазначених реакціях; Розв’язувати задачі “на пластинку”. Задачі такого типу засновані на закономірностях витискувального ряду металів. Як ви уже знаєте, показником порівняльної хімічної […]...
- § 11. МАСА АТОМА. АТОМНА ОДИНИЦЯ МАСИ, ВІДНОСНІ АТОМНІ МАСИ ХІМІЧНИХ ЕЛЕМЕНТІВ № 1. Атомна одиниця маси (а. о. м.) – маса 1/12 частини атома Карбону, ядро якого складається з 6 протонів і 6 нейтронів. № 2, 3. Число, яке одержують діленням маси атома конкретного хімічного елемента на атомну одиницю маси (приблизно на 1,662 • 10-27 кг) має назву відносна атомна маса хімічного елемента й позначається Аr. […]...
- Ентропія реакції – Рушійна сила хімічних реакцій ЕНЕРГЕТИКА ХІМІЧНИХ РЕАКЦІЙ 3. Рушійна сила хімічних реакцій 3.3. Ентропія реакції У кожній реакції впорядкований стан системи змінюється і, отже, змінюється ентропія. Зміна ентропії реакції ∆SR, як і ентальпії реакції, визначається як різниця суми ентропій продуктів реакції і суми ентропій початкових речовин: Приклад. Під час реакції газоподібного гідроген хлориду з газоподібним амоніаком з двох “невпорядкованих” […]...
- МАСА АТОМА. АТОМНА ОДИНИЦЯ МАСИ. ВІДНОСНІ АТОМНІ МАСИ ХІМІЧНИХ ЕЛЕМЕНТІВ Тема 1 ПОЧАТКОВІ ХІМІЧНІ ПОНЯТТЯ & 11. МАСА АТОМА. АТОМНА ОДИНИЦЯ МАСИ. ВІДНОСНІ АТОМНІ МАСИ ХІМІЧНИХ ЕЛЕМЕНТІВ Вивчення параграфа допоможе вам: · розрізняти поняття “маса атома”, “атомна одиниця маси”, “відносна атомна маса хімічного елемента”; · порівнювати масу атомів. МАСА АТОМА. Як ваді відомо з попереднього параграфи, атоми мають вражаюче малі розміри. Відповідно й маса атомів […]...
- СХЕМА ХІМІЧНОЇ РЕАКЦІЇ. РІВНЯННЯ ХІМІЧНИХ РЕАКЦІЙ Тема 2 КИСЕНЬ & 24. СХЕМА ХІМІЧНОЇ РЕАКЦІЇ. РІВНЯННЯ ХІМІЧНИХ РЕАКЦІЙ Вивчення параграфа допоможе вам: · пояснювати суть рівнянь хімічних реакцій; · розрізняти схему і рівняння хімічної реакції, коефіцієнти й індекси; · у рівняннях хімічних реакцій розрізняти реагенти і продукти реакцій; · писати рівняння хімічних реакцій з дотриманням закону збереження маси речовин До цього часу […]...
- Ентропія простих речовин і сполук – Рушійна сила хімічних реакцій ЕНЕРГЕТИКА ХІМІЧНИХ РЕАКЦІЙ 3. Рушійна сила хімічних реакцій 3.2 . Ентропія простих речовин і сполук Прийнято вважати, що атоми елементів і сполук при абсолютному нулі (тобто при 0 К або -273,16 °С) знаходяться в абсолютно впорядкованому стані. Ентропія речовин при абсолютному нулі становить S = 0 Дж/(моль ∙ К). При підвищенні температури порядок у структурі […]...
- СХЕМА ХІМІЧНОЇ РЕАКЦІЇ. РІВНЯННЯ ХІМІЧНИХ РЕАКЦІЙ № 1. Хімічне рівняння – це умовний запис хімічної реакції (хімічного явища) за допомогою хімічних формул, коефіцієнтів і знаків “+” “-” та “=”. Знак “=” вказує на те, що кількість атомів кожного хімічного елемента у лівій та правій частині хімічного рівняння однакова. № 2. Рівняння хімічної реакції відрізняється від її схеми тим, що у рівнянні […]...
- Швидкість хімічних реакцій ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 4. ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ. § 4.1. Швидкість хімічних реакцій Суть хімічних реакцій зводиться до розриву зв’язків у вихідних речовинах і виникнення нових зв’язків у продуктах реакції. При цьому загальне число атомів кожного елемента до і після реакції залишається сталим. Оскільки утворення […]...
- РЕАКЦІЇ СПОЛУЧЕННЯ – ТИПИ ХІМІЧНИХ РЕАКЦІЙ Хімія – універсальний довідник ТИПИ ХІМІЧНИХ РЕАКЦІЙ РЕАКЦІЇ СПОЛУЧЕННЯ Уже сама назва “реакція сполучення” говорить про її тип. У результаті сполучення декількох речовин утворюється одна нова речовина. Практично завжди в реакцію сполучення вступає не більше двох речовин; ці речовини можуть бути як простими, так і складними. Приклади реакцій сполучення: У переважній більшості реакції сполучення є […]...
- Енергетичний ефект хімічних реакцій Хімія Загальна хімія Хімічні реакції Енергетичний ефект хімічних реакцій Хімічні реакції завжди супроводжуються виділенням або поглинанням енергії. Кількість виділеної або поглиненої енергії називається тепловим ефектом хімічної реакції (Q). Реакції, що супроводжуються виділенням енергії, називаються екзотермічнимИ, поглинанням енергії, – ендотермічнимИ. Хімічні рівняння, в яких наводяться теплові ефекти хімічних реакцій, називаються ТермохімічнимИ, наприклад: У цьому рівнянні зазначені […]...
- Вільна енергія реакції Гіббса – Рушійна сила хімічних реакцій ЕНЕРГЕТИКА ХІМІЧНИХ РЕАКЦІЙ 3. Рушійна сила хімічних реакцій 3.4. Вільна енергія реакції Гіббса Кожна реакція характеризується двома тенденціями: – система речовин прагне перейти у стан з якомога меншою ентальпією; – система речовин прагне перейти в стан з якомога більшою ентропією. Тому реакція Проходить самочинно в той бік, де знижується ентальпія реакції і зростає її ентропія. […]...
- РЕАКЦІЇ РОЗКЛАДУ – ТИПИ ХІМІЧНИХ РЕАКЦІЙ Хімія – універсальний довідник ТИПИ ХІМІЧНИХ РЕАКЦІЙ РЕАКЦІЇ РОЗКЛАДУ З назви “реакція розкладу” також випливає, про який тип реакцій іде мова. У реакції розкладу відбувається розкладання складної речовини на декілька речовин. Продуктами реакції можуть бути як прості, так і складні речовини. Наприклад: Майже всі вказані реакції, як і переважна більшість інших реакцій розкладу, ендотермічні. Для […]...
- РЕАКЦІЇ ОБМІНУ – ТИПИ ХІМІЧНИХ РЕАКЦІЙ Хімія – універсальний довідник ТИПИ ХІМІЧНИХ РЕАКЦІЙ РЕАКЦІЇ ОБМІНУ Реакції між складними хімічними речовинами, в результаті яких відбувається обмін між ними окремими атомами або групами атомів, називаються реакціями обміну. Наприклад: Реакції обміну (крім сильно екзотермічної реакції нейтралізації) зазвичай супроводжуються невеликим тепловим ефектом, тобто відбувається лише невелика зміна внутрішньої енергії системи, і вона не може бути […]...
- Типи хімічних реакцій – Хімічна реакція ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 4. Хімічна реакція 4.3. Типи хімічних реакцій Хімічні реакції класифікують за різними ознаками: – за фазовим станом середовища; – за типом перетворення реагентів; – за тепловим ефектом; – за ознакою зміни ступенів окиснення; – за оборотністю. Фазовий стан середовища Залежно від фазового стану […]...
- Класифікація хімічних реакцій – ХІМІЧНІ РЕАКЦІЇ ТА ЗАКОНОМІРНОСТІ ЇХ ПЕРЕБІГУ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЧНІ РЕАКЦІЇ ТА ЗАКОНОМІРНОСТІ ЇХ ПЕРЕБІГУ Класифікація хімічних реакцій Класифікація за числом та складом вихідних реагентів і продуктів реакції Реакція сполучення – реакція, внаслідок якої з кількох речовин з відносно простим складом утворюється одна велика речовина з більш складною структурою. А + В […]...
- ШВИДКІСТЬ ХІМІЧНОЇ РЕАКЦІЇ – ХІМІЧНА КІНЕТИКА. ШВИДКІСТЬ І МЕХАНІЗМ ХІМІЧНИХ РЕАКЦІЙ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ХІМІЧНА КІНЕТИКА. ШВИДКІСТЬ І МЕХАНІЗМ ХІМІЧНИХ РЕАКЦІЙ ШВИДКІСТЬ ХІМІЧНОЇ РЕАКЦІЇ Швидкість і механізм хімічної реакції вивчає хімічна кінетика. Швидкість хімічної реакції характеризується зміною концентрації однієї з вихідних речовин або кінцевих продуктів за одиницю часу. Середня швидкість реакції: Де с1 і с2 – початкова і кінцева концентрація речовини; τ1 і […]...
- ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ – КИСЕНЬ Хімія – універсальний довідник КИСЕНЬ ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ Швидкість реакції – це кількість речовини, що реагує за одиницю часу. Залежно від умов одна і та ж реакція може протікати з різною швидкістю. Так, при збільшенні кількості речовини, що реагує в одиниці об’єму, тобто його концентрації, швидкість реакції зростає, тому що зростає число зіткнень частинок, що […]...
- Відносні атомні маси хімічних елементів Тема 1 Початкові хімічні поняття & 7. Відносні атомні маси хімічних елементів Опанувавши цю тему, ви зможете: – розуміти кількісну характеристику атома; – розрізняти поняття “відносна атомна маса” і “маса атома”; – знати одиницю, щодо якої обчислюють відносні атомні маси елементів, а також першу класифікацію елементів на металічні й неметалічні; – уміти знаходити значення відносних […]...
- Класифікація хімічних реакцій за різними ознаками Тема 2 ХІМІЧНІ РЕАКЦІЇ Урок 21 Тема уроку. Класифікація хімічних реакцій за різними ознаками Цілі уроку: узагальнити й систематизувати знання учнів про хімічні реакції; розвивати вміння й навички визначення типів хімічних реакцій за рівняннями хімічних реакцій; формувати знання учнів про хімічні рівняння на прикладі класифікації рівнянь реакції за тепловим ефектом, наявністю каталізатора, зміною ступенів окиснення […]...
- КАТАЛІЗ – ХІМІЧНА КІНЕТИКА. ШВИДКІСТЬ І МЕХАНІЗМ ХІМІЧНИХ РЕАКЦІЙ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ХІМІЧНА КІНЕТИКА. ШВИДКІСТЬ І МЕХАНІЗМ ХІМІЧНИХ РЕАКЦІЙ КАТАЛІЗ Каталіз – це зміна швидкості хімічної реакції речовинами (каталізаторами), які беруть участь у реакції, але не входять до складу кінцевих продуктів. За участю каталізатора хімічна рівновага системи досягається швидше, ніж без нього. Вплив у каталізатора на швидкість реакції досягають за рахунок […]...