Застосування електролізу
1-й семестр
ЕЛЕКТРОМАГНІТНІ ЯВИЩА
2. Електричний струм
Урок 26/32
Тема. Застосування електролізу
Мета уроку: ознайомити учнів з технічним застосуванням електролізу; навчити їх застосовувати закон електролізу Фарадея під час розв’язання задач.
Тип уроку: урок вивчення нового матеріалу.
План уроку
Контроль знань | 5 хв. | 1. Рухом яких заряджених частинок створюється струм у рідинах? 2. У чому полягає відмінність провідності електролітів від провідності 3. Сформулюйте закон електролізу. 4. Який фізичний зміст має електрохімічний еквівалент? |
Демонстрації | 5 хв. | Фрагменти відеофільму “Електроліз і його промислове застосування”. |
Вивчення нового матеріалу | 25 хв. | 1. Застосування електролізу для одержання чистих металів. 2. Знайомимося з гальваностегією. 3. Вивчаємо гальванопластику |
Закріплення вивченого матеріалу | 10 хв. | 1. Контрольні питання. 2. Навчаємося розв’язувати задачі |
ВИВЧЕННЯ НОВОГО МАТЕРІАЛУ
1. Застосування
Електролітичні процеси класифікуються в такий спосіб:
– одержання неорганічних речовин (водню, кисню, хлору, лугів тощо);
– одержання металів (літій, натрій, калій, берилій, магній, цинк, алюміній, мідь тощо);
– очищення металів (мідь, срібло тощо);
– одержання металевих сплавів;
– одержання гальванічних покриттів;
– одержання органічних речовин;
– нанесення плівок за допомогою електрофорезу.
Актуальність електролізу пояснюється тим, що багато речовин одержують саме в такий спосіб. Наприклад, такі метали, як нікель, натрій, чистий водень та інші, одержують тільки цим методом.
У промисловості алюміній і мідь у більшості випадків одержують саме шляхом електролізу. Перевага цього способу у відносній дешевизні й простоті.
2. Знайомимося з гальваностегією
Гальванотехніка – галузь прикладної електрохімії, що займається процесами нанесення металевих покриттів на поверхню як металевих, так і неметалевих виробів при проходженні постійного електричного струму через розчини їхніх солей.
Гальванотехніка ділиться на гальваностегію та гальванопластику.
За допомогою електролізу можна покрити металеві предмети шаром іншого металу. Цей процес називається гальваностегією.
Особливе технічне значення мають покриття важко-окисними металами, зокрема нікелювання й хромування, а також сріблення й золочення, що часто застосовуються для захисту металів від корозії. Для одержання потрібних покриттів предмет ретельно очищають, добре знежирюють і поміщають як катод в електролітичну ванну, що містить сіль того металу, яким бажають покрити предмет. Для більш рівномірного покриття корисно застосовувати як анод дві пластини, поміщаючи предмет між ними.
На рисунку показані алмазні диски, виготовлені методом гальваностегії.

Фігурки з олова, покриті міддю:

3. Вивчаємо гальванопластику
За допомогою електролізу можна не тільки покрити предмети шаром того чи іншого металу, але й виготовити їхні рельєфні металеві копії (наприклад, монет, медалей). Цей процес був винайдений російським фізиком й електротехніком, членом Російської Академії наук Борисом Семеновичем Якобі (1801 -1874) у 40-х роках XIX століття, і називається він гальванопластикою. Для виготовлення рельєфної копії предмета спочатку роблять зліпок з якого-небудь пластичного матеріалу, наприклад, з воску. Цей зліпок натирають графітом і занурюють в електролітичну ванну як катод, де на ньому й осаджується шар металу. Такий метод застосовується в поліграфії під час виготовлення друкованих форм.
На рисунку показано кілька рельєфних копій, отриманих за допомогою гальванопластики.

Питання до учнів у ході викладу нового матеріалу
– Які особливості проходження електричного струму в рідинах можна використовувати для одержання чистих металів?
– Як можна захистити метали від корозії?
– Наведіть приклади металів, які можна одержувати електролітичним способом.
– У який спосіб можна покривати різні вироби шаром дорогоцінного металу?
ЗАКРІПЛЕННЯ ВИВЧЕНОГО МАТЕРІАЛУ
1). Якісні питання
1. Чи можуть під час дисоціації утворитися іони якого-небудь одного знака? Чому?
2. Чому не можна доторкатися до неізольованих електричних проводів голими руками?
3. Для чого під час нікелювання як анод ставлять нікелеву пластинку? Чи буде відкладатися нікель з розчину нікелевої солі, якщо нікель на аноді замінити яким-небудь іншим металом?
4. Чому для гальванічного покриття виробу найчастіше вживають нікель і хром?
2). Навчаємося розв’язувати задачі
1. За допомогою електролізу зробили нікелювання пластинки площею 200 см2. Електроліз робили за сили струму 2 А. Товщина шару нікелю 0,02 мм. Протягом якого часу відбувався електроліз? Електрохімічний еквівалент нікелю 3-10-7 кг/Кл, його густина 8900 кг/м3.
Розв’язок. Масу шару нікелю, отриманого за час t, одержимо із закону електролізу: m = kІt. З іншого боку, цю саму масу можна виразити через площу пластинки і товщину шару нікелю: m = ?Sh. Прирівнявши обидва вирази для маси, одержуємо: 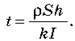 Перевіривши одиниці величин і підставивши числові значення, одержуємо t = 5900 c? 1 год. 40 хв.
Перевіривши одиниці величин і підставивши числові значення, одержуємо t = 5900 c? 1 год. 40 хв.
2. За допомогою електролізу, що відбувався за напруги 5 В, одержали 4 кг алюмінію. Який час світили б 5 енергозберігаючих ламп потужністю по 18 Вт за рахунок цієї енергії? Електрохімічний еквівалент алюмінію дорівнює 0,93-10-7 кг/Кл.
Розв’язок. Відповідно до закону збереження енергії витрати електроенергії дорівнюють роботі електричного струму при електролізі: A = UIt. Скористаємося також законом електролізу: m = kІt. Розділивши перший вираз на другий, одержуємо 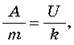 звідки
звідки 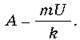 Оскільки A = 5Pt, де P – потужність кожної з ламп, одержуємо час світіння ламп:
Оскільки A = 5Pt, де P – потужність кожної з ламп, одержуємо час світіння ламп:
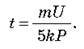
Перевіривши одиниці величин і підставивши числові значення, одержуємо: t = 2,4-106 с, тобто близько 670 годин. Таким чином, лампи могли б світити день і ніч майже 28 діб.
3. За сили струму 5 А за 10 хв. в електролітичній ванні виділився цинк масою 1,017 г. Визначте електрохімічний еквівалент цинку.
4. Під час електролізу розчину мідного купоросу за 1 год. виділилася мідь масою 500 г. Визначте силу струму в колі. Електрохімічний еквівалент міді дорівнює 3,29-10-7 кг/Кл.
Що ми дізналися на уроці
– Гальванотехніка – галузь прикладної електрохімії, що займається процесами нанесення металевих покриттів на поверхню як металевих, так і неметалевих виробів при проходженні постійного електричного струму через розчини їхніх солей.
– Гальваностегією називається процес покриття металевих предметів шаром іншого металу за допомогою електролізу.
– Гальванопластикою називають процес виготовлення рельєфних металевих копій за допомогою електролізу.
Домашнє завдання
1. Підр.: § 20.
2. Зб.:
Рів1 – № 11.7; 11.8; 11.9; 11.25.
Рів2 – № 11.26; 11.27; 11.28; 11.41.
Рів3 – № 11.42, 11.43; 11.44.