Значення води і водних розчинів. Кислотні опади
Розділ 3 Вода
30 Значення води і водних розчинів. Кислотні опади
Матеріал параграфа допоможе вам:
> оцінити роль води і водних розчинів у природі;
> усвідомити значення води для людини і розвитку цивілізації;
> з’ясувати причини виникнення кислотних опадів та їхній вплив на довкілля.
Роль води і водних розчинів у природі. Без води не можна уявити нашої планети. Вода вкриває більшу частину її поверхні, створюючи одну із трьох “сфер” Землі – гідросферу, складовими якої є моря, океани, річки, озера. Гідросфера
Вода – учасник фотосинтезу в рослинах. Крім цього, вона забезпечує їх живлення.
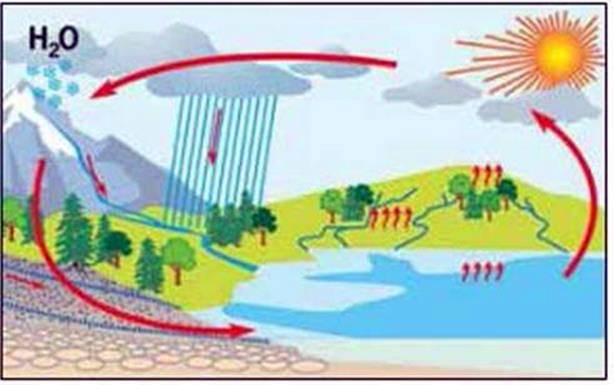
Мал. 84. Колообіг води
Природні розчини потрапляють у рослини через коріння, постачаючи їм необхідні речовини. Без
Дуже важливим для природи є те, що вода, маючи велику теплоємність, повільно охолоджується взимку й так само нагрівається влітку, внаслідок чого пом’якшує клімат.
Значення води і водних розчинів для людини. Організм людини, як і інші живі організми, існує завдяки участі води в біологічних процесах. Без неї людина може прожити не більше тижня. Втрата води призводить до погіршення функціонування різних систем організму.
Біологічні рідини в нашому організмі – це водні розчини. Найважливіші серед них – кров, лімфа, шлунковий сік, жовч, сеча. Воду в різній кількості містять майже всі харчові продукти.
Потреба людини у воді залежить від її віку, обсягу фізичних навантажень, температурних умов довкілля, вологості повітря, інших чинників. Вона задовольняється вживанням питної води (щодня – не менше 1,5-2 л), різних напоїв, страв, які містять воду, фруктів, овочів.
Людина щодоби використовує сотні літрів води в побуті. Жителі сільської місцевості споживають її менше, ніж мешканці міст (мал. 85). Норми добових витрат води людиною, яка проживає в місті, залежать від благоустрою будинків і здебільшого становлять від 200 до 400 л.
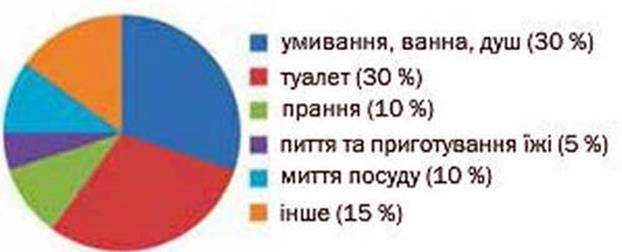
Мал. 85. Приблизний розподіл витрат води в міській квартирі
Цікаво знати
На виробництво 1 т соди витрачається до 50 т води, а 1 т синтетичного волокна – до 6000 т води.
Без води неможливе функціонування промисловості. У багатьох технологічних процесах вона слугує розчинником, теплоносієм, охолоджувачем. Великі кількості води споживає металургія, сільське господарство, енергетична галузь, підприємства легкої та харчової промисловості, побутового обслуговування, медичні та наукові установи. У виробництві мінеральних добрив, кислот, лугів, мийних засобів, лікарських препаратів широко застосовують водні розчини різних речовин.
Природна вода виконує важливу роль у вирішенні проблеми відходів. Попередньо очищені від токсичних речовин промислові і побутові стоки потрапляють у річки й моря, де вода розбавляє їх і розносить на значні відстані, мінімізуючи негативний вплив.
Отже, розвиток нашої цивілізації значною мірою зобов’язаний воді та водним розчинам.
Кислотні опади. Однією з ланок колообігу води в природі є атмосферні опади – дощ, сніг, град. Іноді вони містять домішки кислот. Такі опади називають кислотними. Розглянемо причини їх виникнення.
У газових викидах промислових підприємств, теплоелектростанцій, вихлопних газах автомобільних двигунів містяться невеликі кількості оксидів Сульфуру і Нітрогену. Сірчистий газ SО2 потрапляє в повітря під час випалювання деяких металічних руд на заводах, при спалюванні вугілля, яке містить домішки сполук Сульфуру. Внаслідок взаємодії цього газу з атмосферною вологою утворюється сульфітна кислота:
SО2 + Н2О = H2SO3.
Невелика її частина реагує з киснем і перетворюється па сульфатну кислоту:
2Н2SО3 + O2 = 2H2SO4.
Оксиди Нітрогену з’являються в атмосфері в результаті реакцій за участю головних компонентів повітря – азоту і кисню. Спочатку за дуже високої температури (під час згоряння палива і пального) відбувається реакція
N2 + О2 = 2NO.
У неї вступає дуже мала кількість обох газів. Продукт реакції – нітроген(II) оксид – швидко взаємодіє з киснем
2NO + O2 = 2NO2,
А нітроген(ІV) оксид реагує з атмосферною вологою з утворенням двох кислот – нітритної та нітратної:
2NО2 + Н2О = HNО2 + HNО3.
Усі названі кислоти разом із дощем або снігом потрапляють на земну поверхню (мал. 86). Зафіксовано випадки, коли дощові краплі були такими кислими, як оцет.
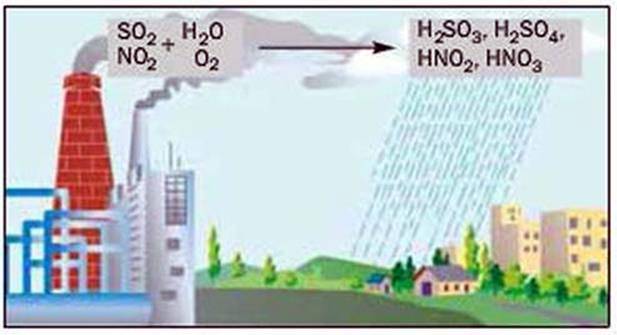
Мал. 86. Утворення кислотного дощу
Кислотні опади негативно впливають па рослини, спричиняють хвороби у тварин, людей, руйнують будівельні матеріали, особливо мармур і вапняк (мал. 87), посилюють корозію металів.
Заходи, спрямовані на зменшення викидів в атмосферу оксидів Сульфуру і Нітрогену, є одними з найважливіших у справі охорони природи. У сучасній теплоенергетиці перевагу падають паливу, що містить якомога менше домішок сполук Сульфуру. Утворенню оксидів Нітрогену запобігають, знижуючи температуру згоряння палива або пального. Серед відповідних заходів у транспортній галузі – зміна конструкцій двигунів, режимів їх роботи, введення спеціальних добавок до пального.

Мал. 87. Історична пам’ятка, пошкоджена кислотними опадами
ВИСНОВКИ
Вода відіграє дуже важливу роль у природі. Вона забезпечує колообіги хімічних елементів, регулює клімат на планеті. Без води не можуть існувати живі організми.
Воду і водні розчини широко використовують у різних галузях промисловості, інших сферах діяльності людей. Значні кількості води витрачаються на побутові потреби.
Потрапляння в повітря оксидів Сульфуру і Нітрогену разом із промисловими і транспортними викидами газів призводить до утворення кислотних опадів, які завдають шкоди довкіллю.
?
215. Назвіть найважливіші ланки колообігу води в природі.
216. Чому більшість хімічних заводів розміщено поблизу річок?
217. Надайте кілька пропозицій з економії води у побуті.
218. Перетворіть схеми реакцій, які відбуваються при випалюванні металічних руд на хімічні рівняння:
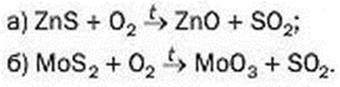
219. Виведіть формулу оксиду Нітрогену, який взаємодіє з водою з утворенням:
А) нітритної кислоти HNО2;
Б) нітратної кислоти HNО3.
220. Обчисліть масу сульфур(ІV) оксиду, що потрапить у повітря під час спалювання 1 т вугілля, в якому масова частка Сульфуру становить 6 %. Припустіть, що сполуки Сульфуру, наявні у вугіллі, повністю вступають у відповідні реакції з утворенням сульфур(ІV) оксиду.