Атомна структура електрики. Досліди Йоффе, Міллікена
ФІЗИКА
Частина 3 ЕЛЕКТРИКА І МАГНЕТИЗМ
Розділ 8 ЕЛЕКТРИКА
8.11. Атомна структура електрики. Досліди Йоффе, Міллікена
Досліди А. Ф. Йоффе, виконані 1912 р., присвячені встановленню атомної структури електрики. Негативно заряджена металева пилинка вміщувалась між пластинами конденсатора, напруженість поля якого добиралась такою, щоб пилинка перебувала в рівновазі, тобто qЕ = mg. Після цього пилинку освітлювали ультрафіолетовим світлом. Унаслідок фотоефекту негативний заряд пилинки поступово зменшувався і для збереження рівноваги
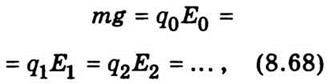
Звідки
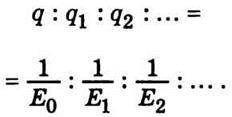
Виявилося, що заряд пилинки може набирати лише дискретних значень.
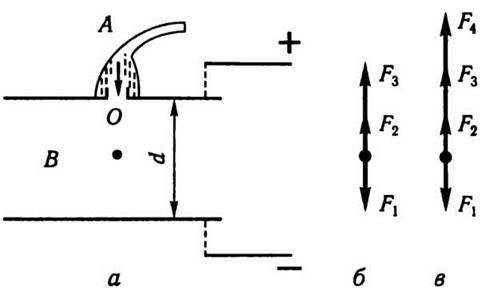
Рис. 8.7
У 1909-1914 рр. американський фізик Р. Міллікен провів досліди, на підставі яких не лише встановив атомність електрики, що доводилося дослідами Йоффе, а й визначив значення елементарного електричного заряду. Схему установки Р. Міллікена зображено на рис. 8.7, а.
Основною частиною приладу є плоский конденсатор, пластини якого під’єднуються до джерела напруги
Розглянемо спочатку випадок, коли електричного поля в конденсаторі немає. Тоді на краплину, що рухається з малою швидкістю у в’язкому середовищі, крім сили тяжіння F1 і виштовхувальної сили F2, яка визначається за законом Архімеда, діятиме сила тертя F3. У разі сферичної краплини силу тертя можна визначити за законом Стокса:

Де r – радіус краплини; υ – швидкість її руху; η – коефіцієнт в’язкості середовища. Напрям сил F1,F2,F3 зображено на рис. 8.7, б. Збільшення швидкості руху краплини и приводить до зростання сили F3, і в деякий момент часу рівнодійна сил, що діють на краплину, дорівнюватиме нулю, тобто F1 = F2 + F3. Починаючи з цього моменту часу краплина рухатиметься рівномірно. Оскільки 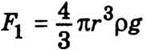 (ρ – густина масла) і
(ρ – густина масла) і 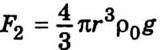 (ρ – густина середовища), то
(ρ – густина середовища), то
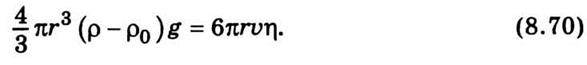
Вимірявши швидкість рівномірного падіння краплини і знаючи характеристики середовища ρ0, η та речовини краплини ρ, неважко визначити радіус краплини:

Якщо тепер між пластинами конденсатора створити поле напруженістю Е = 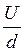 , напрямлене так, що воно сповільнює рух краплини, то на неї з боку поля діятиме додаткова сила
, напрямлене так, що воно сповільнює рух краплини, то на неї з боку поля діятиме додаткова сила
F4 (її напрям показано на рис. 8.7, в):

Де q – заряд краплини; U – різниця потенціалів на пластинах конденсатора; d – відстань між ними. Тоді у разі рівноваги сил, що діють на краплину,
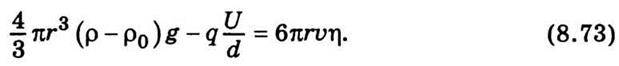
У рівнянні (8.73) всі величини або задано (η, ρ, ρ0, U, d), або визначено під час експерименту (υ1, r), тому можна визначити електричний заряд краплини:
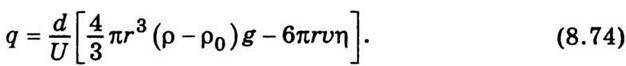
Так Р. Міллікен обчислив заряд краплин для численних випадків. Потім він знайшов довільні різниці між електричними зарядами, які несли на собі краплини масла:
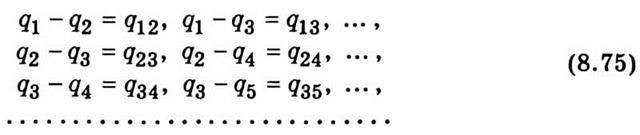
Цими розрахунками він установив, що серед усіх численних різниць між зарядами краплин не було меншої від заряду електрона, вони, були кратні заряду електрона або дорівнювали йому. Таким чином було доведено атомну структуру електрики і наявність елементарного електричного заряду, що дорівнює заряду електрона: е = 1,6 ∙ 10-19 Кл. Отже, заряд електрона є атомом електрики, а не середньостатистичною величиною. Цим також було спростовано гіпотезу про існування субелектронів – частинок, що мають заряд у десятки, сотні й навіть тисячі разів менший, ніж заряд електрона.
Тепер у зв’язку з вивченням структури елементарних частинок висловлено гіпотезу про існування так званих кварків і допускається існування електричних зарядів, менших від заряду електрона (див. підрозділ 18.8).