Електроліз розплавів – Електроліз
ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання
РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ
6. Суміші речовин. Розчини
6.13. Електроліз
Електроліз – це сукупність окисно-відновних процесів, які відбуваються на електродах під час проходження електричного струму крізь розчин або розплав електроліту. Якщо крізь розчин електроліту пропускати постійний електричний струм, то позитивно заряджені частинки (катіони) будуть рухатися до катода (негативно зарядженого електрода), тут відбуватиметься процес відновлення (приєднання
Розрізняють два типи електролізу: електроліз розплавів та електроліз розчинів.
6.13.1. Електроліз розплавів
Луги і більшість солей у розплавленому стані Складаються з іонів, які в електричному полі здатні переміщуватись подібно до гідратованих іонів, що містяться у розчинах. Під час електролізу розплавів електролітів (солей, лугів) на катоді завжди відновлюється метал.
Приклад 1. Електроліз розплаву КВr:
1. Відбувається дисоціація:
2. Іони К+ переміщуються до катода, а йони Вr – -..до. анода, де й відбуваються процеси окиснення – відновлення:
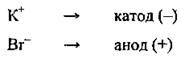
3. Записуємо відповідні електронні рівняння:
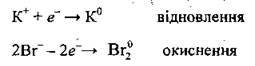
4. Установимо баланс електронів: підставимо “2” і “1” (навхрест, аналогічно схемам електронного балансу):
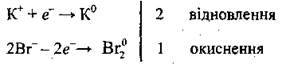
5) Для одержання сумарного рівняння електролізу:
А) коефіцієнти електронного рівняння відновлення 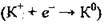 домножують на 2;
домножують на 2;
Б) до нього додають електронне рівняння окиснення (окремо ліву і праву частину):
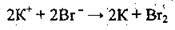
На основі цього йонно-молекулярного рівняння складаємо молекулярне рівняння:
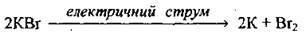
Приклад 2. Електроліз розплаву NaOH:
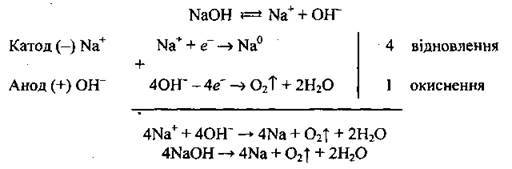
Приклад 3. Електроліз розплаву CaCl2:

Електроліз розплавів має важливе промислове значення. Саме цим методом одержують найактивніші метали: літій, натрій, кальцій та багато інших речовин (Н2, O2, Cl2, NaOH, КСlО3).
Related posts:
- Загальні способи добування металів. Електроліз розплавів солей і лугів – Метали Хімія Неорганічна хімія Метали Загальні способи добування металів. Електроліз розплавів солей і лугів Металургія – це галузь промисловості, яка займається видобуванням металів із руд. Електроліз – окисно-відновний процес, що відбувається на електродах під час проходження електричного струму через розплав або розчин електроліту. Якщо в розплав електроліту, наприклад натрій хлориду, занурити інертні електроди й пропускати постійний […]...
- Електроліз розчинів та розплавів електролітів – ОКИСНО-ВІДНОВНІ ПРОЦЕСИ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ОКИСНО-ВІДНОВНІ ПРОЦЕСИ Електроліз розчинів та розплавів електролітів Сукупність ОВР, які протікають на електродах у розчинах та розплавах електролітів при пропусканні через них електричного струму, називають електролізом. На підставі етимології слова можна сказати, що електроліз (від електро… і грец. лізіс – розклад) – це […]...
- Суть електролізу – ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 7. ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ § 7.6. Суть електролізу У розчинах і розплавах електролітів є різнойменні за знаками іони (катіони й аніони), які подібно до всіх частинок рідини перебувають у хаотичному русі. Якщо в такий розчин або розплав електроліту, наприклад у розплав […]...
- Електроліз водних розчинів електролітів (кислот, основ, солей) – Електроліз ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 6. Суміші речовин. Розчини 6.13. Електроліз 6.13.2. Електроліз водних розчинів електролітів (кислот, основ, солей) Під час електролізу водних розчинів електролітів, крім катіонів і аніонів розчиненої речовини, у процесах окиснення і відновлення, що відбуваються на електродах, можуть брати участь молекули води. При цьому можуть […]...
- Електроліз водних розчинів електролітів – ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 7. ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ § 7.7. Електроліз водних розчинів електролітів Слід розрізняти електроліз розплавлених електролітів і їх розчинів. В останньому випадку в процесах можуть брати участь молекули води. Як приклад розглянемо електроліз концентрованого водного розчину хлориду натрію (електроди вугільні). В цьому […]...
- Електроліз РОЗДІЛ 3 МЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХ СПОЛУКИ § 55. Електроліз Усвідомлення змісту цього параграфа дає змогу: Формулювати означення електролізу; Пояснювати суть електролізу розплавів і розчинів солей; Прогнозувати склад продуктів електролізу: розплавів солей, розчинів солей за активністю йонів у розчині; Складати рівняння реакцій електролізу, схеми окисно-відновних процесів на електродах; Характеризувати практичне значення електролізу. Значна кількість металів […]...
- Розв’язування типових задач – ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 7. ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ § 7.9. Розв’язування типових задач Окисно-відновні реакції Задача 1. Доберіть коефіцієнти у схемі окисно-відновної реакції: S + HNO3 −> H2SO4 + NO. Розв’язання. Коефіцієнти знаходимо методом електронного балансу. Зазначимо ступені окиснення елементів, які їх змінюють: 0 +5 […]...
- Напруга розкладу – Електроліз ОКИСНЕННЯ І ВІДНОВЛЕННЯ 4 . Електроліз Електроліз – це зворотний процес окисно-відновної реакції, що спонтанно протікає в батареї. При використанні електричної енергії примусово викликають процес окисно-відновної реакції. Водночас електрична енергія перетворюється на хімічну енергію. В обох випадках електрод, на якому відбувається окиснення, називають анодом (анодний протектор). Електрод, на якому відбувається відновлення, називають катодом. У батареї […]...
- Закони Фарадея – Електроліз ОКИСНЕННЯ І ВІДНОВЛЕННЯ 4 . Електроліз 4.2 . Закони Фарадея Чим довше триває процес електролізу, тим більше речовини осідає на електродах. Між масою т, що осіла, і зарядом Q = І ∙ t, що проходить, існує лінійна залежність: m1 ~ Q і m2 ~ Q. Перший закон Фарадея: маси речовин, що осідають на електродах, пропорційні […]...
- ЕЛЕКТРОЛІЗ ВОДИ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС РЕАКЦІЇ ЗІ ЗМІНОЮ СТУПЕНІВ ОКИСНЕННЯ ЕЛЕМЕНТІВ ЕЛЕКТРОЛІЗ ВОДИ Електроліз води – окисно-відновний процес розкладу води з утворенням водню і кисню. На катоді відбувається відновлення води з утворенням іонів ОН – і молекул Н2: На аноді здійснюється окиснення води з утворенням молекул О2 і іонів Н+: Дія електричного струму призводить […]...
- Модель Томсона БУДОВА АТОМА 2. Модель Томсона Досліди Майкла Фарадея з електролізу в 1833 році та відкриття електрона Дж. Дж. Стоні в 1881 році вже неможливо було пояснити простою моделлю Дальтона. Дж. Дж. Томсон у 1904 році запропонував модель атома, що включала поняття заряду. – Атом складається з кулі, що має позитивний електричний заряд, в якій розміщені […]...
- Теорія окисно-відновних реакцій – ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 7. ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ § 7.1. Теорія окисно-відновних реакцій Усі хімічні реакції можна розділити на два типи. До першого належать реакції, які відбуваються без зміни ступеня окиснення атомів, що входять до складу реагуючих речовин. Наприклад: +1 +5 -2 +1 -2 +1 […]...
- Застосування електролізу – ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 7. ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ § 7.8. Застосування електролізу Електроліз знаходить досить широке застосування. Для захисту металевих виробів від корозії на їх поверхню наносять дуже тонкий шар іншого металу – хрому, срібла, золота, міді, нікелю тощо, іноді застосовують багатошарові покриття. Наприклад, зовнішні […]...
- Напрям струму 7. Електрика 7.11. Напрям струму За напрям електричного струму взято той напрям, у якому рухаються (або могли б рухатися) позитивно заряджені частинки – від позитивно зарядженого полюса до негативно зарядженого полюса....
- Вплив середовища на характер перебігу реакцій – ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 7. ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ § 7.4. Вплив середовища на характер перебігу реакцій Реакції окиснення – відновлення можуть відбуватися в різних середовищах: у кислому (надлишок Н+-іонів), нейтральному (Н2О) і лужному (надлишок гідроксид-іонів ОН – ). Залежно від середовища може змінюватись і характер […]...
- ЕЛЕКТРОНИ Хімія – універсальний довідник БУДОВА АТОМА ЕЛЕКТРОНИ Усі речовини електронейтральні. Атоми, як складові частини речовини, також повинні бути нейтральними. Крім позитивно зарядженого ядра, до складу атома входять негативно заряджені частинки – електрони. Електричний заряд електрона (негативний) чисельно дорівнює заряду протона (позитивному), тому зрозуміло, що в нейтральному атомі число електронів дорівнює числу протонів у його ядрі. […]...
- Складання рівнянь окисно-відновних реакцій – ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 7. ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ § 7.3. Складання рівнянь окисно-відновних реакцій Застосовуються два методи складання рівнянь окисно – відновних реакцій – метод електронного балансу і метод напівреакцій. Метод електронного балансу. За цим методом порівнюють ступені окиснення атомів у вихідних і кінцевих речовинах, […]...
- Рівняння окисно-відновної реакції – Окисно-відновні реакції ОКИСНЕННЯ І ВІДНОВЛЕННЯ 1. Окисно-відновні реакції 1.3. Рівняння окисно-відновної реакції Дуже часто важко скласти рівняння окисно-відновної реакції, якщо невідомо, як саме реагують речовини одна з одною. Використовуючи ступінь окиснення елементів, цю проблему можна вирішити. Перед складанням рівняння окисно-відновної реакції потрібно знати наступне: – який продукт окиснення і продукт відновлення утворюється; – чи проходить реакція в […]...
- Електрофільне приєднання ОРГАНІЧНІ РЕАКЦІЇ 3. Іонні реакції Іони, що утворилися при гетеролітичному розриві, можуть легко вступати в реакцію з іонами, що мають протилежний заряд. Позитивно заряджені карбкатіони утворюються, наприклад, у реакціях електрофільного приєднання, негативно заряджені карбаніони – в деяких реакціях заміщення. 3.1. Електрофільне приєднання У молекулах ненасичених вуглеводнів атоми Карбону в реакції приєднання намагаються приєднати додаткові частинки […]...
- Найважливіші окисники і відновники – ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 7. ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ § 7.2. Найважливіші окисники і відновники Відновники і окисники можуть бути як простими речовинами, тобто такими, що складаються з одного елемента, так і складними. Відповідно до їх місця в періодичній системі елементів атоми більшості металів містять на […]...
- Рівновага в окисно-відновних реакціях – Окисно-відновні реакції ОКИСНЕННЯ І ВІДНОВЛЕННЯ 1. Окисно-відновні реакції Окисно-відновна реакція складається з двох напівреакцій: напівреакції окиснення і напівреакції відновлення. Окиснення – це віддача електронів, відновлення – отримання електронів. Приклад. При згоранні магнію атоми Магнію окислюються, а молекули кисню відновлюються. При цьому кожен атом Магнію віддає два електрони кожному атому Оксигену. 1.1. Рівновага в окисно-відновних реакціях На відміну […]...
- Окисно-відновні реакції – ОКИСНО-ВІДНОВНІ ПРОЦЕСИ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ОКИСНО-ВІДНОВНІ ПРОЦЕСИ Окисно-відновні реакції За зміною ступенів окиснення елементів, що входять до складу реагентів та продуктів реакції, усі хімічні реакції можна розділити на дві групи, а саме на: 1) Реакції, що протікають без зміни ступенів окиснення всіх елементів. До таких реакцій належать, зокрема, […]...
- Класифікація окисно-відновних реакцій – ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 7. ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ § 7.5. Класифікація окисно-відновних реакцій Звичайно розрізняють три типи окисно-відновних реакцій: міжмолекулярні, внутрішньомолекулярні і реакції диспропорціонування. До міжмолекулярних належать реакції, у яких окисник і відновник входять до складу різних речовин. Розглянуті в §7.3 І 7.4 реакції належать […]...
- § 10. МОЛЕКУЛИ. АТОМИ. ХІМІЧНИЙ ЕЛЕМЕНТ № 1. Молекулами називають найменші частинки речовини, що визначають їх властивості і здатні до самостійного існування. № 2. Атом – електронейтральна частинка речовини, що складається з позитивно зарядженого ядра та негативно заряджених електронів. Головними характеристиками атома є електричний заряд ядра і розташування електронів в атомі. № 3. Хімічний елемент – сукупність атомів з однаковим зарядом […]...
- Складання рівнянь окисно-відновних реакцій – Хімічна реакція ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 4. Хімічна реакція 4.6. Складання рівнянь окисно-відновних реакцій Для складання рівнянь окисно-відновних реакцій використовують метод електронного балансу. Він грунтується на положенні, що загальна кількість електронів, які віддає відновник, має дорівнювати загальній кількості електронів, які приєднує окисник. Розгляньмо основні етапи написання окисно-відновних реакцій на […]...
- Тема 18. Загальні методи добування металів Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА ІІ ЗАВДАННЯ ДЛЯ ПЕРЕВІРКИ ЗНАНЬ НЕОРГАНІЧНА ХІМІЯ Тема 18. Загальні методи добування металів Серед чотирьох наведених варіантів відповідей виберіть одну правильну 1. Позначте метали, що зустрічаються в природі у самородному стані: A. Золото і срібло; Б. Залізо і хром; B. Калій і натрій; Г. Магній і […]...
- Будова атома 7. Електрика 7.6. Будова атома Англійський вчений Ернест Резерфорд зробив висновок про будову атома. У центрі атома є досить важка частина, що має позитивний заряд – ядро атома. Число протонів в атомному ядрі визначає атомний номер елемента і його місце в таблиці Менделєєва. На значній відстані від ядра (порівняно з його розмірами) певними орбітами рухаються […]...
- Стійкість електронних шарів. Перетворення атомів на йони – Електрон. Електронні шари ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 2. Будова атома 2.4. Електрон. Електронні шари 2.4.3. Стійкість електронних шарів. Перетворення атомів на йони Найстійкішою електронною конфігурацією атома є така, при якій у зовнішньому електронному шарі розміщується 2 (як р атома Гелію) або 8 е – (як в атомах інших інертних газів). […]...
- Зміна ступеню окиснення – Хімічна реакція ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 4. Хімічна реакція 4.5. Зміна ступеню окиснення Процес віддачі електронів атомом, молекулою або йоном називають окисненням. Атоми, молекули або йони, що віддають електрони, називають відновниками. Під час реакцій вони окислюються: Процес приєднання електронів атомом, молекулою або йоном називають відновленням. Атоми, молекули або йони, […]...
- Тематичне оцінювання з теми “Хімічний зв’язок і будова речовини” Тема 4 ХІМІЧНИЙ ЗВ’ЯЗОК І БУДОВА РЕЧОВИНИ УРОК 66 Тема. Тематичне оцінювання з теми “Хімічний зв’язок і будова речовини” Цілі уроку: узагальнити й скоригувати знання учнів з теми “Хімічний зв’язок і будова речовини”; визначити рівень навчальних досягнень учнів з теми, розуміння основних понять, уміння використовувати їх на практиці. Тип уроку: контролю й коригування знань, умінь […]...