ОДЕРЖАННЯ ВОДНЮ – ВОДЕНЬ
Хімія – універсальний довідник
ВОДЕНЬ
ОДЕРЖАННЯ ВОДНЮ
Промислові способи одержання простих речовин залежать від того, в якому вигляді відповідний елемент знаходиться у природі, тобто, що може бути сировиною для його одержання.
Кисень, що є у вільному стані, одержують фізичним способом – виділенням із рідкого повітря. А Гідроген практично весь знаходиться у вигляді сполук, тому для одержання водню застосовують хімічні методи. Зокрема, можуть бути використані реакції розкладу. Одним зі способів одержання водню є реакція
Основний промисловий спосіб одержання водню – реакція з водою метану, що входить до складу природного газу. Вона відбувається при високій температурі (легко переконатися, що під час пропускання метану навіть через воду, що кипить, ніякої реакції не відбувається):
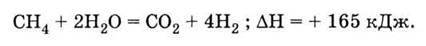
У лабораторії для одержання простих речовин використовують не обов’язково природну сировину, а вибирають ті вихідні речовини, з яких легше виділити необхідну речовину. Наприклад, у лабораторії кисень не одержують із повітря. Це ж стосується і одержання водню.
Одним із лабораторних способів одержання водню, що застосовується іноді й у промисловості, є розклад води електричним струмом.
Зазвичай у лабораторії водень одержують взаємодією цинку із хлоридною кислотою.
Related posts:
- ХІМІЧНІ ВЛАСТИВОСТІ ВОДНЮ – ВОДЕНЬ Хімія – універсальний довідник ВОДЕНЬ ХІМІЧНІ ВЛАСТИВОСТІ ВОДНЮ Молекули водню Н2 досить міцні, і для того, щоб водень міг вступити у реакцію, повинна витрачатися значна енергія: Тому при звичайних температурах водень реагує тільки з дуже активними металами, наприклад, з кальцієм, утворюючи гідрид кальцію: І з єдиним неметалом – фтором, утворюючи фтороводень: З більшістю ж металів […]...
- ФІЗИЧНІ ВЛАСТИВОСТІ ВОДНЮ – ВОДЕНЬ Хімія – універсальний довідник ВОДЕНЬ ФІЗИЧНІ ВЛАСТИВОСТІ ВОДНЮ Молекула водню двохатомна – Н2. За звичайних умов – це газ без кольору, запаху і смаку. Водень – найлегший газ, його густина у багато разів менша за густину повітря. Очевидно, що чим менша маса молекул, тим вища їхня швидкість за однакової температури. Як найлегші, молекули водню рухаються […]...
- Хімічні властивості: повне й часткове окиснення, заміщення, приєднання водню, галогенів, галогеноводнів. Одержання й використання алкінів І СЕМЕСТР Тема 2. ВУГЛЕВОДНІ Урок 15 Тема уроку. Хімічні властивості: повне й часткове окиснення, заміщення, приєднання водню, галогенів, галогеноводнів. Одержання й використання алкінів Цілі уроку: формувати знання учнів про хімічні властивості алкінів; розкрити хімічні властивості ненасичених вуглеводнів на прикладі алкінів, зумовлені наявністю кратного зв’язку, їх взаємодію з розчинами кислот, лугів, калій перманганату; формувати знання […]...
- Проста речовина кисень. Фізичні властивості кисню. Одержання кисню в лабораторії. Реакції розкладу. Поняття про каталізатори Тема 2 ПРОСТІ РЕЧОВИНИ МЕТАЛИ Й НЕМЕТАЛИ Урок 26 Тема. Проста речовина кисень. Фізичні властивості кисню. Одержання кисню в лабораторії. Реакції розкладу. Поняття про каталізатори Цілі: поглибити знання учнів про просту речовину кисень, його фізичні властивості; сформувати уявлення про реакції розкладу та каталізатори на прикладі реакцій одержання кисню в лабораторії; підготувати учнів до практичній роботі […]...
- Хімічні властивості алкенів: повне й часткове окиснення, приєднання водню, галогенів, гідрогенгалогенідів, води, полімеризація. Правило В. В. Марковнікова, механізм реакції приєднання за подвійним зв’язком. Одержання й використання алкенів І СЕМЕСТР Тема 2. ВУГЛЕВОДНІ Урок 13 Тема уроку. Хімічні властивості алкенів: повне й часткове окиснення, приєднання водню, галогенів, гідрогенгалогенідів, води, полімеризація. Правило В. В. Марковнікова, механізм реакції приєднання за подвійним зв’язком. Одержання й використання алкенів Цілі уроку: формувати в учнів знання про хімічні властивості алкенів; розкрити хімічні властивості ненасичених вуглеводнів на прикладі етену та […]...
- Водень. Фізичні властивості. Добування РОЗДІЛ 2 НЕМЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХ СПОЛУКИ ГІДРОГЕН. ВОДЕНЬ § 16. Водень. Фізичні властивості. Добування Усвідомлення змісту цього параграфа дає змогу: Характеризувати фізичні властивості, способи добування водню; складати рівняння, схеми електронного балансу відповідних хімічних реакцій. Фізичні властивості. Водень Н2 – безбарвний газ без запаху і смаку, неотруйний, найлегший на Землі. Мал. 19. Молекула водню: а […]...
- РЕАКЦІЇ РОЗКЛАДУ – ТИПИ ХІМІЧНИХ РЕАКЦІЙ Хімія – універсальний довідник ТИПИ ХІМІЧНИХ РЕАКЦІЙ РЕАКЦІЇ РОЗКЛАДУ З назви “реакція розкладу” також випливає, про який тип реакцій іде мова. У реакції розкладу відбувається розкладання складної речовини на декілька речовин. Продуктами реакції можуть бути як прості, так і складні речовини. Наприклад: Майже всі вказані реакції, як і переважна більшість інших реакцій розкладу, ендотермічні. Для […]...
- Одержання амоніаку в лабораторії. Загальна схема одержання амоніаку в промисловості I СЕМЕСТР Тема 1. НЕМЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ (18 год.) УРОК 10 Тема уроку. Одержання амоніаку в лабораторії. Загальна схема одержання амоніаку в промисловості Цілі уроку: ознайомити учнів із загальними закономірностями виробництва амоніаку; з’ясувати умови синтезу амоніаку, за яких можна керувати хімічною рівновагою; розвивати вміння й навички розв’язувати задачі з використанням поняття “вихід продукту […]...
- Вправа 146-152 № 146. Добування кисню у промисловості: 1. З повітря: – охолодження повітря і перетворення його на рідину; – підвищення температури та виділення газу азоту, потім кисню. № 147. Реакції розкладу – це реакції, під час яких із однієї речовини утворюється кілька інших. № 148. № 149. Каталізатор – речовина, яка спричиняє перебіг реакції або прискорює […]...
- Гідроген – ВОДЕНЬ. ГАЛОГЕНИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 8. ВОДЕНЬ. ГАЛОГЕНИ § 8.2. Гідроген Місце гідрогену в періодичній системі. Гідроген займає перше місце в періодичній системі (Z = 1). Він має найпростішу будову атома: ядро атома оточене електронною хмарою. Електронна конфігурація ls1. За одних умов гідроген виявляє металічні властивості […]...
- ДОБУВАННЯ КИСНЮ – КИСЕНЬ Хімія – універсальний довідник КИСЕНЬ ДОБУВАННЯ КИСНЮ Основною сировиною для промислового добування кисню є повітря. Температура кипіння кисню (-183 °С) вища, ніж температура кипіння азоту (-196 °С) – іншого основного компонента повітря, тому під час випаровування рідкого повітря швидше випаровується азот, а частина рідини, що залишилася, збагачується киснем. На цьому процесі засновано промисловий метод поділу […]...
- Хімічні властивості водню. Застосування РОЗДІЛ 2 НЕМЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХ СПОЛУКИ ГІДРОГЕН. ВОДЕНЬ § 17. Хімічні властивості водню. Застосування Усвідомлення змісту цього параграфа дає змогу: Характеризувати хімічні властивості, практичне значення водню; складати рівняння, схеми електронного балансу відповідних хімічних реакцій; Формулювати закон об’ємних відношень газів. Хімічні властивості. Атоми Гідрогену в молекулах водню сполучені між собою міцним ковалентним неполярним зв’язком, при […]...
- Узагальнення знань про кисень ТЕМА 2. ПРОСТІ РЕЧОВИНИ МЕТАЛИ І НЕМЕТАЛИ Урок 5. Узагальнення знань про кисень Цілі: закріпити знання про кисень як просту речовину, способи його добування, фізичні й хімічні властивості; закріпити вміння складати реакції розкладу і сполучення на прикладах добування і хімічних властивостей кисню; застосовувати набуті знання для складання рівнянь реакцій горіння простих і складних речовин, складати […]...
- Добування альдегідів – АЛЬДЕГІДИ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ОРГАНІЧНА ХІМІЯ АЛЬДЕГІДИ Добування альдегідів 1. Окиснення спиртів. Загальним способом добування альдегідів є реакція окиснення спиртів купрум(ІІ) оксидом: Іноді відзначають, що в реакції окиснення спиртів мідь є каталізатором унаслідок того, що отримана мідь потім окиснюється киснем повітря й знову вступає в реакцію окиснення. […]...
- Хлор – ВОДЕНЬ. ГАЛОГЕНИ-НЕОРГАНІЧНА ХІМІЯ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 8. ВОДЕНЬ. ГАЛОГЕНИ § 8.6. Хлор Поширення у природі. У природі у вільному стані хлор трапляється тільки у вулканічних газах. Дуже поширені його сполуки. Найважливіші з них: хлорид натрію NaCl, хлорид калію КСl, хлорид магнію МgСl2 ∙6Н2О, сильвініт, що складається з […]...
- Водень – Гідроген ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 9. Неметалічні елементи та їхні сполуки. Неметали Атоми неметалічних елементів мають у зовнішньому енергетичному рівні (окрім енергетичних елементів) значну кількість електронів (від чотирьох до семи) і здатні приєднувати певну кількість електронів, а саме стільки, скільки їх не вистачає до октету. Розгляньмо електронну будову […]...
- Практична робота 3. Одержання кисню в лабораторії та вивчення його властивостей Тема 2 ПРОСТІ РЕЧОВИНИ МЕТАЛИ Й НЕМЕТАЛИ Урок 28 Практична робота 3. Одержання кисню в лабораторії та вивчення його властивостей Цілі: продовжити формувати навички роботи з хімічними речовинами й лабораторним устаткуванням; навчити збирати установку для одержання газів, збирати газ витисненням повітря і води; формувати навички й уміння проведення хімічного експерименту й аналізу явищ, що спостерігаються, […]...
- Гідроген – ГІДРОГЕН. ВОДЕНЬ. ВОДА Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЯ ЕЛЕМЕНТІВ ГІДРОГЕН. ВОДЕНЬ. ВОДА Гідроген Характеристика хімічного елемента Гідроген – 1-й елемент Періодичної системи (заряд ядра 1), хімічний знак – Н, відносна атомна маса 1,008 (округлено 1). Валентність Гідрогену у сполуках дорівнює одиниці, найпоширеніший ступінь окиснення +1. Молекула водню Н2, молекулярна маса […]...
- Каталіз ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ 4. Каталіз Багато реакцій, які відповідно до енергетичних передумов повинні відбуватися спонтанно, не починаються або проходять дуже повільно. Приклад. Для процесу утворення газоподібної води з водню і кисню при 25 °С енергія Гіббса реакції ∆G°298 = -229 кДж/моль. Проте суміш водню і кисню може зберігатися як завгодно довго, реакція за цих умов […]...
- ВОДЕНЬ У ПРИРОДІ – ВОДЕНЬ Хімія – універсальний довідник ВОДЕНЬ ВОДЕНЬ У ПРИРОДІ За поширенням у Всесвіті Гідроген займає перше місце. На його частку припадає близько 92% всіх атомів (8% складають атоми Гелію, частка всіх інших разом узятих елементів – менше 0,1%). Таким чином, Гідроген – основна складова частина зірок і міжзоряного газу. В умовах зоряних температур (наприклад, температура поверхні […]...
- Хлороводень і хлоридна кислота – ВОДЕНЬ. ГАЛОГЕНИ-НЕОРГАНІЧНА ХІМІЯ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 8. ВОДЕНЬ. ГАЛОГЕНИ § 8.7. Хлороводень і хлоридна кислота Хлороводень – одна з найважливіших сполук хлору. Це безбарвний газ із різким запахом. Під час вдихання подразнює дихальні шляхи і викликає ядуху. В 1,3 раза важчий за повітря. У вологому повітрі “димить”, […]...
- Радикальне заміщення – Радикальні реакції ОРГАНІЧНІ РЕАКЦІЇ 2. Радикальні реакції Радикали мають високу реакційну здатність і в реакції з молекулами реагенту утворюють нові радикали, які у свою чергу утворюють нові радикали і т. д. У результаті відбувається ланцюгова реакція, в якій світло або теплова енергія, що поступає, дають лише “початковий поштовх”. Після запуску ланцюгової реакції радикалів вона може повторюватися декілька […]...
- Хімічні властивості бензену: повне й часткове окиснення, приєднання, заміщення. Одержання й використання бензену І СЕМЕСТР Тема 2. ВУГЛЕВОДНІ Урок 17 Тема уроку. Хімічні властивості бензену: повне й часткове окиснення, приєднання, заміщення. Одержання й використання бензену Цілі уроку: формувати в учнів знання про хімічні властивості бензену та його похідних, про реакції приєднання й заміщення в бензольному кільці; розвивати вміння складати хімічні рівняння на прикладі властивостей бензену; ознайомити учнів з […]...
- ЕЛЕКТРОЛІЗ ВОДИ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС РЕАКЦІЇ ЗІ ЗМІНОЮ СТУПЕНІВ ОКИСНЕННЯ ЕЛЕМЕНТІВ ЕЛЕКТРОЛІЗ ВОДИ Електроліз води – окисно-відновний процес розкладу води з утворенням водню і кисню. На катоді відбувається відновлення води з утворенням іонів ОН – і молекул Н2: На аноді здійснюється окиснення води з утворенням молекул О2 і іонів Н+: Дія електричного струму призводить […]...
- Методи добування алканів – НАСИЧЕНІ ВУГЛЕВОДНІ. АЛКАНИ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ОРГАНІЧНА ХІМІЯ НАСИЧЕНІ ВУГЛЕВОДНІ. АЛКАНИ Методи добування алканів Основні природні джерела алканів – нафта й природний газ. Різні фракції нафти містять алкани від С5Н12 до С30Н62. Природний газ складається з метану (95 %) з домішкою етану та пропану. Із синтетичних методів добування алканів […]...
- Зворотність реакції – Рушійна сила хімічних реакцій ЕНЕРГЕТИКА ХІМІЧНИХ РЕАКЦІЙ 3. Рушійна сила хімічних реакцій 3.5 . Зворотність реакції Відповідно до рівняння Гіббса-Гельмгольца, вільна енергія реакції ∆G0R залежить від температури. Якщо не враховувати залежність температури від ∆H0R і ∆S0R, то рівняння Гіббса-Гельмгольца відповідає рівнянню прямої. Залежно від знаків ∆H0R і ∆S0R розрізняють чотири типи реакції. Тип 1: при температурі Т < Т0 […]...
- ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ – КИСЕНЬ Хімія – універсальний довідник КИСЕНЬ ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ Швидкість реакції – це кількість речовини, що реагує за одиницю часу. Залежно від умов одна і та ж реакція може протікати з різною швидкістю. Так, при збільшенні кількості речовини, що реагує в одиниці об’єму, тобто його концентрації, швидкість реакції зростає, тому що зростає число зіткнень частинок, що […]...
- Хімічні властивості кисню. Реакція сполучення. Поняття про оксиди ТЕМА 2. ПРОСТІ РЕЧОВИНИ МЕТАЛИ І НЕМЕТАЛИ Урок 2. Хімічні властивості кисню. Реакція сполучення. Поняття про оксиди Цілі: закріпити знання про способи добування кисню, його фізичні властивості, реакцію розкладу, каталізатор; вивчити хімічні властивості кисню на прикладах взаємодії з фосфором, вуглецем, сіркою; дати поняття про реакції сполучення, горіння, оксиди. Обладнання: таблиця “Типи хімічних реакцій”, кисень у […]...
- Типи хімічних реакцій – Хімічна реакція ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 4. Хімічна реакція 4.3. Типи хімічних реакцій Хімічні реакції класифікують за різними ознаками: – за фазовим станом середовища; – за типом перетворення реагентів; – за тепловим ефектом; – за ознакою зміни ступенів окиснення; – за оборотністю. Фазовий стан середовища Залежно від фазового стану […]...
- ПАЛИВНИЙ ЕЛЕМЕНТ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС РЕАКЦІЇ ЗІ ЗМІНОЮ СТУПЕНІВ ОКИСНЕННЯ ЕЛЕМЕНТІВ ПАЛИВНИЙ ЕЛЕМЕНТ Паливний елемент – гальванічний елемент, у якому окисно-відновна реакція підтримується безперервною подачею реагентів (окисника і відновника) та видаленням продуктів реакції. У воднево-кисневому елементі (рис. 40) в електричну енергію перетворюється енергія хімічної реакції Рис. 40. Схема паливного елемента. Електроліт – розчин лугу. […]...