СПОСОБИ ВИРАЖЕННЯ КІЛЬКІСНОГО СКЛАДУ РОЗЧИНУ – ВОДА. ВОДНІ РОЗЧИНИ
Хімія – універсальний довідник
ВОДА. ВОДНІ РОЗЧИНИ
СПОСОБИ ВИРАЖЕННЯ КІЛЬКІСНОГО СКЛАДУ РОЗЧИНУ
Розчини – речовини змінного складу. Природно, що від кількісного складу розчину залежать його властивості, тому при описі властивостей розчину необхідно вказувати його склад.
Склад розчину характеризують відносним вмістом у ньому розчиненої речовини. Прийнято виражати склад розчинів через частки або концентрації.
Частка показує відношення маси, об’єму або кількості (виражене в молях) розчиненої речовини до сумарної
Масова частка розчиненої речовини – це відношення його маси m до маси розчину mp. Її прийнято позначати латинською літерою w (дубль-ве):
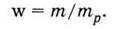
Ця величина виражається в частках одиниці або у відсотках.
У лабораторній практиці часто використовують молярну концентрацію. Молярна концентрація – це відношення кількості розчиненої речовини ν (в молях) до об’єму розчину V (в літрах). Її прийнято позначати літерою С:
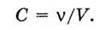
Наприклад, якщо 1 л розчину сульфатної кислоти містить 2 моль Н2SO4, то це означає, що молярна концентрація дорівнює 2 моль/л. Такий розчин називають двомолярним і позначають так: 2М Н2SO4. Запис 0,1 М розчин NаСl означає, що віл розчину міститься 0,1 моль NаСl. Такий розчин називають децимолярним.
Related posts:
- Способи кількісного вираження складу розчинів – РОЗЧИНИ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ РОЗЧИНИ Способи кількісного вираження складу розчинів Для кількісного опису складу розчину часто вживають величини: масова частка розчиненої речовини й молярність розчину. Окрім цих, є й менш популярні способи: мольна частка, моляльність, нормальність, титр, об’ємна частка тощо. Способів вираження концентрації досить багато, тому що […]...
- Чисельне вираження складу розчинів – РОЗЧИНИ. ТЕОРІЯ ЕЛЕКТРОЛІТИЧНОЇ ДИСОЦІАЦІЇ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 5. РОЗЧИНИ. ТЕОРІЯ ЕЛЕКТРОЛІТИЧНОЇ ДИСОЦІАЦІЇ § 5.1. Чисельне вираження складу розчинів У природі й техніці розчини мають величезне значення. Рослини засвоюють речовини у вигляді розчинів. Засвоєння їжі пов’язане з переходом поживних речовин у розчин. Усі природні води є розчинами. Розчинами є […]...
- РОЗЧИНЕННЯ – ФІЗИКО-ХІМІЧНИЙ ПРОЦЕС – ВОДА. ВОДНІ РОЗЧИНИ Хімія – універсальний довідник ВОДА. ВОДНІ РОЗЧИНИ РОЗЧИНЕННЯ – ФІЗИКО-ХІМІЧНИЙ ПРОЦЕС Під час змішування речовин залежно від їх природи й умов, у яких здійснюється операція змішування, можливі три граничні випадки. 1. Речовини не змінюються. Утворюється механічна суміш. Її склад змінний, речовини можуть знаходитися в ній у будь-яких співвідношеннях. Властивості механічної суміші є сумою властивостей речовин, […]...
- Кількісний склад розчинів РОЗДІЛ 1 ПОВТОРЕННЯ ТА ПОГЛИБЛЕННЯ ТЕОРЕТИЧНИХ ПИТАНЬ КУРСУ ХІМІЇ ОСНОВНОЇ ШКОЛИ § 12. Кількісний склад розчинів Усвідомлення змісту цього параграфа дає змогу: Пояснювати поняття “молярна концентрація”, “масова частка” розчиненої речовини; Вміти визначати зазначені поняття, обчислювати склад розчинів і виготовляти розчини з певною молярною концентрацією розчиненої речовини. Кількісний склад розчинів найчастіше виражається безрозмірною відносною величиною – […]...
- РОЗЧИННІСТЬ РЕЧОВИНИ – ВОДА. ВОДНІ РОЗЧИНИ Хімія – універсальний довідник ВОДА. ВОДНІ РОЗЧИНИ РОЗЧИННІСТЬ РЕЧОВИНИ Під час утворення механічної суміші взаємодії між речовинами – компонентами суміші відсутні, тому речовини фізично можуть змішуватися у будь-яких кількісних співвідношеннях. Утворення хімічної сполуки в результаті хімічної реакції відповідно до закону сталості складу вимагає певних співвідношень речовин, що вступають у реакцію. Розчинення є фізико-хімічним процесом взаємодії […]...
- Масова частка розчиненої речовини – Розчини Хімія Загальна хімія Розчини Масова частка розчиненої речовини Масова частка розчиненої речовини – це відношення маси розчиненої речовини до загальної маси розчину: Масова частка виражається в частках одиниці або відсотках. В останньому випадку одержана внаслідок обчислення величина масової частки множиться на 100 %. Маса розчиненої речовинИ: Маса розчинУ: Масу розчину можна також знайти, склавши маси […]...
- КІЛЬКІСНИЙ СКЛАД РОЗЧИНУ. МАСОВА ЧАСТКА РОЗЧИНЕНОЇ РЕЧОВИНИ № 1. Масова частка розчиненої речовини (ω) – це відношення маси розчиненої речовини mрозчиненої речовини до загальної маси розчину mрозчину, яка складається з маси розчиненої речовини і маси розчинника. Масову частку обчислюють у частках від одиниці та у відсотках. № 2. Щоб визначити масову частку розчиненої речовини в розчині слід скористатися для цього такою формулою: […]...
- КІЛЬКІСНИЙ СКЛАД РОЗЧИНУ. МАСОВА ЧАСТКА РОЗЧИНЕНОЇ РЕЧОВИНИ Тема 3 ВОДА & 33. КІЛЬКІСНИЙ СКЛАД РОЗЧИНУ. МАСОВА ЧАСТКА РОЗЧИНЕНОЇ РЕЧОВИНИ Вивчення параграфа допоможе вам: · описувати кількісний склад розчину; · визначати масову частку розчиненої речовини в розчині. Характеризуючи розчин, можна зазначити масу розчиненої речовини та об’єм або масу розчинника. Наприклад, розчин масою 200 г складається з 40 г кухонної солі і 160 г […]...
- Розчини ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 6. Суміші речовин. Розчини 6.3. Розчини Розчини – гомогенні (однорідні) суміші з двох, (або кількох) речовин, відносні кількості яких можуть значно змінюватись. Будь-який розчин складається з розчиненої речовини (речовин) і розчинника, тобто середовища, у якому молекули або йони цієї речовини рівномірно розподілені. Розчинник […]...
- ВОДА – РОЗЧИННИК – ВОДА. ВОДНІ РОЗЧИНИ Хімія – універсальний довідник ВОДА. ВОДНІ РОЗЧИНИ ВОДА – РОЗЧИННИК Вода – хімічно активна речовина, що взаємодіє з багатьма іншими речовинами. Найвідоміша, видима з таких взаємодій – розчинення речовин у воді. Вода є універсальним розчинником, тобто в ній добре розчиняється багато речовин. Будь-яка природна вода є розчином, у якому містяться різні солі, гази й інші […]...
- Кількісний склад розчину. Масова частка розчиненої речовини. Приготування розчинів Тема 1 РОЗЧИНИ Урок 7 Тема уроку. Кількісний склад розчину. Масова частка розчиненої речовини. Приготування розчинів Цілі уроку: ознайомити учнів зі способами вираження складу розчинів, поняттями “масова частка розчиненої речовини”, “концентрація”; формувати навички використання цих понять для обчислень і приготування розчинів. Тип уроку: формування нових знань, умінь і навичок. Форми роботи: фронтальна бесіда, розв’язання задач. […]...
- ХІМІЧНІ ВЛАСТИВОСТІ ВОДИ – ВОДА. ВОДНІ РОЗЧИНИ Хімія – універсальний довідник ВОДА. ВОДНІ РОЗЧИНИ ХІМІЧНІ ВЛАСТИВОСТІ ВОДИ Вода реагує з багатьма металами. З найбільш активними металами (у таблиці Д. І. Менделєєва вони знаходяться в 1А і НА групах) відбуваються реакції типу: З менш активними металами вода реагує лише за високих температур (при цьому вона, зазвичай, знаходиться в газоподібному стані). У результаті реакції […]...
- ВОДА У ПРИРОДІ. ОДЕРЖАННЯ ВОДИ – ВОДА. ВОДНІ РОЗЧИНИ Хімія – універсальний довідник ВОДА. ВОДНІ РОЗЧИНИ ВОДА У ПРИРОДІ. ОДЕРЖАННЯ ВОДИ Найважливіша сполука Гідрогену і Оксигену – вода Н2О. Її роль у процесах перетворення речовин як у живій, так і неживій природі величезна. Без перебільшення можна сказати, що практично всі хімічні перетворення на Землі відбуваються або з безпосередньою участю води, або у водних розчинах, […]...
- Розчин і його компоненти. Кількісний склад розчину Тема 3 Вода & 23. Розчин і його компоненти. Кількісний склад розчину Опанувавши цю тему, ви зможете: – визначати й розрізняти компоненти розчину: розчинник. розчинену речовину; – наводити приклади розчинів, що використовуються в хімічній лабораторії; – визначати за таблицею розчинності розчинні й нерозчинні у воді речовини; – обчислювати масову частку та масу розчиненої речовини в […]...
- ВИГОТОВЛЕННЯ РОЗЧИНУ ДОСЛІДЖУЄМО НА УРОЦІ ТА ВДОМА ЛАБОРАТОРНИЙ ДОСЛІД 5 Виготовлення водних розчинів із заданими масовими частками розчинених речовин Речовини та обладнання: терези, аркуш паперу, мірна посудина, 2 хімічні стакани на 250 мл, мірна ложечка для набирання сипучих речовин, скляна паличка, цукор, дистильована вода. Розрахунки. Завдання 1. Виготовити розчин цукру масою 50 г з масовою часткою розчиненої […]...
- Поняття про розчини і розчинність – Розчини Хімія Загальна хімія Розчини Поняття про розчини і розчинність Розчини – однорідні системи, що складаються з двох і більше компонентів і продуктів їх взаємодії. Розчини належать до однорідних сумішеЙ. Так, водні розчини складаються з розчинника (води), розчиненої речовини Та продуктів їхньої взаємодії – гідратованих (сполучених з молекулами води) йоніВ. Розчинність – здатність речовини розчинятися у […]...
- Обчислення масової частки й маси речовини в розчині Тема 1 РОЗЧИНИ Урок 8 Тема уроку. Обчислення масової частки й маси речовини в розчині Цілі уроку: закріпити знання про масову частку розчиненої речовини; формувати навички й уміння обчислювати масову частку розчиненої речовини, застосовувати ці знання для обчислення маси розчиненої речовини, приготування розчинів із заданою масовою часткою розчиненої речовини. Тип уроку: застосування знань, умінь і […]...
- ФІЗИЧНІ ВЛАСТИВОСТІ ВОДИ – ВОДА. ВОДНІ РОЗЧИНИ Хімія – універсальний довідник ВОДА. ВОДНІ РОЗЧИНИ ФІЗИЧНІ ВЛАСТИВОСТІ ВОДИ Вода – єдина речовина у природі, що в земних умовах існує у всіх трьох агрегатних станах – твердому, рідкому і газоподібному. На відміну від переважної більшості інших речовин густина води у твердому стані менша, ніж у рідкому. Вода володіє найбільшою серед інших речовин теплоємністю, а […]...
- ВИГОТОВЛЕННЯ РОЗЧИНУ Тема 3 ВОДА & 35. ВИГОТОВЛЕННЯ РОЗЧИНУ Вивчення параграфа допоможе вам: · навчитись виготовляти розчини з певною масовою часткою розчиненої речовини; · розвивати навички роботи з лабораторним обладнанням і посудом. Розглянемо, що необхідно робити, чим користуватися, щоб виготовити розчин з певною масовою часткою розчиненої речовини. ЩО ПОТРІБНО ДЛЯ ВИГОТОВЛЕННЯ РОЗЧИНУ. Незалежно від того, які розчини […]...
- Розчини. Кількісний склад розчинів ЛАБОРАТОРНИЙ ДОСЛІД № 4 Виготовлення водних розчинів із заданими масовими частками розчинених речовин. Обладнання: терези, мірний циліндр, скляна паличка, хімічна склянка. Реактиви: будь-яка наявна в кабінеті хімії розчинна сіль. Правила безпеки. При проведенні дослідів: – використовуйте невеликі кількості реактивів; – остерігайтеся потрапляння реактивів на одяг, шкіру, в очі. 1. Виготовити розчин солі масою 50 г […]...
- ОДИНИЦЯ КІЛЬКОСТІ РЕЧОВИНИ – МОЛЬ Хімія – універсальний довідник КІЛЬКІСНІ ВІДНОШЕННЯ В ХІМІЇ ОДИНИЦЯ КІЛЬКОСТІ РЕЧОВИНИ – МОЛЬ Речовини, що вступають в хімічну взаємодію, можуть складатися з атомів, або молекул, або інших частинок. Кількість речовини, що реагує, зручно характеризувати числом таких частинок. Одиницею кількості речовини, що визначає число частинок, з яких ця речовина складається, є моль. Кількість речовини, виражена в […]...
- Моль. Молярна маса ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 1. ОСНОВНІ ПОНЯТТЯ І ЗАКОНИ ХІМІЇ § 1.6. Моль. Молярна маса У Міжнародній системі одиниць (Сl) за одиницю кількості речовини прийнято моль. Моль – це кількість речовини, що містить стільки структурних одиниць (молекул, атомів, іонів, електронів чи інших), скільки атомів міститься […]...
- Способи вираження простого дієслівного присудка – Присудок. Способи його вираження – Члени речення УКРАЇНСЬКА МОВА. ПІДГОТОВКА ДО ЗНО СИНТАКСИС І ПУНКТУАЦІЯ Члени речення Присудок. Способи його вираження Присудком називається головний член речення, який означає, що говориться про підмет, і відповідає на питання Що робить підмет? що з ним робиться? який він є? ким він є? Присудки бувають прості та складені. Способи вираження простого дієслівного присудка У ролі простого […]...
- СПЛАВИ МЕТАЛІВ – СПОЛУКИ ЗМІННОГО СКЛАДУ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ СПОЛУКИ ЗМІННОГО СКЛАДУ СПЛАВИ МЕТАЛІВ Для одержання сплаву суміш металів розплавляють, а потім, охолоджуючи, кристалізують. При цьому між металами відбувається хімічна взаємодія. При сплавленні металів, подібних за хімічними властивостями і близьких за розмірами атомів, утворюється твердий розчин заміщення (рис. 29). Такий розчин утворюється, наприклад, при сплавленні золота і срібла […]...
- Розв’язування типових задач Масова частка розчиненої речовини – РОЗЧИНИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 5. РОЗЧИНИ. ТЕОРІЯ ЕЛЕКТРОЛІТИЧНОЇ ДИСОЦІАЦІЇ § 5.14. Розв’язування типових задач Масова частка розчиненої речовини Задача 1. Потрібно приготувати розчин масою 320 г з масовою часткою хлориду калію 3%. Розрахуйте масу КСl і масу води, які необхідні для приготування розчину. Розв’язання. Обчислюємо […]...
- Узагальнення й систематизація знань з теми “Розчини” Тема 1 РОЗЧИНИ Урок 19 Тема уроку. Узагальнення й систематизація знань з теми “Розчини” Цілі уроку: узагальнити, систематизувати та скоригувати знання учнів з теми “Розчини”; з’ясувати рівень засвоєння знань, умінь і навичок про процеси, що протікають у розчинах, рівень розуміння основних понять, умінь використовувати їх на практиці. Тип уроку: узагальнення й систематизації знань, умінь і […]...
- Вправа 195-204 № 195. Відповідь: m(р. р.) = 6 г. № 196. Дано: Розв’язання 1. Обчислимо m розчину: 2. Обчислимо масову частку розчиненої речовини: Відповідь: ω(цукру) = 0,2 або 20 %. № 197. M (р-ну), г M (р. р.), г M (води), г ω(р. р.) 400 8 392 0,02 або 2 % 500 40 460 0,08 або […]...
- Дія буферів – Буферні розчини – Протолітична рівновага КИСЛОТИ Й ОСНОВИ 2. Протолітична рівновага 2.5. Буферні розчини Дія буферів Використовуючи константу рівноваги процесу дисоціації кислоти, можна показати дію буфера: – Додавання кислоти, тобто збільшення с(Н3О+). Для збереження рівноваги додані іони гідроксонію реагуватимуть з відповідними іонами А-, утворюючи недисоційовану НА, практично не змінюючи концентрацію іонів гідроксонію. – Додавання лугу, тобто збільшення с(ОН-). Додані гідроксид-іони […]...
- Практична робота № 1. Приготування розчину солі із заданою масовою часткою розчиненої речовини Тема 1 РОЗЧИНИ Урок 10 Тема уроку. Практична робота № 1. Приготування розчину солі із заданою масовою часткою розчиненої речовини Цілі уроку: перевірити знання правил техніки безпеки, практичні вміння й навички приготування розчинів із заданою масовою часткою розчиненої речовини. Тип уроку: практичного використання знань, умінь і навичок. Форми роботи: виконання практичної роботи. Обладнання: періодична система […]...
- Ступінь дисоціації – РОЗЧИНИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 5. РОЗЧИНИ. ТЕОРІЯ ЕЛЕКТРОЛІТИЧНОЇ ДИСОЦІАЦІЇ § 5.9. Ступінь дисоціації Оскільки електролітична дисоціація – процес оборотний, то в розчинах електролітів поряд з їх іонами є й молекули. Тому розчини електролітів характеризуються ступенем дисоціації (позначається грецькою буквою “альфа” а). Ступінь дисоціації – це […]...