Умовні позначення, назви та одиниці фізичних величин
ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ
ДОДАТОК
1. Умовні позначення, назви та одиниці фізичних величин
η – Вихід продукту (масова частка виходу) –
Аr – Відносна атомна маса –
Mr – Відносна молекулярна маса –
DH2 – Відносна густина за воднем –
Dn – Відносна густина за повітрям –
Х – Відносна електронегативність –
PH – Водневий показник –
Р – Густина г/мл, г/см, кг/л
L – Довжина –
μ – Електричний момент диполя Кл ∙ м
Е – Електродний
X – Електронегативність еВ
L – Енергія іонізації еВ
Q – Заряд електричний Кл
∆Н – Зміна ентальпії Дж
Кв – Іонний добуток води –
N – Кількість речовини моль, моль
K – Константа швидкості реакції –
M – Маса кг, г, кг, г
W – Масова частка –
С – Молярна концентрація моль/л
М – Молярна маса г/моль
Vm – Молярний об’єм газу л/моль
V – Об’єм л, м3
Е – Спорідненість до електрода еВ
Na – Стала Авогадро моль-1
Е° – Стандартний електродний потенціал В
А – Ступінь дисоціації –
Т – Температура –
T
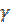 – Температурний коефіцієнт швидкості –
– Температурний коефіцієнт швидкості –
Реакції
Р – Тиск Па
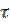 – Час с
– Час с
N – Число структурних одиниць –
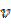 – Швидкість реакції моль/(л ∙ с)
– Швидкість реакції моль/(л ∙ с)
Related posts:
- Деякі фізичні величини та одиниці їх вимірювання – Величини та одиниці ДОДАТОК 1. Величини та одиниці Міжнародна система одиниць (Systeme International d’Unites SI = CI) встановлює одиниці, обов’язкові для всіх фізичних і хімічних величин. Деякі фізичні величини та одиниці їх вимірювання Величина Визначення Одиниця Інші одиниці Довжина 1 Шлях s 1 м Площа S S = a ∙ b 1 м2 Об’єм V V = а […]...
- Довідник формул Хімія Загальна хімія Основні поняття, закони й теорії хімії Довідник формул ; ; Об’єм V (л) ; ; Кількість речовини n (моль) ; ; Молярна маса M (г/моль) ; ; Число частинок N ; ; Густина (г/мл) Відносна густина D Масова частка елемента в складній речовині Масова частка (%) Маса розчину ; Вихід продукту реакції […]...
- Деякі похідні одиниці фізичних величин системи СІ – Одиниці фізичних величин – Фізичні величини та їх вимірювання 2. Фізичні величини та їх вимірювання 2.3. Одиниці фізичних величин 2.3.2. Деякі похідні одиниці фізичних величин системи СІ Величина Одиниця Найменування Позначення Найменування Позначення Площа S Квадратний метр М2 Об’єм V Кубічний метр М3 Швидкість V Метр за секунду М/с Кутова швидкість Ю Радіан за секунду Рад/с Прискорення A Метр за секунду у квадраті М […]...
- Одиниці фізичних величин – КІНЕМАТИКА ФІЗИКА Частина 1 МЕХАНІКА Розділ 1 КІНЕМАТИКА 1.5. Одиниці фізичних величин Фізична величина – характеристика однієї з властивостей фізичного об’єкта (фізичної системи, явища або процесу), спільна в якісному відношенні для багатьох фізичних об’єктів, проте в кількісному відношенні індивідуальна у кожного з них. Термін “величина” не треба застосовувати для позначення тільки якісного боку досліджуваної властивості, наприклад […]...
- Основні фізико-хімічні величини – ХІМІЯ Формули й таблиці ХІМІЯ Основні фізико-хімічні величини № Назва Позначення Формула Одиниці вимірювання 1 Маса M – Кг(г) 2 Атомна одиниця маси А. о. м. 3 Відносна атомна маса Аr – 4 Відносна молекулярна маса Мr Де і – число атомів у молекулі – 5 Молярна маса М 6 Кількість речовини ν Моль 7 Стала […]...
- Обчислення відносної густини газу – Приклади розв’язування типових задач ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 1. Основні хімічні поняття. Речовина Приклади розв’язування типових задач III. Обчислення відносної густини газу Формули і поняття, які використовуються: Де Dnов.(X) – відносна густина газу X за повітрям, DA(X) – відносна густина газу X за газом А, М(Х) – молярна маса газу X, […]...
- Фізичні величини. Одиниці фізичних величин Розділ І ФІЗИКА ЯК ПРИ РОДНИЧА НАУКА. МЕТОДИ НАУКОВОГО ПІЗНАННЯ &6. Фізичні величини. Одиниці фізичних величин ✓ Що називають температурою? ✓ Що таке швидкість тіла? Для того, щоб кількісно охарактеризувати фізичне явище, необхідно ввести певні фізичні величини. Будемо спостерігати за нагріванням води у чайнику. Ступінь нагрітості води характеризується фізичною величиною, яка називається температурою. Температура є […]...
- ДЕЯКІ ФІЗИЧНІ ВЕЛИЧИНИ І ЇХ ОДИНИЦІ – ЗАКОНИ ЗБЕРЕЖЕННЯ. СТЕХІОМЕТРІЯ Хімія – універсальний довідник ЗАКОНИ ЗБЕРЕЖЕННЯ. СТЕХІОМЕТРІЯ У хімічних реакціях атоми не утворюються заново і не руйнуються. Цей факт відображають закони стехіометрії. Маса речовин, які вступили в хімічну реакцію, дорівнює масі речовин, які утворилися в результаті реакції (закон збереження маси). Об’єми газів, що реагують, відносяться один до одного і до об’єму отриманих газів як прості […]...
- Система СІ – Одиниці фізичних величин – Фізичні величини та їх вимірювання 2. Фізичні величини та їх вимірювання 2.3. Одиниці фізичних величин 2.3.1. Система СІ № Фізична Величина Одиниця вимірювання Позна Чення Одиниці Визначення одиниць вимірювання Основні 1 Довжина l, s Метр М Довжина, що проходить світло в вакуумі за проміжок часу, який дорівнює 1/299 792 458 секунди 2 Маса m Кілограм Кг Одиниця маси, яка дорівнює […]...
- ФІЗИЧНІ ВЕЛИЧИНИ ТА ЇХ ВИМІРЮВАННЯ. ОДИНИЦІ ФІЗИЧНИХ ВЕЛИЧИН Розділ 1 ФІЗИКА ЯК ПРИРОДНИЧА НАУКА МЕТОДИ НАУКОВОГО ПІЗНАННЯ & 8. ФІЗИЧНІ ВЕЛИЧИНИ ТА ЇХ ВИМІРЮВАННЯ. ОДИНИЦІ ФІЗИЧНИХ ВЕЛИЧИН Фізичні величини. Тіла та явища розрізняються своїми властивостями. Одні тіла великі, інші маленькі. Вони різні за кольором, мають різний смак, запах, форму. Явища можуть тривати певний час, супроводжуватися змінами температури, розташуванням тіл. У повсякденному житі, в […]...
- Ізопроцеси – МОЛЕКУЛЯРНА ФІЗИКА Формули й таблиці ФІЗИКА МОЛЕКУЛЯРНА ФІЗИКА Відносна молекулярна маса Mr – відносна молекулярна маса; M0 – маса молекули даної речовини, ; M0с – маса молекули вуглецю, . Кількість речовини ν – кількість речовини, ; N – число молекул; Na – число Авогадро, NA = 6,02 · 1023 моль-1. Молярна маса М – молярна маса, . […]...
- Приставки СІ для створення десятинних та частинних одиниць – Одиниці фізичних величин – Фізичні величини та їх вимірювання 2. Фізичні величини та їх вимірювання 2.3. Одиниці фізичних величин 2.3.3. Приставки СІ для створення десятинних та частинних одиниць Найменування Позначення приставки Множник Назва множника Українське Міжнародне Екса Е E 1018 Квінтильйон Пета П P 1015 Квадрильйон Тера Т T 1012 Трильйон Гіга Г G 109 Мільярд Мега М M 106 Мільйон Кіло К K […]...
- Фізичні сталі – Величини та одиниці ДОДАТОК 1. Величини та одиниці Фізичні сталі Число, стала величина Символ Значення і розмірність Стала Авогадро Число Лошмідта NA(NL) 6,0221367 ∙ 1023 моль-1 Елементарний (електричний) заряд E 1,60217733 ∙ 10-19 Кл Стала Фарадея F 96487,0 Кл ∙ моль-1 Стала Планка H 6,6256 ∙ 10-34 Дж ∙ с Співвідношення мас протона й електрона M(p+)/m(e-) 1836,1527 Молярний […]...
- Моль. Молярна маса ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 1. ОСНОВНІ ПОНЯТТЯ І ЗАКОНИ ХІМІЇ § 1.6. Моль. Молярна маса У Міжнародній системі одиниць (Сl) за одиницю кількості речовини прийнято моль. Моль – це кількість речовини, що містить стільки структурних одиниць (молекул, атомів, іонів, електронів чи інших), скільки атомів міститься […]...
- Визначення середньої молярної маси суміші газів – Приклади розв’язування типових задач ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 1. Основні хімічні поняття. Речовина Приклади розв’язування типових задач V. Визначення середньої молярної маси суміші газів Формули і поняття, які використовуються: Де М(суміші) – середня молярна маса суміші газів, М(А), М(Б), М(В) – молярні маси компонентів суміші А, Б і В, Χ(А), χ(Б), […]...
- Умовні позначення, які застосовують на схемах 10. Додатки 20. Умовні позначення, які застосовують на схемах 1 – гальванічний елемент або акумулятор; 2 – батарея елементів та акумуляторів; 3 – з’єднання проводів; 4 – перетин проводів без з’єднання; 5 – затискачі для під’єднання якого-небудь приладу; 6 – ключ; 7 – електрична лампа; 8 – електричний дзвінок; 9 – провідник, що має певний […]...
- Фізичні величини. Вимірювання фізичних величин МЕХАНІКА РОЗДІЛ 1. ФІЗИКА ЯК ПРИРОДНИЧА НАУКА. МЕТОДИ НАУКОВОГО ПІЗНАННЯ § 4. Фізичні величини. Вимірювання фізичних величин Контрольні запитання 1. Фізична величина – це кількісно виражена характеристика тіла або фізичного явища. 2. Об’єм – характеризує загальну властивість тіла займати певну частину простору; час – характеризує тривалість фізичного процесу; довжина – характеризує розмір тіла в просторі […]...
- ТОЧНІСТЬ ВИМІРЮВАННЯ. МІЖНАРОДНА СИСТЕМА ОДИНИЦЬ ФІЗИЧНИХ ВЕЛИЧИН Розділ 1 ФІЗИКА ЯК ПРИРОДНИЧА НАУКА. ПІЗНАННЯ ПРИРОДИ &5. ТОЧНІСТЬ ВИМІРЮВАННЯ. МІЖНАРОДНА СИСТЕМА ОДИНИЦЬ ФІЗИЧНИХ ВЕЛИЧИН Виконання лабораторних робіт пов’язане з вимірюванням різних фізичних величин і подальшою обробкою результатів. Одержані результати в ході будь-якого фізичного експерименту завжди міститимуть певні похибки (будуть неточними), оскільки вимірювання практично неможливо провести з абсолютною точністю. Вимірювання – знаходження значення фізичної […]...
- Кількісний склад розчинів РОЗДІЛ 1 ПОВТОРЕННЯ ТА ПОГЛИБЛЕННЯ ТЕОРЕТИЧНИХ ПИТАНЬ КУРСУ ХІМІЇ ОСНОВНОЇ ШКОЛИ § 12. Кількісний склад розчинів Усвідомлення змісту цього параграфа дає змогу: Пояснювати поняття “молярна концентрація”, “масова частка” розчиненої речовини; Вміти визначати зазначені поняття, обчислювати склад розчинів і виготовляти розчини з певною молярною концентрацією розчиненої речовини. Кількісний склад розчинів найчастіше виражається безрозмірною відносною величиною – […]...
- Похибки та оцінювання точності вимірювань. Міжнародна система одиниць фізичних величин МЕХАНІКА РОЗДІЛ 1. ФІЗИКА ЯК ПРИРОДНИЧА НАУКА. МЕТОДИ НАУКОВОГО ПІЗНАННЯ § 5. Похибки та оцінювання точності вимірювань. Міжнародна система одиниць фізичних величин Запитання до вивченого 1. При прямих вимірюваннях приладом фізичної величини максимально можлива абсолютна похибка? – дорівнює ціні поділки шкали приладу, якщо значення фізичної величини збігається зі штрихом шкали; дорівнює половині ціни поділки шкали, […]...
- ОДИНИЦЯ КІЛЬКОСТІ РЕЧОВИНИ – МОЛЬ Хімія – універсальний довідник КІЛЬКІСНІ ВІДНОШЕННЯ В ХІМІЇ ОДИНИЦЯ КІЛЬКОСТІ РЕЧОВИНИ – МОЛЬ Речовини, що вступають в хімічну взаємодію, можуть складатися з атомів, або молекул, або інших частинок. Кількість речовини, що реагує, зручно характеризувати числом таких частинок. Одиницею кількості речовини, що визначає число частинок, з яких ця речовина складається, є моль. Кількість речовини, виражена в […]...
- ФІЗИЧНІ ВЕЛИЧИНИ. ВИМІРЮВАННЯ ФІЗИЧНИХ ВЕЛИЧИН РОЗДІЛ 1 ФІЗИКА ЯК ПРИРОДНИЧА НАУКА. ПІЗНАННЯ ПРИРОДИ & 4. ФІЗИЧНІ ВЕЛИЧИНИ. ВИМІРЮВАННЯ ФІЗИЧНИХ ВЕЛИЧИН Як ви вважаєте, наскільки часто люди виконують вимірювання? Наскільки важливо вміти це робити правильно? яких наслідків слід очікувати, якщо результати вимірювань будуть хибними? Щоб допомогти вам відповісти на ці запитання, нагадаємо кілька приладів, якими ви та ваша родина користуєтесь майже […]...
- Основні фізичні величини, які використовують у хімії Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ОСНОВНІ ЗАКОНИ Й ПОНЯТТЯ ХІМІЇ Основні фізичні величини, які використовують у хімії У хімії використовують такі фізичні величини: маса, об’єм, кількість речовини, густина, атомна маса, відносна атомна й молекулярна маса, молярна маса, молярний об’єм, відносна густина газів, тиск, температура, час, концентрація, швидкість хімічної […]...
- Тематичне оцінювання з теми “Кількість речовини. Розрахунки за хімічними формулами” Тема 1 КІЛЬКІСТЬ РЕЧОВИНИ. РОЗРАХУНКИ ЗА ХІМІЧНИМИ ФОРМУЛАМИ УРОК 10 Тема. Тематичне оцінювання з теми “Кількість речовини. Розрахунки за хімічними формулами” Цілі уроку: перевірити рівень знань учнів та їх уміння виконувати розрахунки з використанням понять “кількість речовини”, “молярна маса”, “молярний об’єм”, “відносна густина газу”; виявити рівень навчальних досягнень учнів з теми. Тип уроку: контроль знань, […]...
- Вимірювання фізичних величин Розділ І ФІЗИКА ЯК ПРИ РОДНИЧА НАУКА. МЕТОДИ НАУКОВОГО ПІЗНАННЯ &7. Вимірювання фізичних величин ✓ Що називають фізичною величиною? ✓ Які вимірювальні прилади ви знаєте? 1. Джерелом наших знань про природу є спостереження й експерименти. Під час проведення фізичних дослідів доводиться вимірювати найрізноманітніші величини. Наприклад, спостереження та численні експерименти показують, що об’єм тіла збільшується з […]...
- Кількість речовини, молярна маса ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 1. Основні хімічні поняття. Речовина 1.7. Кількість речовини, молярна маса Кількість речовини п (або V, ню) – це фізична величина, яка визначає кількість частинок (молекул, атомів, йонів, йонних угруповань – асоціатів) у певній її порції. Одиницею вимірювання кількості речовини є моль. Моль – […]...
- Одиниці вимірювання величин НУМЕРАЦІЯ БАГАТОЦИФРОВИХ ЧИСЕЛ Одиниці вимірювання величин ОДИНИЦІ ВИМІРЮВАННЯ ДОВЖИНИ 315. 1) Назви відомі тобі одиниці довжини, починаючи з найменшої (міліметр) і закінчуючи найбільшою (кілометр). 2) Прочитай і запам’ятай. 1 м = 10 дм 1 км = 1000 м 1 м = 100 см 1 дм = 10 см 1 м 1000 мм 1 см = […]...
- Розв’язування розрахункових задач на виведення формули органічної речовини Хімія Органічна хімія Вуглеводні Розв’язування розрахункових задач на виведення формули органічної речовини Задача. Визначте істинну формулу вуглеводню, при спалюванні 4,4 г якого одержали 13,2 г карбон(IV) оксиду і 7,2 г води. Відносна густина парів вуглеводню за воднем дорівнює 22. Розв’язання I спосіб 1) Напишемо рівняння реакції: . 2) Із рівняння реакції видно, що всі атоми […]...
- Умовні одиниці Умовні одиниці – натуральні вимірники, що використовуються в системі бухгалтерського обліку для зведення не порівняльних (важкопорівняльних) показників до єдиної порівняльної бази. У. о. є тонно – кілометри, тисячі умовних банок, умовні еталонні гектари, кормо-дні, умовні голови тварин, рамо-дні, квадратні метро-дні та ін. За допомогою У. о. ведуть облік виробленої продукції (виконаних робіт, наданих послуг) або […]...
- Карта України. Умовні позначення на карті (рівнини, гори, водойми) МОЯ КРАЇНА – УКРАЇНА Урок 61 Тема. Карта України. Умовні позначення на карті (рівнини, гори, водойми) Мета: дати учням уявлення про карту України та умовні позначення на ній рівнин, гір, річок, морів; учити знаходити на карті України рівнини, гори, водойми; розвивати мислення, мовлення, увагу, спостережливість; розширювати світогляд дітей; виховувати любов до рідної країни. ХІД УРОКУ […]...