Урок 7. Поняття про органічні та неорганічні речовини
Урок 7. Поняття про органічні та неорганічні речовини
Мета: дати поняття про органічні та неорганічні речовини; формувати вміння орієнтуватися в елементарних термінах хімічної науки; визначати та класифікувати речовину за їх будовою або складом; аналізувати й систематизувати значний обсяг інформації, розвивати навички самостійної та групової роботи, виховувати самостійність та відповідальність.
Тип уроку: формування нових знань та їх узагальнення.
Хід уроку
I. Організаційний момент
II. Мотивація навчальної та пізнавальної
Чи знаєте ви, що…
1. У 1860 році було відомо понад 60 хімічних елементів, а на сьогоднішній день відкрито більше 114 елементів?
2. В організмі людини близько 70 хімічних елементів у складі простих і складних речовин, найбільша масова частка в нашому організмі – кисню, вуглецю, азоту, кальцію?
3. Для виготовлення однієї лампочки накалювання потрібно використати 7 різних металів (залізо, вольфрам, свинець, цинк, Ni, Sn, Sb)?
4. Вуглець називають царем “живої” природи, а кремній – царем “неживої природи”?
Учитель наголошує на важливості систематизації великого обсягу знань.
Поки
Втім, і алхіміки виявляли бажання навести лад у списку хімічних реактивів. Вони теж виділяли серед речовин “масла”, “землі”, “парфуми” (спирти), “горілки”, “стекла”… Так, сульфатну кислоту називали “купоросним маслом”, хлорну – “духом солей”. Залізний купорос був відомий під назвою “зеленого скла” (“вітріола”). Правда, алхімічні терміни часом збігалися для речовин, зовсім різних за складом. Наприклад, назва “магнезія біла” стосувалася карбонату магнію, а “магнезія чорна” – діоксиду марганцю. Іноді, навпаки, та сама речовина могла фігурувати під різними назвами. Оцтова кислота була відома як “кисла вологість” й “деревна кислота”, а нітратна – як “міцна горілка”, “селітряна димчаста горілка” й “кислота, що світиться червоним гасом”…
За розробку системи класифікації й номенклатури хімічних речовин вперше (а це розпочалося 1787 р.) взялася четвірка французьких учених: Антуан – Лоран Лавуазьє (1743-1794), Клод-Луї Бертолле (1748-1822), Луї-Бернар Гітон де Морво (1737-1816) й Антуан Фуркруа (1755-1809).
Понад двісті років тому вони прийняли рішення “розкласти по поличках” всі хімічні знання. Це завдання було б не під силу одній людині, навіть досить визначній і талановитій. Але чотири видатних учені виявилися спроможними класифікувати речовини.
Адже за справу узялися блискучо обізнані й енергійні люди. Фуркруа й Гитон де Морво були не тільки хіміками, але й видатними державними діячами, Бертолле був відомим лікарем й аптекарем, навіть служив лейбмедиком при дворі герцога Орлеанського. А Лавуазьє здобув визнання і як хімік, і як юрист, і як фінансист.
Яка властивість у речовин найголовніша? Запах, кольори, смак? Здатність розчинятися чи випаровуватися? Придатність до споживання у їжу або застосовність їх як ліки? Мабуть, жодний із цих варіантів.
Хімія вивчає хімічні реакції між речовинами, тож є сенс вибрати якусь речовину-еталон (зразок), з якою по черзі взаємодіятимуть всі інші. З часом ми подивимося, що із цього вийде. У тій хімічній класифікації, якою ми користуємося, речовин-еталонів відразу дві, і ми добре їх знаємо. Це вода й кисень.
ІІІ. Вивчення нового материалу
1. Звучать доповіді учнів, які готували індивідуальні випереджальні завдання (див. додаток).
Під час доповіді на дошці складається схема:
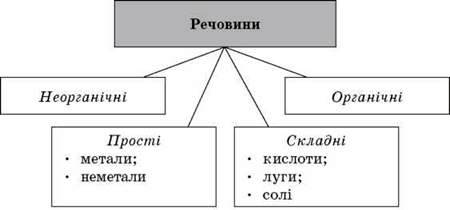
2. Після цього доповідають представники домашніх груп за темами:
¦ “новини з кухні”;
¦ “Швидка допомога в побуті”;
¦ “За дверима ванної кімнати”;
¦ “наша сумка небезпечна і складна”;
¦ “Солянка з подіуму краси”.
3. Використовуючи текст підручника (або роздавальний матеріал), учні складають таблицю.
Назва тіла | Уміст речовин |
Неорганічні | Органічні |
IV. Закріплення знань
У класі формується кілька команд для проведення експериментального туру. Командам пропонується розділити суміші:
¦ крейди й цукру;
¦ води та спирту;
¦ олії та води;
¦ мідних та залізних ошурок та ін.
V. Домашнє завдання
Підготуватися до підсумкового уроку.
Урок 8. Підсумковий. (Проводиться на розсуд учителя)