Брутто, структурні та електронні формули сполук – ЗАГАЛЬНА ХАРАКТЕРИСТИКА ОРГАНІЧНИХ СПОЛУК
Хімія підготовка до ЗНО та ДПА
Комплексне видання
ЧАСТИНА І
ЗАГАЛЬНА ХІМІЯ
ОРГАНІЧНА ХІМІЯ
ЗАГАЛЬНА ХАРАКТЕРИСТИКА ОРГАНІЧНИХ СПОЛУК
Брутто, структурні та електронні формули сполук
Другий постулат Вутлерова. Хімічні реакційні здатності певних груп атомів суттєво залежать від їхнього хімічного оточення, тобто від того, з якими атомами або групами атомів сусідить певна група.
Формули сполук, якими ми користалися при вивченні неорганічної хімії, відображають тільки кількість атомів того чи іншого елемента в
Як випливає з першого постулату Вутлерова, в органічній хімії важлива не тільки кількість тих чи інших атомів у молекулі, а ще й порядок їхнього зв’язування, тобто брутто-формули не завжди доцільно використовувати для органічних сполук. Наприклад, для наочності при розгляді структури молекули метану ми використовували структурні формули – схематичне зображення порядку зв’язування атомів у молекулу. При зображенні структурних формул хімічний зв’язок позначають рискою, подвійний зв’язок – двома
Електронна формула (або формула Льюїса) дуже схожа на структурну формулу, але в цьому випадку зображають не утворені зв’язки, а електрони, як ті, що утворюють зв’язок, так і ті, що його не утворюють.
Наприклад, уже розглянуту сульфатну кислоту можна записати за допомогою таких формул. Брутто-формула – Н2804, структурна й електронна формули мають такий вигляд:
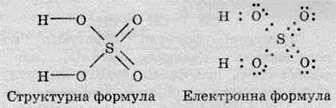
Структурні формули органічних сполук
Майже всі органічні речовини складаються з молекул, склад яких виражається хімічними формулами, наприклад СН4, С4Н10, С2Н4О2. А яку будову мають молекули органічних речовин? Це питання ставили собі в середині XIX століття засновники органічної хімії – Ф. Кекуле і О. М. Вутлеров. Досліджуючи склад і властивості різних органічних речовин, вони прийшли до наступних висновків:
– атоми в молекулах органічних речовин з’єднані хімічними зв’язками в певній послідовності, відповідно до їх валентності. Цю послідовність прийнято називати хімічною будовою;
– атоми Карбону у всіх органічних сполуках чотиривалентні, а інші елементи виявляють характерні для них валентності.
Ці положення є основою теорії будови органічних сполук, сформульованої О. М. Бутлеровим в 1861 році.
Хімічну будову органічних сполук наочно подають структурними формулами, в яких хімічні зв’язки між атомами позначають рисками. Загальне число рисок, що відходять від символу кожного елемента, дорівнює валентності його атома. Кратні зв’язки зображують двома або трьома рисками.
На прикладі насиченого вуглеводню пропану С3Н8 розглянемо, як скласти структурну формулу органічної речовини.
1. Зображуємо карбоновий кістяк. У даному випадку ланцюг складається з трьох атомів Карбону:
С-С-С
2. Карбон чотиривалентний, тому від кожного атома Карбону зображуємо недостатні риски таким чином, щоб поряд з кожним атомом було по чотири риски:

3. Дописуємо символи атомів Гідрогену:
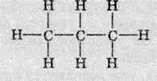
Часто структурні формули записують у скороченому вигляді, не зображуючи зв’язки С – Н. Скорочені структурні формули набагато компактніше, ніж розгорнуті:
СН3 – СН2 – СН3.
Структурні формули показують тільки послідовність з’єднання атомів, але не відображують просторової будови молекул, зокрема валентні кути. Відомо, наприклад, що кут між зв’язками С в пропані дорівнює 109,5°. Проте структурна формула пропану виглядає так, начебто цей кут дорівнює 180°. Тому вірніше було б записувати структурну формулу пропану в менш зручному, але у більш правдивому вигляді:
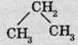
Професійні хіміки використовують такі структурні формули, в яких взагалі не показані ні атоми Карбону, ні атоми Гідрогену, а зображений лише карбоновий кістяк у вигляді з’єднаних між собою С – С-зв’язків, а також функціональні групи. Для того щоб кістяк не виглядав однією суцільною лінією, хімічні зв’язки зображують під кутом один до одного. Так, у молекулі пропану С3Н8 усього два зв’язки С-С, тому пропан зображують двома рисками.
Гомологічні ряди органічних сполук
Розглянемо структурні формули двох сполук одного класу, наприклад спиртів:
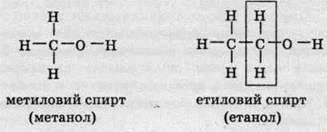
Молекули метилового СН3ОН й етилового С2Н5ОН спиртів мають однакову функціональну групу ОН, загальну для всього класу спиртів, але відрізняються довжиною карбонового кістяка: в етанолі на один атом Карбону більше. Порівнюючи структурні формули, можна помітити, що при збільшенні карбонового ланцюга на один атом Карбону склад речовини змінюється на групу СН2, при подовженні карбонового ланцюга на два атоми – на дві групи СН2 тощо.
Сполуки одного класу, що мають подібну будову, але відрізняються за складом на одну або кілька груп СН2, називають гомологами.
Групу СН2 називають гомологічною різницею. Сукупність всіх гомологів утворює гомологічний ряд. Метанол і етанол належать до гомологічного ряду спиртів. Усі речовини одного ряду мають подібні хімічні властивості, а їхній склад можна виразити загальною формулою. Наприклад, загальна формула гомологічного ряду спиртів – СnН2n+1ОН, де n – натуральне число.
Клас сполук | Загальна формула | Загальна формула з виокремленням функціональної групи |
Алкани | СnН2n+2 | |
Циклоалкани | СnН2n | |
Алкени | СnН2n | |
Алкадієни | СnН2n-2 | |
Алкіни | СnН2n-2 | |
Одноядерні арени (гомологічний ряд бензену) | СnН2n-6 | |
Одноатомні насинені спирти | СnН2n+2О | СnН2n+1ОH |
Багатоатомні спирти | СnН2n+2Оx | СnН2n+2-x(ОH)x |
Альдегіди | СnН2nО | СnН2n+1CHO |
Одноосновні карбонові кислоти | СnН2nО2 | СnН2n+1COOH |
Естери | СnН2nО | СnН2n+1COOCnH2n+1 |
Вуглеводи | Сn(Н2О)m | |
Аміни первинні | СnН2n+3N | СnН2n+1NH2 |
Амінокислоти | СnН2n+1NO | Н2NCnH2nCOOH |
