Головна ⇒ 📌Довідник з хімії ⇒ ДОНОРНО-АКЦЕПТОРНИЙ МЕХАНІЗМ УТВОРЕННЯ ХІМІЧНОГО ЗВ’ЯЗКУ
ДОНОРНО-АКЦЕПТОРНИЙ МЕХАНІЗМ УТВОРЕННЯ ХІМІЧНОГО ЗВ’ЯЗКУ
Хімія – універсальний довідник
БУДОВА РЕЧОВИНИ
ХІМІЧНИЙ ЗВ’ЯЗОК
ДОНОРНО-АКЦЕПТОРНИЙ МЕХАНІЗМ УТВОРЕННЯ ХІМІЧНОГО ЗВ’ЯЗКУ
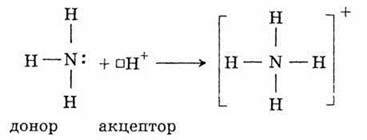
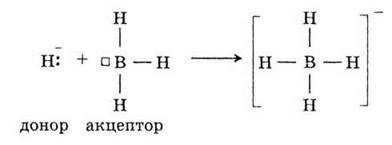
Згідно з донорно-акцепторним механізмом ковалентний зв’язок утворюється за рахунок взаємодії частинок, одна з яких має пару електронів – донор, а друга – вільну орбіталь –акцептор:
Related posts:
- УТВОРЕННЯ ХІМІЧНОГО ЗВ’ЯЗКУ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ ХІМІЧНИЙ ЗВ’ЯЗОК УТВОРЕННЯ ХІМІЧНОГО ЗВ’ЯЗКУ Хімічний зв’язок здійснюється за рахунок електростатичної взаємодії позитивно заряджених атомних ядер і негативно заряджених електронів. Під час утворення хімічних сполук з атомів виділяється енергія....
- СПОЛУЧЕННЯ АТОМІВ МІЖ СОБОЮ. УТВОРЕННЯ ХІМІЧНОГО ЗВ’ЯЗКУ Хімія – універсальний довідник БУДОВА АТОМА СПОЛУЧЕННЯ АТОМІВ МІЖ СОБОЮ. УТВОРЕННЯ ХІМІЧНОГО ЗВ’ЯЗКУ Як і чому відбувається сполучення нейтральних атомів? Почнемо пояснення з найпростішого випадку. Нехай на деякій відстані один від одного (наприклад, 0,1нм) знаходяться два протони – два ядра атома Гідрогену. У чому полягатиме їх взаємодія? Звичайно, вони будуть відштовхуватися, тому що заряджені однойменно. […]...
- Кратні зв’язки – Ковалентний зв’язок – Типи хімічного зв’язку ХІМІЧНИЙ ЗВ’ ЯЗОК 2. Типи хімічного зв’язку 2.3. Ковалентний зв’язок Формування ковалентного зв’язку відбувається також за правилом октету. Атоми з’єднуються в молекули і при цьому намагаються шляхом утворення спільних електронних пар сформувати стійку конфігурацію інертного газу. Розрізняють два випадки утворення ковалентного зв’язку: – кожен атом віддає один електрон для спільної електронної пари; – один атом […]...
- ЕНЕРГІЯ ГІББСА. УТВОРЕННЯ РЕЧОВИНИ – ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ ЕНЕРГІЯ ГІББСА. УТВОРЕННЯ РЕЧОВИНИ Стандартною молярною енергією Гіббса утворення речовини ΔG°УТB<298 називають зміну енергії Гіббса при утворенні 1 моль речовини з простих речовин у стандартних умовах. Стандартна молярна енергія Гіббса утворення простої речовини, стійкої у стандартних умовах, дорівнює нулю. Одиниця виміру енергії Гіббса утворення речовини – […]...
- СУТНІСТЬ ХІМІЧНОГО ПЕРЕТВОРЕННЯ – ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ СУТНІСТЬ ХІМІЧНОГО ПЕРЕТВОРЕННЯ Хімія вивчає перетворення речовин, які супроводжуються зміною їх складу і (або) будови. Наприклад: Суть хімічної реакції – перегрупування атомів, яке супроводжується розривом хімічних зв’язків у вихідних речовинах і утворенням хімічних зв’язків у продуктах реакції. Хімічна реакція супроводжується енергетичними змінами, тому що під час […]...
- Механізм утворення естерів – Реакції естерифікації ОРГАНІЧНІ РЕАКЦІЇ 4. Реакції естерифікації Реакцію обміну спиртів з карбоновими кислотами називають реакцією естерифікації, при відщеплюванні води утворюються естери. Приклад. Із метанової (мурашиної) кислоти і метанолу утворюється метиловий естер метанової кислоти: Естерифікація оборотна (омилення) і веде до встановлення рівноваги між початковими речовинами і продуктами реакції. Механізм утворення естерів Оскільки дана реакція оборотна, то й усі […]...
- ІОННИЙ І КОВАЛЕНТНИЙ ЗВ’ЯЗОК Хімія – універсальний довідник ВІД НАТРІЮ ДО АРГОНУ ІОННИЙ І КОВАЛЕНТНИЙ ЗВ’ЯЗОК Атоми того самого елемента притягують до себе електрони однаково, тому електрони на зв’язучій молекулярній орбіталі між однаковими атомами (у простих речовинах), можна сказати, однаковою мірою належать обом атомам. У цьому випадку кажуть про ковалентний зв’язок. Різні атоми притягують електрони з різною силою, тому […]...
- Загальна характеристика – Урок 4 – Елементи VA групи ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 9. Неметалічні елементи та їхні сполуки. Неметали 9.4. Елементи VA групи 9.4.1. Загальна характеристика До складу головної підгрупи V групи1 входять Нітроген N, Фосфор Р, Арсен As, Стибій Sb і Вісмут Ві. Будова зовнішнього електронного шару елементів – ns’2np3. Це p-елементи: Валентність Нітрогену […]...
- Гібридизація орбіталей – Ковалентний зв’язок – Типи хімічного зв’язку ХІМІЧНИЙ ЗВ’ ЯЗОК 2. Типи хімічного зв’язку 2.3. Ковалентний зв’язок Гібридизація орбіталей Виходячи з конфігурації електронів, атом Карбону мав би бути двовалентним, утворюючи зв’язки в результаті перекривання двох напівзайнятих 2р-орбіталей з орбіталями інших атомів. Проте це не так: – Карбон у своїх сполуках найчастіше є чотиривалентним. – У молекулі метану є чотири ідентичні зв’язки, які […]...
- Вандерваальсова взаємодія (сила) – Типи хімічного зв’язку ХІМІЧНИЙ ЗВ’ ЯЗОК 2. Типи хімічного зв’язку 2.5 . Вандерваальсова взаємодія (сила)1 Водневі зв’язки обумовлені постійною наявністю диполів, вандерваальсові сили виникають при взаємодії короткочасно утворених диполів. Вандерваальсовий зв’язок – найслабший з усіх типів зв’язку. Короткочасний асиметричний розподіл зарядів є тимчасовим диполем. Цей диполь може поляризувати сусідні молекули і тим самим індукувати (лат. inducere – вводити) […]...
- Полярний і неполярний ковалентний зв’язок. Властивості хімічного зв’язку Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЧНИЙ ЗВ’ЯЗОК І БУДОВА РЕЧОВИНИ Полярний і неполярний ковалентний зв’язок. Властивості хімічного зв’язку Полярність ковалентного зв’язку У молекулах водню, фтору й фтороводню між атомами утворюється ковалентний зв’язок за рахунок утворення спільної електронної пари. Атоми різних хімічних елементів здатні притягувати валентні електрони інших атомів. […]...
- МОЛЕКУЛЯРНІ ОРБІТАЛІ. МОЛЕКУЛА Н2 Хімія – універсальний довідник БУДОВА РЕЧОВИНИ ХІМІЧНИЙ ЗВ’ЯЗОК МОЛЕКУЛЯРНІ ОРБІТАЛІ. МОЛЕКУЛА Н2 Для опису розподілу електронної густини в молекулі використовують уявлення про молекулярну орбіталь. Молекулярна орбіталь – ділянка простору в молекулі, в якій можливе перебування електрона. Знаходження електрона між атомними ядрами молекули описує зв’язуюча молекулярна орбіталь. Знаходження електрона в молекулі за атомними ядрами описує антизв’язуюча […]...
- ОКИСНО-ВІДНОВНІ РЕАКЦІЇ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС РЕАКЦІЇ ЗІ ЗМІНОЮ СТУПЕНІВ ОКИСНЕННЯ ЕЛЕМЕНТІВ ОКИСНО-ВІДНОВНІ РЕАКЦІЇ Окисно-відновні реакції проходять за рахунок переходу електронів або атомів від одних частинок до інших. У реакції Відбувається перехід електронів від атомів заліза (відновник) до іонів Купруму (окисник). В реакції Відбувається перехід атомів Оксигену від іонів СlO – (окисник) до йонів SO32- […]...
- КАТАЛІЗ – ХІМІЧНА КІНЕТИКА. ШВИДКІСТЬ І МЕХАНІЗМ ХІМІЧНИХ РЕАКЦІЙ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ХІМІЧНА КІНЕТИКА. ШВИДКІСТЬ І МЕХАНІЗМ ХІМІЧНИХ РЕАКЦІЙ КАТАЛІЗ Каталіз – це зміна швидкості хімічної реакції речовинами (каталізаторами), які беруть участь у реакції, але не входять до складу кінцевих продуктів. За участю каталізатора хімічна рівновага системи досягається швидше, ніж без нього. Вплив у каталізатора на швидкість реакції досягають за рахунок […]...
- Зв’язок відносних електронегативностей із типом хімічного зв’язку – ХІМІЯ Формули й таблиці ХІМІЯ Зв’язок відносних електронегативностей із типом хімічного зв’язку Тип зв’язку Різниця відносних електронегативностей Ковалентний Неполярний 0 – 0,4 Полярний 0,5 – 1,9 Іонний > 1,9...
- Хімічний зв’язок РОЗДІЛ 1 ПОВТОРЕННЯ ТА ПОГЛИБЛЕННЯ ТЕОРЕТИЧНИХ ПИТАНЬ КУРСУ ХІМІЇ ОСНОВНОЇ ШКОЛИ § 7. Хімічний зв’язок Усвідомлення змісту цього параграфа дає змогу: Пояснювати природу хімічного зв’язку, суть збудженого стану атома, правило октету, кратність зв’язку; Вміти розрізняти різні типи хімічного зв’язку, пояснювати механізми їх утворення. Ви вже знаєте, що лише деякі елементи (пригадайте, які саме) за стандартних […]...
- ЕНЕРГІЯ АКТИВАЦІЇ – ХІМІЧНА КІНЕТИКА. ШВИДКІСТЬ І МЕХАНІЗМ ХІМІЧНИХ РЕАКЦІЙ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ХІМІЧНА КІНЕТИКА. ШВИДКІСТЬ І МЕХАНІЗМ ХІМІЧНИХ РЕАКЦІЙ ЕНЕРГІЯ АКТИВАЦІЇ Енергія активації Еа – надлишкова енергія, яку повинні мати молекули, щоб у результаті їхнього зіткнення відбулася хімічна реакція. Хімічна реакція Здійснюється через утворення активованого комплексу А2 … В2, в якому відбувається перегрупування атомів (рис. 44): Рис. 44. Енергетична схема проходження […]...
- ЕНЕРГІЯ (МІЦНІСТЬ) І ДОВЖИНА ХІМІЧНОГО ЗВ’ЯЗКУ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ ХІМІЧНИЙ ЗВ’ЯЗОК ЕНЕРГІЯ (МІЦНІСТЬ) І ДОВЖИНА ХІМІЧНОГО ЗВ’ЯЗКУ Енергія хімічного зв’язку – це енергія, необхідна для роз’єднання атомів і віддалення їх на таку відстань, на якій вони вже не відчувають сили притягування один до одного. Довжина зв’язку – відстань між ядрами атомів, що утворюють хімічний зв’язок....
- ПОЛОЖЕННЯ ЕЛЕМЕНТІВ У ПЕРІОДИЧНІЙ СИСТЕМІ Д. І. МЕНДЕЛЄЄВА І СТРУКТУРА УТВОРЕННЯ НИМИ ПРОСТИХ РЕЧОВИН – КРИСТАЛИ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ КРИСТАЛИ ПОЛОЖЕННЯ ЕЛЕМЕНТІВ У ПЕРІОДИЧНІЙ СИСТЕМІ Д. І. МЕНДЕЛЄЄВА І СТРУКТУРА УТВОРЕННЯ НИМИ ПРОСТИХ РЕЧОВИН Будова простих речовин визначається числом валентних електронів (рис. 24). Рис. 24. Моделі будови простих речовин елементів третього періоду: Аргон Аr – молекула одноатомна; Хлор Сl2 – молекула двохатомна; Сірка S8 – молекула восьмиатомна; Сірка […]...
- ЕНТРОПІЯ – ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ ЕНТРОПІЯ Ентропію можна охарактеризувати, як ступінь безладдя (невпорядкованості) системи. Ентропію речовини прийнято відносити до стандартних умов: до тиску р = 101 325 Па (1 атм) і, зазвичай, до температури 298 К (25 °С). Ентропія 1 моль речовини у стандартному стані називається стандартною молярною ентропією. Її позначають […]...
- Основні характеристики ковалентного зв’язку. Одинарні, подвійні, потрійні зв’язки І СЕМЕСТР Тема 2. ВУГЛЕВОДНІ Урок 7 Тема уроку. Основні характеристики ковалентного зв’язку. Одинарні, подвійні, потрійні зв’язки Цілі уроку: розвивати знання учнів про ковалентний карбон-карбоновий зв’язок на прикладі утворення? – та п-зв’язків атомами Карбону; ознайомити учнів з основними характеристиками ковалентного зв’язку (довжиною, енергією, полярністю, просторовою спрямованістю) на прикладі одинарного, подвійного, потрійного карбон-карбонового зв’язку; розширити знання […]...
- ЕНТАЛЬПІЙНИЙ І ЕНТРОПІЙНИЙ ФАКТОРИ І НАПРЯМОК ХІМІЧНОЇ РЕАКЦІЇ – ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ ЕНТАЛЬПІЙНИЙ І ЕНТРОПІЙНИЙ ФАКТОРИ І НАПРЯМОК ХІМІЧНОЇ РЕАКЦІЇ Згідно з рівнянням Можливість реакції Визначає ентальпійний фактор: ΔH < 0. Можливість реакції Визначає ентропійний фактор: TΔS > 0. Реакція протікає за високої температури....
- Структура молекулярних граток речовин – Ковалентний зв’язок – Типи хімічного зв’язку ХІМІЧНИЙ ЗВ’ ЯЗОК 2. Типи хімічного зв’язку 2.3. Ковалентний зв’язок Структура молекулярних граток речовин Молекулярні речовини утворюють у твердому агрегатному стані молекулярну гратку. На відміну від іонної гратки між молекулами в молекулярній решітці існують лише слабкі вандерваальсові зв’язки. Запам’ятайте: усі неметали, оксиди неметалів, безводні кислоти й органічні речовини у твердому стані утворюють молекулярну гратку. Через […]...
- Гібридизація електронних орбіталей ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 3. Хімічний зв’язок 3.4. Гібридизація електронних орбіталей Під час утворення молекул з ковалентним полярним зв’язком у деяких атомів відбувається характерне явище, яке називають гібридизацією електронних орбіталей – перетворення електронних орбіталей різного виду (s, р)1 на однакові за формою та енергією гібридні орбіталі. Sp3-гібридизація […]...
- Характеристика хімічних елементів – НІТРОГЕН. ФОСФОР Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЯ ЕЛЕМЕНТІВ НІТРОГЕН. ФОСФОР Характеристика хімічних елементів Властивості хімічних елементів Властивість Нітроген Фосфор Хімічний символ N Р Порядковий номер 7 15 Атомна маса 14,007 30,974 Місце в ПС 2 період; V група 3 період; V група Число електронів на енергетичних рівнях 2; 5 […]...
- Водневий зв’язок – Типи хімічного зв’язку ХІМІЧНИЙ ЗВ’ ЯЗОК 2. Типи хімічного зв’язку 2.4 . Водневий зв’язок У молекулах атоми Гідрогену крім електронної пари не мають інших електронів. Ядро атома Гідрогену (протон) дуже мале, тому густина позитивного заряду дуже велика. Якщо атоми Гідрогену утворюють молекули з найбільш електронегативними атомами, то зв’язуюча електронна пара значно відтягнута від протонів. Тому на зовнішнє оточення […]...
- Умови виникнення хімічного зв’язку Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЧНИЙ ЗВ’ЯЗОК І БУДОВА РЕЧОВИНИ Умови виникнення хімічного зв’язку Хімічний зв’язок – це взаємодія атомів, здійснювана шляхом обміну електронами або їхнім переходом від одного атома до іншого. Не всі атоми можуть взаємодіяти між собою. Буває так, що при зближенні атомів та перекриванні їхніх […]...
- ЕНЕРГІЯ ГІББСА – ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ ЕНЕРГІЯ ГІББСА Щоб однозначно оцінити можливість або неможливість здійснення реакції, необхідно враховувати як зміну ентальпії, так і зміну ентропії. Сумарну зміну ентальпії й ентропії для реакції при сталому тиску і температурі відображає зміна енергії Гіббса: Де ΔG – зміна енергії Гіббса; Т – абсолютна температура. У […]...
- Іонний зв’язок – Типи хімічного зв’язку ХІМІЧНИЙ ЗВ’ ЯЗОК 2. Типи хімічного зв’язку При утворенні хімічного зв’язку атоми, що беруть участь у ньому, намагаються набути конфігурації інертного газу. Оскільки при цьому задіяні лише оболонки валентних електронів, то для зображення атома використовують так звану формулу Льюїса, в якій зображені лише валентні електрони. Приклад. Зображення електронної будови атома Натрію і атома Хлору та […]...
- ТЕПЛОВИЙ ЕФЕКТ РЕАКЦІЇ. ЕНТАЛЬПІЯ РЕАКЦІЇ – ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ ТЕПЛОВИЙ ЕФЕКТ РЕАКЦІЇ. ЕНТАЛЬПІЯ РЕАКЦІЇ Кількість теплоти Q, яку передали системі, йде на зміну її внутрішньої енергії ΔUі на здійснення системою роботи* W проти зовнішніх сил (зовнішнього тиску р) (рис. 32): Рис. 32. Робота, яку виконує хімічна система проти зовнішнього тиску (поршень невагомий). Вуглекислий газ, який […]...