Оксиди нітрогену – ПІДГРУПА НІТРОГЕНУ
ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ
Частина II. НЕОРГАНІЧНА ХІМІЯ
Розділ 10. ПІДГРУПА НІТРОГЕНУ
§ 10.6. Оксиди нітрогену
Нітроген утворює шість кисневих сполук, в яких виявляє ступені окиснення
+1 +2 +3 +4 +4 +5
Від +1 до +5: N2O, NO, N2O3, NO2, N2O4, N2O5. При безпосередньому сполученні нітрогену з оксигеном утворюється лише оксид нітрогену(ІІ) NO, інші оксиди добувають непрямими способами. NO і NO – несолетворні оксиди, решта – солетворні. З усіх оксидів нітрогену найбільше значення мають оксиди нітрогену(ІІ) та нітрогену(ІV)
Оксид нітрогену(ІІ) NO – безбарвний газ, погано розчиняється у воді (його можна збирати у циліндрі над водою). Оксид нітрогену(ІІ) має чудову властивість: безпосередньо сполучається з киснем повітря, утворюючи бурий газ – оксид нітрогену(ІV):
2NO + O2 = 2NO2.
У лабораторних умовах оксид нітрогену(ІІ) добувають при взаємодії розведеної нітратної кислоти з міддю:
3Сu + 8HNO3 = 3Cu(NO3)2 + 2NO↑ + 4Н2О;
Оксид нітрогену(ІІ) добувають також окисненням аміаку киснем повітря за наявності каталізатора – платини (див. § 10.3). Він постійно утворюється у повітрі
Оксид нітрогену(ІV) NO2 – газ бурого кольору зі специфічним запахом, важчий за повітря, отруйний, подразнює дихальні шляхи. В лабораторних умовах NO2 добувають при взаємодії концентрованої нітратної кислоти з міддю:
Cu + 4HNO3 = Сu(NО3)2 + 2NO2↑ + 2Н2О;
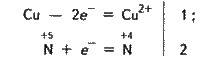
Або прожарюванням кристалічного нітрату плюмбуму:
2Рb(N3)2 = 2РbО + 4NO2 ↑ + О2 ↑.
Як зазначалося вище, оксид нітрогену(ІV) також утворюється з оксиду нітрогену(ІІ) при сполученні його з киснем.
Оксид нітрогену(ІV) піддається димеризації, утворюючи безбарвну рідину – димер оксиду нітрогену(ІV):
2NO2 ⇆ N2O4.
Реакція оборотна. При – 11С˚ рівновага практично повністю зміщується в бік утворення N2O4 (димеризація NO2), при 140°С – в бік утворення NO2 (термічна дucоціація N2O4). Проміжним температурам відповідає стан рівноваги між молекулами NO2 і N2.
Процес сполучення однакових молекул у більші молекули називається полімеризацією.
У даному випадку відбулася димеризація – утворення більшої молекули N2O4 з двох молекул NO2. Процес полімеризації відіграє важливу роль в органічній хімії (див. § 16.7).
При взаємодії оксиду нітрогену (IV) з водою утворюються нітратна і нітритна кислоти:
+4 +5 +3
2NO2 + Н2О = HNO3 + HNO2;
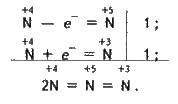
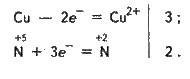
HNO2 малостійка, особливо при нагріванні. Тому при розчиненні NO2 у теплій воді утворюються нітратна кислота і оксид нітрогену(ІІ):
+4 +5 +2
3NO2 + Н2О = 2HNO3 + NO;

За надлишку кисню утворюється тільки нітратна кислота:
+4 0 +5 -2
4NO2 + 2Н2О + O2 = 4HNO3;
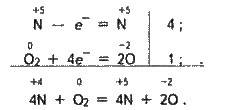
Оксид нітрогену(ІV) – сильний окисник: вугілля, фосфор, сірка горять у ньому, а оксид сульфуру(ІV) окиснюється до оксиду сульфуру(VІ).




 (1 votes, average: 5.00 out of 5)
(1 votes, average: 5.00 out of 5)Related posts:
- Оксиди Нітрогену – НІТРОГЕН. ФОСФОР Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЯ ЕЛЕМЕНТІВ НІТРОГЕН. ФОСФОР Оксиди Нітрогену Нітроген утворює оксиди, перебуваючи у всіх ступенях окиснення, тобто існують нітроген(І) оксид N2O, нітроген(ІІ) оксид NO, нітроген(ІІІ) оксид N2O3, нітроген(ІV) оксид NO2, нітроген(V) оксид N2O5. Властивість N2O NO N2O3 NO2 N2O5 Зовнішній вигляд при н. у. Безбарвний […]...
- Оксиди фосфору і фосфатні кислоти – ПІДГРУПА НІТРОГЕНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 10. ПІДГРУПА НІТРОГЕНУ § 10.11. Оксиди фосфору і фосфатні кислоти Оксиди фосфору. Фосфор утворює декілька оксидів. Найважливішими з них є Р4О6 та Р4О10. Часто їх формули пишуть у спрощеному вигляді як Р2О3 та Р2О5 (індекси попередніх поділено на 2). Оксид фосфору(ІІІ) […]...
- ОКСИДИ НІТРОГЕНУ – ХІМІЯ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ Хімія – універсальний довідник ХІМІЯ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ ОКСИДИ НІТРОГЕНУ Позитивну валентність Нітроген виявляє у сполуках з Оксигеном – оксидах. При цьому особливістю Нітрогену є те, що він утворює оксиди, які відповідають усім теоретично можливим валентностям від 1 до 5 (зовнішній енергетичний рівень атома Нітрогену містить п’ять електронів). Відповідно існують наступні оксиди нітрогену: N2O, NO, N2O3, […]...
- Взаємодія нітратної кислоти з металами і неметалами – ПІДГРУПА НІТРОГЕНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 10. ПІДГРУПА НІТРОГЕНУ § 10.8. Взаємодія нітратної кислоти з металами і неметалами При взаємодії нітратної кислоти з металами водень, як правило, не виділяється: він окиснюється, утворюючи воду. Кислота ж, залежно від концентрації і активності металу, може відновлюватися до сполук: +5 +4 […]...
- Нітратна кислота – ПІДГРУПА НІТРОГЕНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 10. ПІДГРУПА НІТРОГЕНУ § 10.7. Нітратна кислота Добування. У лабораторних умовах нітратну (азотну) кислоту добувають з її солей дією концентрованої сульфатної кислоти: KNO3 + H2SO4 = HNO3 + KHSO4. Реакція відбувається при слабкому нагріванні (сильне нагрівання розкладає HNO3). У промисловості нітратну […]...
- Солі нітратної кислоти – ПІДГРУПА НІТРОГЕНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 10. ПІДГРУПА НІТРОГЕНУ § 10.9. Солі нітратної кислоти Одноосновна нітратна кислота утворює тільки середні солі, які називаються нітратами. Вони утворюються при дії кислоти на метали, їх оксиди і гідроксиди. Нітрати натрію, калію, амонію і кальцію називаються селітрами. NaNO3 – натрієва селітра, […]...
- Оксиди Нітрогену РОЗДІЛ 2 НЕМЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХ СПОЛУКИ ХІМІЧНІ ЕЛЕМЕНТИ VA ГРУПИ § 35. Оксиди Нітрогену Усвідомлення змісту цього параграфа дає змогу: Характеризувати будову молекул оксидів Нітрогену(ІІ) і (IV), їх фізичні та хімічні властивості, добування і застосування; висловлювати судження про вплив оксидів Нітрогену на довкілля; складати рівняння та схеми електронного балансу відповідних хімічних реакцій. Нітроген утворює […]...
- Аміак – ПІДГРУПА НІТРОГЕНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 10. ПІДГРУПА НІТРОГЕНУ § 10.3. Аміак Будова молекули. Нітроген утворює з гідрогеном кілька сполук, з яких найважливішою є аміак. Електронна формула молекули аміаку така: Видно, що з чотирьох електронних пар у нітрогену – три спільні (зв’язуючі) і одна неподілена (незв’язуюча). Будову […]...
- Загальна характеристика підгрупи нітрогену – ПІДГРУПА НІТРОГЕНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 10. ПІДГРУПА НІТРОГЕНУ § 10.1. Загальна характеристика підгрупи нітрогену Підгрупу нітрогену складають п’ять елементів: нітроген, фосфор, стибій, арсен і бісмут. Це р-елементи V групи періодичної системи Д. І. Менделєєва. На зовнішньому енергетичному рівні їх атоми мають по п’ять електронів – ns2 […]...
- Оксиди карбону. Карбонатна кислота – ПІДГРУПА КАРБОНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 11. ПІДГРУПА КАРБОНУ § 11.3. Оксиди карбону. Карбонатна кислота Відомо два оксиди карбону: СО і СО2. Оксид карбону(ІІ). Оксид карбону(ІІ) СО утворюється в процесі згоряння вугілля при нестачі кисню. В промисловості його добувають пропусканням вуглекислого газу над розжареним вугіллям при високій […]...
- Нітроген(IV) оксид – Елементи VA групи ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 9. Неметалічні елементи та їхні сполуки. Неметали 9.4. Елементи VA групи 9.4.5. Нітроген( IV ) оксид Нітроген утворює п’ять оксидів зі ступенями окиснення +1, +2, +3, +4 і +5. Нітроген(ІV) оксид, нітроген діоксид NO2 за стандартних умов – це газ бурого кольору1 з […]...
- Кислотні оксиди – Оксиди – Основні класи неорганічних сполук ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 7. Основні класи неорганічних сполук 7.1. Оксиди 7.1.2. Кислотні оксиди Кислотні оксиди – це оксиди, гідрати яких є кислотами. Тому кислотні оксиди ще називають кислотними ангідридами. До кислотних оксидів належать: – оксиди неметалічних елементів; – оксиди металічних елементів з високим значенням ступенів окиснення […]...
- Тема 27. Нітратна кислота Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА ІІ ЗАВДАННЯ ДЛЯ ПЕРЕВІРКИ ЗНАНЬ НЕОРГАНІЧНА ХІМІЯ Тема 27. Нітратна кислота Серед чотирьох наведених варіантів відповідей виберіть одну правильну 1. Укажіть речовини, при взаємодії яких утворюється жовтий осад: A. Карбон(ІІ) оксид та кисень; Б. Натрій нітрит та хлоридна кислота; B. Натрій фосфат та аргентум нітрат; Г. […]...
- Азот. Сигма – та пі-зв’язки – ПІДГРУПА НІТРОГЕНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 10. ПІДГРУПА НІТРОГЕНУ § 10.2. Азот. Сигма – та пі-зв’язки Поширення у природі. Азот у природі трапляється переважно у вільному стані. У повітрі об’ємна частка його становить 78,09 %, а масова частка – 75,6 %. Сполуки нітрогену в невеликих кількостях є […]...
- Амфотерні оксиди – Оксиди – Основні класи неорганічних сполук ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 7. Основні класи неорганічних сполук 7.1. Оксиди 7.1.3. Амфотерні оксиди Амфотерні оксиди – це оксиди, які в хімічних реакціях можуть виявляти кислотні або основні властивості залежно від того, з якою сполукою вони взаємодіють. Амфотерним оксидам відповідають амфотерні гідроксиди1: До амфотерних оксидів відносять значну […]...
- Солі амонію – ПІДГРУПА НІТРОГЕНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 10. ПІДГРУПА НІТРОГЕНУ § 10.5. Солі амонію Солі амонію та їх властивості. Солі амонію складаються з катіона амонію та аніона кислоти. За будовою вони аналогічні відповідним солям однозарядних іонів металів. Солі амонію добувають при взаємодії аміаку або його водних розчинів з […]...
- Амфотерні оксиди – Амфотерні сполуки – Основні класи неорганічних сполук ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 7. Основні класи неорганічних сполук 7.5. Амфотерні сполуки Здатність сполуки виявляти основні та кислотні властивості називають амфотерністю, а саму сполуку – амфотерною. Кожному амфотерному оксидові відповідає амфотерна основа, яку теж можна розглядати як кислоту: Гідроксид Оксид Кислота Сіль Zn(OH)2 цинк гідроксид ZnO H2ZnO2 […]...
- Мінеральні добрива – ПІДГРУПА НІТРОГЕНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 10. ПІДГРУПА НІТРОГЕНУ § 10.12. Мінеральні добрива Речовини, переважно солі, які містять необхідні для рослин елементи живлення, називаються мінеральними добривами. їх вносять у грунт для підвищення його родючості з метою вирощування високих та стійких врожаїв. Макро – та мікродобрива. Основними хімічними […]...
- Оксиди Карбону – Елементи IV групи ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 9. Неметалічні елементи та їхні сполуки. Неметали 9.5. Елементи IV Групи 9.5.3. Оксиди Карбону Карбон утворює два оксиди – карбон(ІІ) оксид СО та карбон(ІV) оксид СO2 зі ступенями окиснення Карбону відповідно +2 та +4. Карбон(ІІ) оксид, карбон монооксид Атом Карбону в цьому оксиді […]...
- Оксиди – НАЙВАЖЛИВІШІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 6. НАЙВАЖЛИВІШІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК § 6.1. Оксиди Класифікація речовин полегшує їх вивчення. Знаючи особливості класів сполук, можна схарактеризувати властивості окремих їх представників. Найважливішими класами неорганічних сполук є оксиди, кислоти, основи, солі. Оксидами називаються складні речовини, до яких входять два елементи, […]...
- ОКСИДИ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ. КИСЛОТНИЙ ХАРАКТЕР ОКСИДІВ І ГІДРАТІВ ОКСИДІВ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ ТЕМА 1. НЕМЕТАЛІЧНІ ЕЛЕМЕНТИ ТА ЇХНІ СПОЛУКИ УРОК 8. ОКСИДИ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ. КИСЛОТНИЙ ХАРАКТЕР ОКСИДІВ І ГІДРАТІВ ОКСИДІВ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ Цілі: формувати знання про оксиди неметалічних елементів, їх добування і властивості, формули й характер відповідних їм гідратів та вміння складати формули сполук і хімічні рівняння, що характеризують властивості й добування оксидів неметалів. Обладнання: роздавальний матеріал, […]...
- Амфотерні оксиди та гідроксиди – ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК Амфотерні оксиди та гідроксиди Поняття про амфотерність Іноді трапляються сполуки, які можуть проявляти і кислотні, і основні властивості. Речовини, які можуть виявляти кислотні й основні властивості залежно від сполуки, з якою вони взаємодіють, називають амфотерними. Амфотерність виявляють оксиди й […]...
- Оксид сульфуру – ПІДГРУПА ОКСИГЕНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 9. ПІДГРУПА ОКСИГЕНУ § 9.5. Оксид сульфуру(І V ). Сульфітна кислота Оксид сульфуру(ІV). Оксид сульфуру(ІV), або сірчистий газ, за звичайних умов – безбарвний газ з різким, задушливим запахом. Під час охолодження до – 10°С зріджується у безбарвну рідину. У рідкому стані […]...
- Фосфор – ПІДГРУПА НІТРОГЕНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 10. ПІДГРУПА НІТРОГЕНУ § 10.10. Фосфор Фосфор – аналог нітрогену, оскільки електронна конфігурація його валентних електронів, як і у нітрогену, s2p3. Однак порівняно з атомом нітрогену атом фосфору має меншу енергію іонізації і більший радіус (див. п. З та п. 6, […]...
- Оксиди Карбону та Силіцію – КАРБОН. СИЛІЦІЙ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЯ ЕЛЕМЕНТІВ КАРБОН. СИЛІЦІЙ Оксиди Карбону та Силіцію Карбон(ІІ) оксид У молекулі карбон мснооксиду (чадного газу) СО атоми Карбону й Оксигену зв’язані потрійним зв’язком: два зв’язки утворені за ковалентним механізмом, а третій – за донорно-акцепторним: Фізичні й біологічні властивості Чадний газ являє собою […]...
- НІТРАТНА КИСЛОТА – ХІМІЯ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ Хімія – універсальний довідник ХІМІЯ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ НІТРАТНА КИСЛОТА Найважливішою сполукою Нітрогену є нітратна кислота НNO3. У ній Нітроген проявляє свою вищу валентність +5, як і у відповідному кислотному оксиді N2O5. Для одержання нітратної кислоти у промисловості використовують реакцію: Нітратна кислота (безводна) за звичайних умов є безбарвною рідиною, яка, як і сульфатна кислота, змішується з […]...
- Виявлення Нітрогену – Якісний аналіз – Визначення формули АНАЛІЗ ОРГАНІЧНИХ СПОЛУК Виявлення Нітрогену При нагріванні сполук амінів й амінокислот, що містять Нітроген, із сумішшю з натрій гідроксиду і кальцій оксиду (натронного вапна) утворюється амоніак, який ідентифікується завдяки своєму запаху за допомогою вологого індикаторного паперу або димучої (концентрованої) хлоридної кислоти....
- Оксиди та гідроксиди хрому – МЕТАЛИ ПОБІЧНИХ ПІДГРУП ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 14. МЕТАЛИ ПОБІЧНИХ ПІДГРУП § 14.3. Оксиди та гідроксиди хрому Хром утворює три оксиди: СrО, Сr2О3 та СrО3. Оксид хрому(ІІ) СrО – пірофорний чорний порошок (пірофорність – здатність в тонкоподрібненому стані займатися на повітрі). Добувають його окисненням амальгами хрому киснем повітря. […]...
- Нітроген і Фосфор. Сполуки Нітрогену та фосфору – Неметали Хімія Неорганічна хімія Неметали Нітроген і Фосфор. Сполуки Нітрогену та фосфору Нітроген і Фосфор Елементи Нітроген і Фосфор розташовані в V групі Періодичної системи, Нітроген у 2-му періоді, Фосфор – у 3-му. Електронна конфігурація атома Нітрогену: Валентність Нітрогену: III і IV, ступінь окиснення в сполуках: від –3 до +5. Будова молекули азоту: , . Електронна […]...
- Оксиди фосфору – НІТРОГЕН. ФОСФОР Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЯ ЕЛЕМЕНТІВ НІТРОГЕН. ФОСФОР Оксиди фосфору Фосфор утворює два оксиди – Р2O3 та Р2O5. Це спрощені формули речовин. Насправді молекули оксидів Фосфору мають такий склад: Р4O6 та Р4O10. Фізичні властивості Оксидів Фосфору Фосфор(ІІІ) оксид Р2O3 (фосфітний ангідрид) являє собою легкоплавку речовину (Тпл = […]...
- Хімічні основи виробництва аміаку – ПІДГРУПА НІТРОГЕНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 10. ПІДГРУПА НІТРОГЕНУ § 10.4. Хімічні основи виробництва аміаку Теорія синтезу аміаку з простих речовин досить складна. Тут лише зазначаються оптимальні умови процесу, що грунтуються на принципі зміщення хімічної рівноваги. Оскільки ця реакція екзотермічна, то при зниженні температури рівновага зміщуватиметься в […]...
- Основні оксиди – Оксиди – Основні класи неорганічних сполук ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 7. Основні класи неорганічних сполук 7.1. Оксиди Оксиди – це бінарні сполуки елементів з Оксигеном, у яких він виявляє ступінь окислення -2. Характерні Ознаки оксидів: – ступінь окиснення Оксигену – -2; – атоми Оксигену не зв’язані між собою, а сполучаються лише з атомами […]...
- Тема 16. Оксиди – ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА ІІ ЗАВДАННЯ ДЛЯ ПЕРЕВІРКИ ЗНАНЬ ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК Тема 16. Оксиди Серед чотирьох наведених варіантів відповідей виберіть одну правильну 1. Вкажіть ряд речовин, в якому наведено лише кислотні оксиди: A. К2O, МgО, Fе2O3; Б. Аl2O3, SiO2, NO2; B. SO2, SO3, СO2; Г. N2O, СО, СаО. […]...
- Нітратна кислота – Елементи VA групи ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 9. Неметалічні елементи та їхні сполуки. Неметали 9.4. Елементи VA групи 9.4.6. Нітратна кислота Нітратна кислота HNO3 – одна з найважливіших неорганічних кислот. Зв’язки між атомами в молекулі кислоти полярні ковалентні. Нітроген у нітратній кислоті виявляє свою максимальну валентність – IV, а ступінь […]...
- Нітратна кислота – НІТРОГЕН. ФОСФОР Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЯ ЕЛЕМЕНТІВ НІТРОГЕН. ФОСФОР Нітратна кислота У молекулі нітратної кислоти HNО3 Нітроген перебуває в ступені окиснення +5, але при цьому проявляє валентність, що дорівнює 4. Будова молекули нітратної кислоти зображена нижче. Пунктиром показана валентність, розподілена між двома атомами Оксигену й атомом Нітрогену; отже, […]...
- ОКСИГЕН ЯК ХІМІЧНИЙ ЕЛЕМЕНТ. ОКСИДИ – КИСЕНЬ Хімія – універсальний довідник КИСЕНЬ ОКСИГЕН ЯК ХІМІЧНИЙ ЕЛЕМЕНТ. ОКСИДИ Хімічний символ Оксигену – О. Його відносна атомна маса 15,9994 ≈ 16. Елемент О знаходиться в VIA групі періодичної системи, отже, можливі його валентності – вища 6 і нижча 2. Але правіше від Оксигену в таблиці розташований лише один елемент F, а вище – жодного. […]...
- Оксиди Сульфуру – ОКСИГЕН. СУЛЬФУР Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЯ ЕЛЕМЕНТІВ ОКСИГЕН. СУЛЬФУР Оксиди Сульфуру Фізичні властивості оксидів Сульфуру Сульфур(ІV) оксид, або сульфур діоксид, або сірчистий ангідрид, – це безбарвний газ із характерним різким запахом. Саме він створює запах при згоранні сірників. При температурі -10 °С він скраплюється в безбарвну рідину, а […]...
- Оксиди, їх склад і назви. Класифікація оксидів Тема 2 ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК УРОК 12 Тема. Оксиди, їх склад і назви. Класифікація оксидів Цілі уроку: розширити знання про класифікацію неорганічних речовин на прикладі оксидів та їх класифікації за складом; ознайомити із сучасною науковою українською номенклатурою оксидів; формувати навички використання номенклатури на прикладі назв оксидів; розвивати навички учнів у складанні формул бінарних сполук […]...
- Солі карбонатної кислоти – ПІДГРУПА КАРБОНУ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина II. НЕОРГАНІЧНА ХІМІЯ Розділ 11. ПІДГРУПА КАРБОНУ § 11.4. Солі карбонатної кислоти Карбонатна кислота утворює два ряди солей: середні – карбонати і кислі – гідрокарбонати. Вони виявляють загальні властивості солей. Карбонати і гідрокарбонати лужних металів та амонію добре розчиняються у воді. Солі карбонатної кислоти – […]...
- Оксиди Сульфуру – Елементи VIA групи ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ 9. Неметалічні елементи та їхні сполуки. Неметали 9.3. Елементи VIA Групи 9.3.8. Оксиди Сульфуру Сульфур(ІV) оксид Сульфур утворює два оксиди – сульфур(ІV) оксид і сульфур(VІ) оксид. Найбільше значення серед сполук Сульфуру зі ступенем окиснення +4 має сульфур(ІV) оксид (сульфур діоксид, сірчистий газ) SO2. […]...