Поширення Феруму в природі. Використання заліза. Руйнування (іржавіння) заліза в природних умовах
Тема 2
ПРОСТІ РЕЧОВИНИ МЕТАЛИ Й НЕМЕТАЛИ
Урок 32
Тема. Поширення Феруму в природі. Використання заліза. Руйнування (іржавіння) заліза в природних умовах
Цілі: закріпити знання про фізичні та хімічні властивості заліза; ознайомити учнів з поширеністю Феруму в природі, використанням заліза; поглибити знання учнів про хімічні явища на прикладі іржавіння заліза; познайомити учнів зі способами захисту від корозії.
Тип уроку: засвоєння нових знань, умінь і навичок.
Форми роботи: самостійна робота з опорною схемою, групова робота
Обладнання: періодична система хімічних елементів, картки із завданнями.
ХІД УРОКУ
I. Організація класу
II. Актуалізація опорних знань
Фронтальна бесіда
– В якій групі періодичної системи знаходиться хімічний елемент Ферум? (VIII група, побічна підгрупа)
– До якого типу хімічних елементів належить Ферум? (До металів)
– Які фізичні властивості відрізняють метали від неметалів? (Металевий блиск, тепло – й електропровідність, ковкість, пластичність та ін.)
– Що таке сплави? (Це суміші металів)
– Які хімічні властивості заліза ми вивчили?
ІІІ. Засвоєння нових навичок знань
Учні об’єднуються в групи для спільного виконання завдання. Знайдіть у підручнику відповідь на запитання.
Група 1. Поширення заліза і Феруму в природі.
Група 2. Способи одержання заліза.
Група 3. Використання і значення заліза.
Група 4. Руйнування заліза в природних умовах.
Група 5. Способи захисту від корозії.
Після вивчення відповідного розділу підручника і консультації вчителя учні складають відповідь на запитання, представник кожної групи розповідає біля дошки про результати роботи групи. Учитель робить узагальнюючий висновок:
1. Залізо – один з найбільш поширених у природі елементів: за вмістом у земній корі – 4,7 % (масових). Зустрічається у вигляді оксидів і сульфідів, сконцентрованих у вигляді родовищ, придатних для промислової розробки.
Найважливіші руди:
– бурі залізняки (HFeO2 – nН2O), пірит FeS2;
– червоні залізняки (Fe2O3);
– магнітні залізняки (Fe3O4);
– шпатові залізняки (FeCO3).
Більшість із них жовто-бурі, коричневі, бурі й темно-червоні.
2. Одержують залізо з руди на металургійних заводах. Відновлюють з оксидів вугіллям, карбон(ІІ) оксидом або воднем. Запишемо рівняння реакції.
А) Fe3O4 + 2C 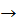 3Fe + 2CO2
3Fe + 2CO2
Б) Fe2O3 + 3CO 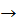 2Fe + 3CO2
2Fe + 3CO2
В) FeO + H2 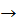 Fe + H2O
Fe + H2O
(Тип реакцій а), в) – заміщення: одна проста речовина заміщає в складній сполуці іншу.)
3. Широко використовується в техніці завдяки своїм властивостям і легкості одержання.
Має дуже важливе значення для людини. На частку заліза та його сплавів припадає близько 95 % усіх вироблених у світі металів. Але не тільки техніка має потребу в залізі. Без заліза не могло б існувати життя у звичній для нас формі: двовалентний Ферум міститься в гемоглобіні крові – речовині, що забезпечує насичення живих тканин киснем.
4. 3Fe + 4H2O 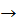 Fe3O4 + 4H2
Fe3O4 + 4H2
У вологому повітрі за звичайної температури залізо легко окислюється, вкриваючись рихлою іржею (її склад – Fe2O3 – nH2O). Унаслідок своєї пористості іржа не перешкоджає доступу кисню і вологи до металу, тому залізо руйнується. За деякими даними, у XIX столітті від корозії загинула половина всього виробленого заліза.
5. Корозія – хімічне або електрохімічне руйнування металів під впливом навколишнього середовища.
Сьогодні розроблено способи боротьби з корозією:
– покриття фарбою;
– нікелювання заліза;
– оцинковування заліза;
– покриття емаллю;
– покриття антикорозійними оліями та ін.
IV. Підбиття підсумків уроку
Тестова робота за варіантами
Варіант I
1. Хімічна формула простої речовини заліза:
А) Fe3;
Б) FeО;
В) Fe.
2. Формула ферум(ІІІ) оксиду:
А) Fe3O4;
Б) Fe2O3;
В) FeО.
3. Дано рівняння реакції: Fe+O2 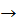 Fe3O4
Fe3O4
Сума коефіцієнтів у рівнянні:
А) 3;
Б) 9;
В) 6.
4. Масова частка Феруму у ферум(ІІ) оксиді:
А) 77,8 %;
Б) 70,0 %;
В) 79,4 %.
5. ___________________ використовується:
– у медицині;
– у техніці;
– у побуті тощо.
Варіант II
1. Хімічний символ елемента Ферум:
А) Ni;
Б) Fe;
В) Mg.
2. Формула ферум(ІІ) оксиду:
А) Fe3O4;
Б) Fe2O3;
В) FeО.
3. Дано рівняння реакції: Fe+O2 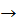 Fe2O3
Fe2O3
Сума коефіцієнтів у рівнянні:
А) 3;
Б) 6;
В) 9.
4. Масова частка Феруму у ферум(ІІІ) оксиді:
А) 77,8 %;
Б) 70,0 %;
В) 72,4 %.
5. ___________________ зустрічається в природі у вигляді:
– оксидів;
– простої речовини;
– сульфідів та ін.
Виставляємо оцінку за урок з урахуванням роботи в групах і тестів.
V. Домашнє завдання
Прочитати параграф про властивості заліза, відповісти на запитання.