Структурні формули
ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ
Частина І. ЗАГАЛЬНА ХІМІЯ
Розділ 3. ХІМІЧНИЙ ЗВ’ЯЗОК
§ 3.8. Структурні формули
Склад сполуки зображується у вигляді хімічних формул: емпіричних, електронних і структурних. Як приклад запишемо відповідні формули молекул водню, води, аміаку і метану.
Емпіричні формули: Н2 Н2O NH3 СН4
Електронні формули: 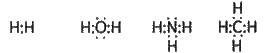
Структурні формули: 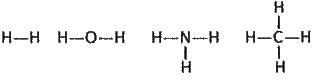
Емпіричні, або молекулярні, формули відбивають тільки якісний і кількісний склад молекул,
Електронні формули складаються із символів елементів, навколо яких точками позначають електрони зовнішнього рівня, а між атомами – зв’язуючі електронні пари. Вони показують порядок сполучення атомів у молекулі, а також природу хімічного зв’язку і механізм утворення молекули з атомів, а тому часто застосовуються для пояснення поведінки сполук у різних реакціях. Двома точками між атомами в електронних формулах позначають місця перекривання електронних хмар, а значить, і найбільшу густину зв’язуючої двохелектронної хмари.
Структурні електронні формули,
У перших кулі-атоми сполучені за допомогою стержнів, що символізують валентні зв’язки, у других пластилінові кулі вдавлені одна в одну, демонструючи заповнення простору молекули. Обидві моделі наочно передають форму молекули. Модель молекули метану, де карбон сполучений з чотирма однаковими атомами гідрогену, можна подати у вигляді тетраедра (правильного чотиригранника): у центрі його розміщений атом карбону, у вершинах – атоми гідрогену (див. рис. 3.11). Отже, чотири валентності карбону напрямлені у просторі до чотирьох вершин тетраедра. Ці напрямки зберігаються і під час утворення карбонових ланцюгів. Молекулу етану можна зобразити у вигляді фігури, що складається з Двох тетраедрів, сполучених вершинами (рис. 3.20), тощо.
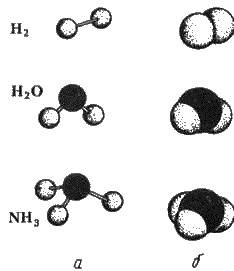
Рис. 3.19. Моделі молекули: а – кулестержневі; б – масштабні
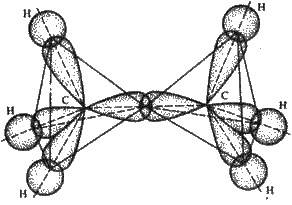
Рис. 3.20. Молекула етану
У хімії звичайно користуються структурними формулами, пам’ятаючи, що атоми мають просторове розміщення. Ці формули застосовують тільки для сполук з ковалентними зв’язками, що мають молекулярні кристалічні решітки. До останніх належать переважна більшість органічних сполук, багато кислот і деякі оксиди неметалів.