Головна ⇒ 📌ГДЗ з Хімії ⇒ Вправа 95-105
Вправа 95-105
№ 95.
Валентність – здатність атома сполучатися з певною кількістю таких самих або інших атомів.
Мінімальне значення – І.
Максимальне – VIII (за числом груп періодичної системи).
№ 96.
Стала валентність – К, Са, F, Н, Zn.
№ 97.
Р – максимальне значення V, Вr – VII, Hg – II, Se – VI.
№ 98.
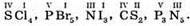
№ 99.
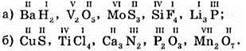
№ 100.
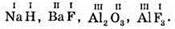
№ 101.
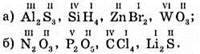
№ 102.
H2Se, HCl, AsH5.
№ 103.
A) Li2O; б) MgO; в) OsO2 або OsO4.
№ 104.
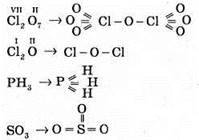
№ 105.
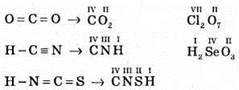
Related posts:
- ВИЗНАЧЕННЯ ВАЛЕНТНОСТІ ЕЛЕМЕНТІВ ЗА ФОРМУЛАМИ БІНАРНИХ СПОЛУК. ЗВ’ЯЗОК МІЖ РОЗМІЩЕННЯМ ЕЛЕМЕНТА У ПЕРІОДИЧНІЙ СИСТЕМІ ТА ЙОГО ВАЛЕНТНІСТЮ ДОСЛІДЖУЄМО НА УРОЦІ ТА ВДОМА У періодичній! системі максимальна величина валентності неметалічного хімічного елемента Карбону у бінарних сполуках з Оксигеном та Гідрогеном збігається: В) з номером групи. № 1. Щоб визначити валентність елемента за формулою бінарної сполуки, необхідно добуток величини валентності й індексу одного елемента поділити не індекс іншого. № 2. Значення постійної валентності у […]...
- Вправа 1 Вправа 1 1. Дано: Q = 0,2 мкКл = 2 ? 10-7 Кл Розв’язання: Сила, з якою електричне поле діє на заряджене тіло, дорівнює: Модуль цієї сили F = qE. Перевіримо одиниці фізичних величин: Підставимо числові значення: F = 8 ? 2 ? 10-7 = 16 ? І0-7 = 1,6 ? 10-6 (Н). Відповідь: поле […]...
- Вправа 19 Вправа 19 1. Дано: S = 100 см2 = = 10-2 м2 В = 1 Тл α = 0° ?t = 0,01 с Розв’язання: Зміна магнітного поля спричинить ЕРС індукції, яка за законом електромагнітної індукції дорівнює За формулою? ф = ?В? S? cos α. Початковий магнітний потік ф1= BS cos α. Після зникнення магнітного поля […]...
- Вправа 16 Вправа 16 І = 0,25 м B = 0,2 Тл = = 8 ?10 -3 Тл α = 30° εі -? 1. За правилом правої руки визначаємо напрямок Індукційного струму: Розв’язання: Оскільки провідник рухається рівномірно в однорідному Магнітному полі, то значення ЕРС індукції визначається за Формулою: εі = Blv sin α. Перевіримо одиниці фізичних величин: […]...
- Вправа 26 Вправа 26 1. Дано: С; λ1 Розв’язання: За формулою λ – v? Т, маємо λ1 – сТ, λ2 = vТ. Із маємо λ1 = 9λ2; λ1= 9 · vΤ. Отже, сТ = 9 · vΤ, звідси Відповідь: швидкість поширення зменшиться у 9 разів. 2. Дано λ = 500 м T = T V = 3000Гц […]...
- Вправа 20 Вправа 20 1. Дано: ε = 30 В Розв’язання: Згідно із законом ЕРС самоіндукції: Звідси Визначимо значення: Відповідь: індуктивність соленоїда 0,375 Гн. L – ? 2. Дано: L = 2 Гн ε= 20 В Розв’язання: Згідно із законом ЕРС самоіндукції: Звідси: Визначимо значення: Відповідь: швидкість зміни струму в обмотці електромагніту 3. Дано: ?І = 2А […]...
- Вправа 24 Вправа 24 1. Дано: V = 20 м/с Т = 0,5 с Розв’язання: Довжину хвилі можна визначити за формулою λ = v? T Обчислимо значення: λ = 20 м/с? 0,5 с = 10 м. Відповідь: довжина хвилі 10 м. λ – ? 2. Дано: λ = 300 м Т = 15 с V – ? […]...
- Вправа 25 Вправа 25 1. Дано: С = 2 пФ = = 2 ? 10-12Ф L = 0,5 мкГн = = 0,5 ? 10-6 Гн Розв’язання: За формулою обчислимо значення Періоду: Отже, Відповідь: частота коливань у контурі 160 МГц. V – ? 2. Дано: С = 1 мкФ = = 10-6 Ф U = 225 В L […]...
- Вправа 31 Вправа 31 1. Дано: λ1= 400 нм = = 4 · 10-7 м λ2 =760 нм = = 760 · 10-9 м С = З 108 м/с А = 6,626 · 10-34 Джс Розв’язання: Обчислимо значення: Відповідь: 5 ? 10-19 Дж; 2,6 · 10-19 Дж; 1,66 ? 10-27 кг(м/с); 8,7 ? 10-28 кг(м/с); 5,5 ? […]...
- Вправа 11 Вправа 11 1. Дано: С = 200 мкФ = 2 ? 10-4 Ф?φ = 1000 В Розв’язання: Енергія конденсатора визначається за формулою: Перевіримо одиниці фізичних величин: Підставимо числові значення: Відповідь: енергія конденсатора 100 Дж. W – ? 2. Дано: Q = 4,8 ? 10-3 Кл ?φ = 600 В Розв’язання: Енергія конденсатора визначається за формулою: […]...
- Вправа 5 Вправа 5 1. Дано: Q = 2мкКл = = 2 ? 10-6 Кл R = 3 м Розв’язання: Потенціал електричного поля точкового заряду дорівнює: Перевіримо одиниці фізичних величин: Підставимо числові значення: Відповідь: потенціал поля 6 кВ. φ-? 2. Дано: R = 30 м φ = 3000 В Розв’язання: Потенціал електричного поля точкового заряду Дорівнює: Звідси […]...
- Вправа 15 Вправа 15 1. Дано: V = 103 м/с Q = 2е Е – 1,6 ? 10 -6 Кл В = 0,2 Тл Розв’язання: Значення сили Лоренца визначається за формулою Fл= qvB. Оскільки q = 2е, то Fл = 2еvB. Перевіримо одиниці фізичних величин: Підставимо числові значення: Fл л = 2· 1,6 · ? 10 -19 […]...
- Вправа 9 Вправа 9 1. Дано: S = 15 см2 = = 15 · 10 -4 м2 D = 0,02 см = = 2 · 10-4 ε = 6 Розв’язання: Ємність плоского конденсатора визначається з формули Перевіримо одиниці фізичних величин: Підставимо числові значення: Відповідь: ємність конденсатора 400 пФ. C – ? 2. Дано: С = 1 мкФ […]...
- Вправа 18 Вправа 18 1. Дано: S = 40 см2 = = 4 · 10 -3 м2 В = 0,2 Тл Розв’язання: Магнітний потік, що проходить крізь поверхню, визначається за формулою Ф = BS. Перевіримо одиниці фізичних величин: [Ф] = Тл · м2 = Вб. Підставимо числові значення: Ф = 0,2 · 4 · 10 -3 = […]...
- Вправа 7 Вправа 7 1. Дано: φ = 6 ? 103 В Q = 3 ? 10-8 Кл Розв´язання: Відповідно до означення електроємність кульки Перевіримо одиниці фізичних величин: Підставимо числові значення: Відповідь: електроємність кульки 5 пФ. С – ? 2. Дано: φ = 30 В С = 150 пФ = = 150 ? 10-12 Ф Розв’язання: Відповідно […]...
- Вправа 14 Вправа 14 1. Дано: L = 0,5 м α = 90° В = 2 ? 10 -62 Тл FA = 0,15 Н Два паралельні провідники, якими йде струм одного напряму, притягуються під дією сили Ампера. На два паралельні пучки електронів також діє сила Ампера, але вона менша за кулонівську силу відштовхування, тобто FA < Fкул. […]...
- Вправа 13 Вправа 13 1. Дано: R = 10 см = 0,1 м І = 600 А Розв’язання: Магнітна індукція поля прямого провідника обчислюється за формулою Перевіримо одиниці фізичних величин: Підставимо числові значення: Відповідь: магнітна індукція поля 1,2 мТл. В – ? 2. Дано: R = 10 см = 1 м В = 4 ? 10 -6 […]...
- Вправа 6 Вправа 6 1. Дано: Q = 0,012 Кл А = 0,36 Дж Розв’язання: Різниця потенціалів між двома точками електричного поля: Перевіримо одиниці фізичних величин: Підставимо числові значення: Відповідь: різниця потенціалів 30 В. ?φ – ? 2. Дано: Q = 4,6 ? 10 6 Кл ?φ = 2000 В Розв’язання: Різниця потенціалів між двома точками електричного […]...
- Вправа 106-114 № 106. Відносна молекулярна маса – це відношення маси молекули до 1/12 маси атома Карбону. Її позначають Мr. Її розраховують за хімічною формулою (б). Маса дорівнює сумі відносних мас атомів, які містяться в молекулі. № 107. Найменшу відносну масу має речовина водень: Мr(Н2) = 2 • Аr(Н) = 2 • 1 = 2. № 108. […]...
- Вправа 12 Вправа 12 1. Дано: ε – 12 В /=2А, U = 10 В Розв’язання: Згідно із законом Ома для ділянки кола: Звідси Згідно із законом Ома для повного кола: Звідси Перевіримо одиниці фізичних величин: Підставимо числові значення: Відповідь: внутрішній опір джерела 1 Ом, опір навантаження 5 Ом. R – ? R – ? 2. Дано: […]...
- Вправа 139-145 № 139. Хімічне рівняння – це запис хімічної реакції за допомогою формул реагентів і продуктів, який відповідає закону збереження маси речовин. № 140. № 141. № 142. № 143. № 144. № 145. Дано: Розв’язання 1. Запишемо рівняння реакції: Згідно із законом збереження маси речовин під час хімічної реакції, маса речовин, що вступила в реакцію, […]...
- Вправа 215-220 № 215. Ланки колообігу води в природі: – випаровування; – конденсація; – дощові опади; – участь у фотосинтезі; – поглинання коренями рослин з грунту. № 216. Технологічні процеси неможливі без води. Вода є: – розчинником; – теплоносієм; – охолоджувачем. № 218. № 219. № 220. Дано: Розв’язання 1. m(С) = 1 т = 1000 кг […]...
- Вправа 73-82 № 73. Проста речовина – речовина, утворена одним хімічним елементом. Сірка, цинк, мідь, графіт. № 74. Прості речовини: метали і неметали. № 75. Б). № 76. Фізичні властивості металів: – твердість; – електропровідність; – теплопровідність; – висока температура плавлення; – пластичність, ковкість. № 77. А) азот; б) азоту, Нітрогену; в) Нітрогену; г) азот. № 78. […]...
- Вправа 205-210 № 205. Гідроксиди – сполуки металічних елементів із загальною формулою М(ОН)n (М – металічний елемент). Основи – це гідроксиди Натрію, Калію, Барію, кальцію, інших металічних елементів. Луги – це розчинні у воді основи. № 206. № 207. № 208. Відповідь: a) 56,3 %; б) 65,3 %. № 209. Дано: Розв’язання 1. Обчислимо масу NaOH: (бо […]...
- Вправа 57-64 № 57. Хімічний елемент – вид атомів із певним зарядом ядра. Хімічний елемент – не атом і не речовина. Він не має агрегатного стану, густини, інших фізичних властивостей. № 58. Короткий варіант – має 7 груп, 11 рядів; – має 8 періодів. Довгий варіант – має 7 груп, 7 рядів; – має 18 періодів (Іа, […]...
- Вправа 8 Вправа 8 1. Дано: U =1,5 В Q = 30 нКл = = 3 · 10-8 Кл Розв’язання: Ємність конденсатора дорівнює Перевіримо одиниці фізичних величин: Підставимо числові значення: Відповідь: ємність конденсатора 20 нФ. С – ? 2. Дано: Δφ = 1000 В С = 3 мкФ = = 3 · 10-6 Ф Розв’язання: Ємність конденсатора […]...
- Вправа 195-204 № 195. Відповідь: m(р. р.) = 6 г. № 196. Дано: Розв’язання 1. Обчислимо m розчину: 2. Обчислимо масову частку розчиненої речовини: Відповідь: ω(цукру) = 0,2 або 20 %. № 197. M (р-ну), г M (р. р.), г M (води), г ω(р. р.) 400 8 392 0,02 або 2 % 500 40 460 0,08 або […]...
- Вправа 46-55 № 46. 1-А, 2-В, 3-Б, А, 4-В. № 47. Фільтруванням – б), г. Б) мідні ошурки; Г) шматочки пластмаси. № 48. Фільтрування – суміш пропускають через фільтр, а часточки твердої речовини затримуються фільтром. № 50. А) Суміш кухонної солі та крейди треба розчинити у воді, сіль розчиниться у воді, а крейда – ні. Фільтруванням можна […]...
- Вправа 115-124 № 115. Масова частка елемента у сполуці обчислюється, якщо відомі маса елемента і відповідна маса сполуки (а). Масова частка елемента – це відношення маси елемента до відповідної маси сполуки. Її виражають або у% , або частках від 1. № 116. Масова частка елемента у простій речовині дорівнює 1. Тому що проста речовина утворена одним хімічним […]...
- Вправа 156-164 № 156. Реакції сполучення Реакції розкладу 1. Беруть участь кілька речовин 1. Бере участь одна речовина 2. Утворюється одна речовина 2. Утворюється кілька інших речовин Приклади № 157. Формули оксидів: Н2O, І2O5, ВаО. № 158. 1) – в – ферум(ІІ) оксид 2) – а – ферум(ІІІ) оксид 3) – б – ферум(II, III) оксид № […]...