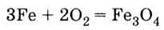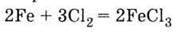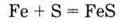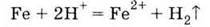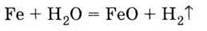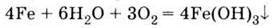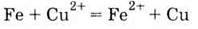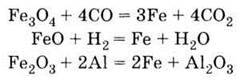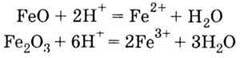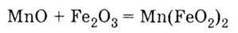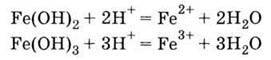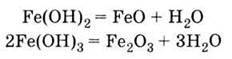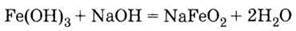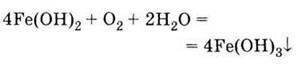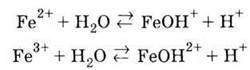ЗАЛІЗО І ЙОГО СПОЛУКИ – ХІМІЯ МЕТАЛІЧНИХ ЕЛЕМЕНТІВ
Хімія – універсальний довідник
ХІМІЯ МЕТАЛІЧНИХ ЕЛЕМЕНТІВ
ЗАЛІЗО І ЙОГО СПОЛУКИ
Проста речовина залізо – метал з усіма характерними для металічного стану властивостями: високими тепло – і електропровідністю, ковкістю, “металічним” блиском та ін.; здатний утворювати сплави з іншими металами, а також, що дуже важливо на практиці, і з вуглецем. Від більшості інших металів залізо відрізняється здатністю намагнічуватися; воно володіє так званим феромагнетизмом.
Залізо – тугоплавкий метал (tлл = 1540 °С), і в цьому його
Зазвичай Ферум проявляє валентності +2 і +3, утворюючи два ряди сполук – Феруму (II) (“закисного”) і Феруму (III) (“окисного”): FеО і Fе2O3, Fе(ОН)2 і Fе(ОН)3, FеSO4 і Fе2(SO4)3 і т. д.
Під час взаємодії з кислотами утворюються солі
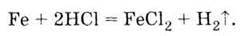
Додаючи до розчину солі феруму (II) розчин лугу, отримаємо гідроксид феруму:
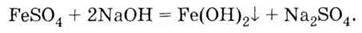
Гідроксид феруму (II) Fе(ОН)2 – основа, відповідний їй оксид FеО має основний характер.
Стосовно окиснювачів, у тому числі кисню повітря, сполуки феруму (II) нестійкі. Вони окислюються і переходять у сполуки феруму (III), наприклад:
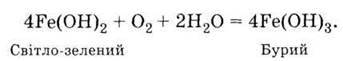
Оксид і гідроксид феруму (III) виявляють у більшості реакцій основні властивості. Але відповідно до сказаного у попередньому параграфі про кислотно-основні властивості оксидів і гідроксидів елементів у різних станах валентності Fе2O3 і Fе(ОН)3 повинні володіти амфотерністю, тобто, крім основних властивостей, проявляти і кислотні.
Отже, при взаємодії оксиду феруму (III) з основними оксидами у твердому стані при високих температурах (-1000 °С) утворюються солі, що відповідають кислоті НFеO2. Ці солі називаються феритами. Наприклад, у процесі виробництва цементу, крім основних продуктів – силікатів і алюмінатів, утворюється і ферит кальцію:
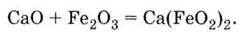
Феритом феруму (II) є і залізна окалина Fе3O4, або Fе(FеO2)2, яка утворюється при високотемпературному окисненні заліза.
Залізо може витісняти водень не тільки з кислот, але і з води, однак лише під час сильного нагрівання:
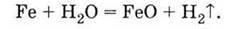
За звичайних умов вода не діє на залізо. Однак, у присутності кисню реакція проходить:
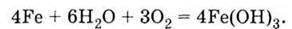
Утворюється гідроксид феруму (III) – основна складова частина іржі. Для протікання реакції необхідний одночасний вплив на залізо і води, і кисню. У протилежному випадку корозія практично відсутня.
Хімічні властивості заліза і його сполук подано у таблиці.
Таблиця
Залізо і його сполуки
Залізо | Сполуки Феруму | |
Оксиди феруму (II) і (III) | Гідроксиди феруму (II) і (III) | |
1. Сріблясто-білий метал 2. Взаємодіє з простими речовинами: А) горить у кисні
Б) реагує з хлором
З) взаємодіє з сіркою
3. Реагує з розчинами кислот:
4. Витісняє водень із води при сильному нагріванні:
5. Окислюється в присутності води і кисню повітря (з утворенням іржі):
6. Заміщає менш активний метал в розчині його солі:
Одержання Відновлення оксидів феруму оксидом карбону (II), воднем або алюмінієм:
| 1. Проявляють основні властивості, взаємодіючи з кислотами:
2. Оксид феруму (III) проявляє слабкі амфотерні властивості, взаємодіючи при нагріванні з основними оксидами з утворенням феритів:
| 1. Проявляють властивості нерозчинних у воді основ:
Розкладаються при нагріванні:
2. Гідроксид феруму (III) проявляє слабкі амфотерні властивості, реагуючи з гарячими конц. розчинами лугів:
3. Гідроксид феруму (II) на повітрі окислюється в гідроксид феруму (III):
4. Солі феруму (II) і (III) гідролізуються:
|