Бензол та його гомологи
ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ
Частина III. ОРГАНІЧНА ХІМІЯ
Розділ 16. ВУГЛЕВОДНІ
§ 16.12. Бензол та його гомологи
Властивості. Бензол – безбарвна, летка, вогненебезпечна рідина з характерним запахом. У воді практично не розчиняється. Горить дуже кіптявим полум’ям. Пара бензолу з повітрям утворює вибухову суміш. Рідкий бензол і пара бен золу отруйні. За звичайних умов більшість ароматичних вуглеводнів також являють собою безбарвні рідини, нерозчинні у воді, з характерним запахом.
За хімічними
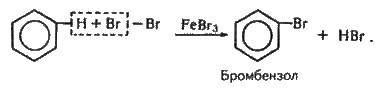
Бромбензол – безбарвна рідина, не розчинна у воді. При іншому каталізаторі можна всі атоми гідрогену у бензолі замістити галогеном. Це відбувається, наприклад, коли пропускати
АlСl3
С6Н6 + 6Сl2 >С6l6 + 6НСl.
Гексахлорбензол
Гексахлорбензол – безбарвна кристалічна речовина, застосовується для протруювання насіння і консервування деревини.
Якщо на бензол діяти сумішшю концентрованих азотної і сірчаної кислот (нітруючою сумішшю), то атом гідрогену заміщується нітрогрупою – NO2:
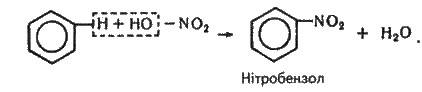
Це реакція нітрування бензолу. Нітробензол – блідо-жовта масляниста рідина із запахом мигдалю, не розчинна у воді, застосовується як розчинник, а також для добування аніліну.
У молекулі бензолу можна замістити атом гідрогену на алкільний радикал дією галогенопохідних вуглеводнів за наявності хлориду алюмінію:
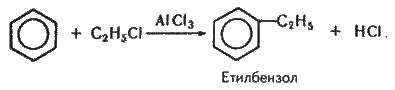
Реакції приєднання до бензолу проходять важко. Щоб вони відбулися, потрібні особливі умови: підвищення температури і тиску, підбір каталізатора, світлове опромінювання та ін. Так, з каталізатором – нікелем чи платиною – бензол гідрогенізується, тобто приєднує гідроген, утворюючи циклогексан:
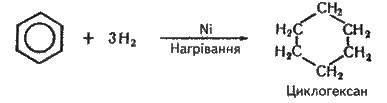
Циклогексан – безбарвна летка рідина із запахом бензину, у воді не розчиняється.
При ультрафіолетовому опромінюванні бензол приєднує хлор:
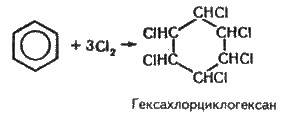
Гексахлорциклогексан, або гексахлоран, – кристалічна речовина, застосовується як сильний засіб для знищення комах.
Бензол не приєднує галогеноводнів і води. Бензол дуже стійкий до дії окисників. На відміну від ненасичених вуглеводнів він не знебарвлює бромної води і розчину КМnO4. За звичайних умов бензольне кільце не руйнується і під дією багатьох інших окисників. Однак гомологи бензолу окиснюються легше, ніж насичені вуглеводні. При цьому окиснюються лише радикали, зв’язані з бензольним ядром:
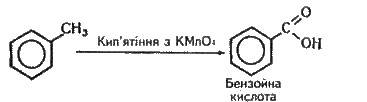
Таким чином, ароматичні вуглеводні можуть вступати як в реакції заміщення, так і в реакції приєднання, однак умови цих перетворень значно відрізняються від умов аналогічних перетворень насичених і ненасичених вуглеводнів.
Добування. Бензол і його гомологи у великих кількостях добувають з нафти і кам’яновугільної смоли, що утворюється під час сухої перегонки кам’яного вугілля (коксування). Суха перегонка провадиться на коксохімічних і газових заводах.
Реакція перетворення циклогексану на бензол (дегідрування, або дегідрогенізація) проходить при пропусканні його над каталізатором (платиновою черню) при 300 °С (§ 16.4). Насичені вуглеводні реакцією дегідрування також можна перетворювати на ароматичні. Наприклад:
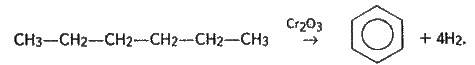
Реакції дегідрування дають змогу використовувати нафтові вуглеводні для добування вуглеводнів ряду бензолу. Вони вказують на зв’язок між різними групами вуглеводнів та їх взаємне перетворення.
За способом М. Д. Зелінського і Б. О. Казанського бензол можна добути, пропускаючи ацетилен крізь нагріту до 600 °С трубку з активованим вугіллям. Весь процес полімеризації трьох молекул ацетилену можна зобразити схемою:
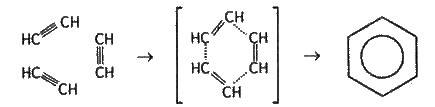
Застосування. Бензол і його гомологи застосовуються як хімічна сировина для виробництва ліків, пластмас, барвників, отрутохімікатів та багатьох інших органічних речовин. Широко використовують їх як розчинники. Бензол як добавка поліпшує якість моторного палива.