Фосфор – ПІДГРУПА НІТРОГЕНУ
ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ
Частина II. НЕОРГАНІЧНА ХІМІЯ
Розділ 10. ПІДГРУПА НІТРОГЕНУ
§ 10.10. Фосфор
Фосфор – аналог нітрогену, оскільки електронна конфігурація його валентних електронів, як і у нітрогену, s2p3. Однак порівняно з атомом нітрогену атом фосфору має меншу енергію іонізації і більший радіус (див. п. З та п. 6, табл. 10.1). Це означає, що неметалічні ознаки у фосфору виражені слабкіше, ніж у нітрогену. Тому для фосфору рідше буває ступінь окиснення – З і частіше +5. Мало характерні й інші
Поширення у природі. Загальний вміст фосфору в земній корі становить 0,08 %. У природі фосфор трапляється лише у вигляді сполук; найважливіша з них – фосфат кальцію – мінерал апатит. Відомо багато різновидів апатиту, з яких найбільш поширений фторапатит ЗСа3(РO4)2 ∙ CaF2. З різновидів апатиту складаються осадові гірські породи – фосфорити. Фосфор входить також до складу білкових речовин у вигляді різних сполук. Вміст фосфору у тканинах мозку становить 0,38 %, у м’язах – 0,27 %.
Найбагатші у світі поклади апатитів розташовані поблизу м. Кіровська на Кольському півострові.
Фосфор необхідний для життя рослин. Тому у грунті завжди має бути достатня кількість сполук фосфору.
Фізичні властивості. Зменшення неметалічності елемента фосфору порівняно з нітрогеном позначається на властивостях його простих речовин. Так, фосфор на відміну від азоту має кілька алотропічних модифікацій: білий, червоний, чорний тощо.
Білий фосфор – безбарвна і дуже отруйна речовина. Добувають конденсацією пари фосфору. Не розчиняється у воді, але добре розчиняється у сірковуглеці. За тривалого слабкого нагрівання білий фосфор переходить у червоний.
Червоний фосфор – порошок червоно-бурого кольору, не отруйний. Не розчиняється у воді й сірковуглеці. Встановлено, що червоний фосфор являє собою суміш кількох алотропічних модифікацій, які відрізняються одна від одної за кольором (від червоного до фіолетового) та деякими іншими властивостями. Властивості червоного фосфору багато в чому залежать від умов його добування.
Чорний фосфор за зовнішнім виглядом схожий на графіт, масний на дотик, має властивості напівпровідників. Добувають тривалим нагріванням білого фосфору під великим тиском (200 °С і 1 200 МПа).
Червоний і чорний фосфор при сильному нагріванні сублімуються.
Природний фосфор складається з одного стабільного ізотопу 3115 Р. Широко застосовується штучний радіоактивний ізотоп 3215Р (період напіврозпаду 14,3 доби).
Властивості алотропічних модифікацій – фосфору пояснюються їх будовою. Детальніше вивчено будову білого фосфору. Він має молекулярну кристалічну решітку. Його молекули чотириатомні (Р4 – тетрафосфор) і мають форму правильної тригранної піраміди

Кожний атом фосфору розташований в одній з вершин піраміди і зв’язаний трьома о-зв’язками з іншими трьома атомами. Як усі речовини з молекулярною решіткою, білий фосфор легко плавиться і леткий. Він добре розчиняється в органічних розчинниках.
На відміну від білого фосфору червоний і чорний фосфори мають атомну кристалічну решітку. Тому вони нерозчинні майже у всіх розчинниках, але леткі і, як уже зазначалося, не отруйні.
Хімічні властивості. У хімічному відношенні білий фосфор дуже відрізняється від червоного. Так, білий фосфор легко окиснюється і самозаймається на повітрі, тому його зберігають під водою. Червоний фосфор не загоряється на повітрі, але загоряється при нагріванні понад 240 °С. При окисненні білий фосфор світиться в темряві – відбувається безпосереднє перетворення хімічної енергії на світлову.
У рідкому і розчиненому стані, а також у парі при температурі нижчій за 800 °С фосфор складається з молекул Р4. При нагріванні понад 800 °С молекули дисоціюють: Р4 ⇆ 2Р2. Останні при температурі понад 2 000°С розкладаються на атоми: Р2 ⇆ 2Р. Атоми фосфору можуть об’єднуватися в молекули Р2, Р4 і в полімерні речовини. Очевидно, молекула Р4, де атоми сполучені між собою трьома σ-зв’язками, міцніша за молекулу Р2, в якій атоми сполучені одним σ- і двома п – зв’язками. Вже за звичайної температури молекула Р2 нестійка (стійкість же N2 за цих умов слід пояснити дуже малими розмірами атома, див. п. 6, табл. 10.1).
Фосфор сполучається з багатьма простими речовинами – киснем, галогенами, сіркою та деякими металами, виявляючи окисні та відновні властивості. Наприклад:
2Р + 3S = P2S3; 2Р + ЗСа = С3Р2;
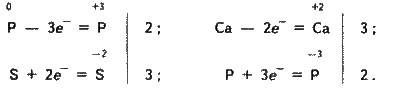
Реакції з білим фосфором відбуваються легше, ніж з червоним.
Сполуки фосфору з металами називаються фосфідами. Вони легко розкладаються водою з утворенням фосфіну РН3
– дуже отруйного газу із запахом часнику:
Са3Р2 + 6Н2О = ЗСа(ОН)2 + 2РН3 ↑.
За аналогією з NH3 фосфін здатний до реакції приєднання:
РН3 + Нl = РН4l.
Добування і застосування. Фосфор добувають з апатитів або фосфоритів. Останні змішують з вугіллям (коксом) та піском і прожарюють в електричній печі при 1 500 °С:
+5 0 0 +2
2Са3(РO4)2 + 10С + 6SiO2 = бСаSіО3 + Р4 + 10СО;
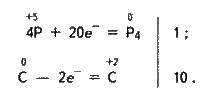
Під час реакції пару фосфору згущують і вловлюють у приймачі з водою.
Червоний фосфор застосовують у виробництві сірників. З червоного фосфору, сульфіду стибію(ІІІ), залізного сурику (природного оксиду феруму(ІІІ) з домішкою кварцу) та клею виготовляють суміш, яку наносять на бічні поверхні сірникової коробки. Головки сірників складаються головним чином з бертолетової солі, молотого скла, сульфуру та клею. Під час тертя головки по намазці сірникової коробки червоний фосфор займається, підпалює склад головки, а від нього загоряється дерево.
Білий фосфор широкого застосування не має. Звичайно його використовують для утворення димових завіс. Чорний фосфор застосовується дуже рідко.