Хімічні властивості простих речовин – НІТРОГЕН. ФОСФОР
Хімія підготовка до ЗНО та ДПА
Комплексне видання
ЧАСТИНА І
ЗАГАЛЬНА ХІМІЯ
ХІМІЯ ЕЛЕМЕНТІВ
НІТРОГЕН. ФОСФОР
Хімічні властивості простих речовин
Хімічні властивості азоту
Азот являє собою дуже стійку інертну сполуку. Атоми Нітрогену зв’язані в молекулу потрійним зв’язком: одним σ-зв’язком і двома π-зв’язками. Для руйнування такої молекули на атоми необхідно затратити величезну кількість енергії. Наприклад, при 3000 °С дисоціація молекули на атоми відбувається не більш ніж на 0,5%. За рахунок високої
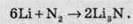
При нагріванні азот взаємодіє з деякими металами та неметалами, при цьому утворюються нітриди, сполуки, в яких Нітроген проявляє ступінь окиснення -3:
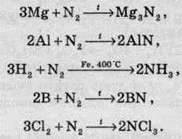
В електричному розряді азот реагує з киснем, при цьому утворюються оксиди Нітрогену II та IV. За рахунок цього під час грози повітря, а згодом і грунт, збагачується складними сполуками Нітрогену:

Реакції зі складними сполуками для азоту не характерні,
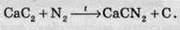
Хімічні властивості фосфору
Хімічні властивості всіх алотропних модифікацій фосфору однакові, за винятком того, що білий фосфор активніший, ніж червоний, а червоний активніший, ніж чорний. Таким чином, речовину фосфор при складанні хімічних реакцій будемо записувати просто як Р. Червоний і чорний фосфор реагують із киснем повітря при підвищеній температурі, а білий – навіть при кімнатній температурі:

Білий фосфор при повільному окисненні киснем повітря випромінює світло. Це відбувається внаслідок того, що в процесі окиснення енергія, яка виділяється, витрачається на випромінювання світла. Це явище називають хемілюмінесценцією.
Фосфор реагує з деякими неметалами-окисниками, при цьому можуть утворюватися похідні Фосфору з різним ступенем окиснення. Це залежить від кількості речовини-окисника. При надлишку окисника утворюються сполуки Фосфору(V), а при нестачі – Фосфору(ІІІ):
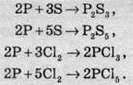
Фосфор вступає у взаємодію з багатьма активними металами. При цьому утворюються фосфіди металів. Фосфіди – це сполуки, в яких атом Фосфору виявляє ступінь окиснення -3:
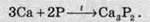
З воднем пряма реакція не проходить, тому фосфін (РН3) добувають непрямими методами з фосфідів:
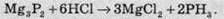
Фосфін – це дуже нестійка сполука, на повітрі вона самозаймається:
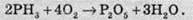
Фосфін утворюється при гнитті на болотах та цвинтарях, саме тому багато людей вважають процес самозаймання фосфіну виходом душі людини з тіла.
Оскільки білий фосфор може самозайматися на повітрі, його залишки необхідно утилізувати, задля того аби уникнути пожежі. Відходи фосфору знищують за допомогою розчину купрум(ІІ) сульфату:
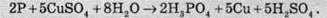
У результаті цієї реакції шматочки білого фосфору покриваються плівкою металічної міді, й окиснення фосфору стає неможливим.
