Іонний добуток води – Протолітична рівновага
КИСЛОТИ Й ОСНОВИ
2. Протолітична рівновага
Рівновага, яка виникає в процесі протолізу, залежить від температури, хімічної природи реагентів і зміщується в бік утворення стійкіших сполук.
2.1. Іонний добуток води
Молекула води, згідно теорії Бренстеда, може виступати як кислота або як основа. І навіть у чистій воді відбувається так званий автопротоліз (грец. autos – сам):
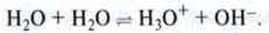
Проте рівновага майже повністю зміщена в бік початкової речовини:
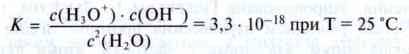
Концентрація с(Н2О) недисоційованих молекул води порівняно з концентраціями с(Н3О+) і с(ОН-) настільки велика, що її можна об’єднати з константою рівноваги К і отримати нову константу КW.
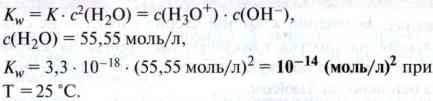
Константу KW називають іонним добутком води.
У чистій воді присутня рівна кількість іонів гідроксонію і гідроксид-іонів: с(Н3О+) = с(ОН-).
Звідси при 25 °С:
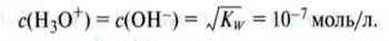
Related posts:
- Водневий показник – Протолітична рівновага КИСЛОТИ Й ОСНОВИ 2. Протолітична рівновага 2.2. Водневий показник У водних розчинах електролітів (кислот, основ) іонний добуток води залишається практично незмінним, поки їх концентрація не стане дуже великою. Отже, якщо концентрація с(Н3О+) у розчині більша, ніж у чистій воді, то с(ОН-) повинна бути менша, і навпаки. Приклад. Рівновага НСl + Н2O Н3O+ + Сl – […]...
- Дія буферів – Буферні розчини – Протолітична рівновага КИСЛОТИ Й ОСНОВИ 2. Протолітична рівновага 2.5. Буферні розчини Дія буферів Використовуючи константу рівноваги процесу дисоціації кислоти, можна показати дію буфера: – Додавання кислоти, тобто збільшення с(Н3О+). Для збереження рівноваги додані іони гідроксонію реагуватимуть з відповідними іонами А-, утворюючи недисоційовану НА, практично не змінюючи концентрацію іонів гідроксонію. – Додавання лугу, тобто збільшення с(ОН-). Додані гідроксид-іони […]...
- Водневий показник розчинів слабких кислот і основ – Сила кислот і основ – Протолітична рівновага КИСЛОТИ Й ОСНОВИ 2. Протолітична рівновага 2.3. Сила кислот і основ Водневий показник розчинів слабких кислот і основ Оскільки при протолізі кислоти чи основи утворюється рівна кількість позитивних і негативних іонів, їхня концентрація буде однаковою: Якщо в даних рівняннях прологарифмувати значення концентрацій іонів (Н3О+) і (ОН-), то одержимо значення pH розчину кислоти або значення рОН […]...
- ІОНІЗАЦІЯ ВОДИ. ІОННИЙ ДОБУТОК ВОДИ. КОНСТАНТА ІОНІЗАЦІЇ ВОДИ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ХІМІЧНА РІВНОВАГА ІОНІЗАЦІЯ ВОДИ. ІОННИЙ ДОБУТОК ВОДИ. КОНСТАНТА ІОНІЗАЦІЇ ВОДИ Іонний добуток води: Водневий показник Нейтральне середовище: Кисле середовище: Лужне середовище: Нижче наведена шкала взаємозв’язку pH і...
- Добуток розчинності – Рівновага розчинності ХІМІЧНА РІВНОВАГА 3. Рівновага розчинності 3.2 . Добуток розчинності Якщо до насиченого розчину солі у воді ще додати цю ж сіль, то ця добавка випаде в нерозчинений осад. Якщо до нього додати сіль, що містить один з іонів розчиненої солі, то утвориться такий самий осад. Приклад. Якщо до насиченого розчину кальцій сульфату додати трохи кальцій […]...
- Слабкі кислоти й основи – Сила кислот і основ – Протолітична рівновага КИСЛОТИ Й ОСНОВИ 2. Протолітична рівновага 2.3. Сила кислот і основ Слабкі кислоти й основи У слабких кислот і основ дисоціація є неповною. Внаслідок цього в розчині є недисоційовані молекули. Тому показник pH неможливо розрахувати лише з концентрації кислоти або основи. Додатково потрібна інформація про стан протолітичної рівноваги: Оскільки в цьому випадку концентрація молекул води […]...
- Значення pH буферів – Буферні розчини – Протолітична рівновага КИСЛОТИ Й ОСНОВИ 2. Протолітична рівновага 2.5. Буферні розчини Суміш слабкої кислоти і зв’язаної основи, або слабкої основи і її зв’язаної кислоти характеризується тим, що її водневий показник при додаванні не дуже великої кількості іонів гідроксонію або гідроксид-іонів практично не змінюється. Розчини, показник pH яких по відношенню до кислот і лугів залишається стабільним, називають буферними […]...
- Сильні кислоти й основи – Сила кислот і основ – Протолітична рівновага КИСЛОТИ Й ОСНОВИ 2. Протолітична рівновага 2.3. Сила кислот і основ Силу кислоти або основи, за Бренстедом, визначають здатністю до протолізу, що залежить від того, як сильно виражена готовність речовини віддавати або приймати протони. Реагент визначає, яку функцію – кислоти чи основи – виконує речовина в реакції. У цьому випадку важливим реагентом є вода, оскільки […]...
- Водневий показник розчинів солей – Протолітична рівновага КИСЛОТИ Й ОСНОВИ 2. Протолітична рівновага 2.4. Водневий показник розчинів солей Багато сольових розчинів мають нейтральне середовище, деякі – кисле або лужне. За Бренстедом, вода при цьому виконує функцію основи або кислоти. Приклад. Натрій хлорид Іон Na+: не вступає в реакцію з водою. Іон Сl-: надзвичайно слабка основа, тому протоліз не відбувається. Розчин натрій хлориду […]...
- Залежність розчинності від температури – Рівновага розчинності ХІМІЧНА РІВНОВАГА 3. Рівновага розчинності Багато іонних речовин – наприклад, кухонна сіль – добре розчиняються у воді. Розчинність цих речовин однак обмежена: починаючи з певної кількості, речовина більше не може розчинятися, залишаючись у нерозчиненому стані в насиченому розчині. Увага: частка речовини в насиченому розчині, тобто її концентрація, не залежить від кількості нерозчиненого осаду. 3.1. Залежність […]...
- ЕЛЕКТРОЛІЗ ВОДИ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС РЕАКЦІЇ ЗІ ЗМІНОЮ СТУПЕНІВ ОКИСНЕННЯ ЕЛЕМЕНТІВ ЕЛЕКТРОЛІЗ ВОДИ Електроліз води – окисно-відновний процес розкладу води з утворенням водню і кисню. На катоді відбувається відновлення води з утворенням іонів ОН – і молекул Н2: На аноді здійснюється окиснення води з утворенням молекул О2 і іонів Н+: Дія електричного струму призводить […]...
- Стан рівноваги – Константа рівноваги – Характеристики хімічної рівноваги ХІМІЧНА РІВНОВАГА 1. Характеристики хімічної рівноваги 1.2 . Константа рівноваги У ході реакції рівноваги первинна концентрація початкових речовин постійно зменшується. Внаслідок цього знижується і швидкість прямої реакції. Одночасно постійно підвищується концентрація продуктів реакції. Внаслідок цього підвищується швидкість зворотної реакції. Для бімолекулярної реакції типу можна скласти наступні вирази швидкості прямої та зворотної реакції: Коли швидкості обох […]...
- Хімічна рівновага ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 4. ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ. § 4.6. Хімічна рівновага Оборотні реакції не доходять до кінця і завершуються встановленням хімічної рівноваги. Наприклад, у реакції синтезу аміаку (див. § 10.4) рівновага настає тоді, коли за одиницю часу утворюється стільки само молекул аміаку, скільки їх […]...
- Хімічна рівновага – Хімічні реакції Хімія Загальна хімія Хімічні реакції Хімічна рівновага Хімічні реакції, які за одних і тих самих умов можуть іти в протилежних напрямах, називаються оборотнимИ. У випадку, якщо за даних умов реагенти повністю перетворюються на продукти реакції, реакції називаються НеоборотнимИ. Умови необоротності хімічних реакцій 1) Продукти, що утворюються, виводяться зі сфери реакції – випадають у вигляді осаду, […]...
- Дисоціація води – РОЗЧИНИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 5. РОЗЧИНИ. ТЕОРІЯ ЕЛЕКТРОЛІТИЧНОЇ ДИСОЦІАЦІЇ § 5.12. Дисоціація води. pH Водa і як слабкий електроліт незначною мірою дисоціює на іони Н+ і ОН-, що перебувають у рівновазі з недисоційованими молекулами: Н2O ⇆ Н+ + ОН-. Концентрацію іонів звичайно виражають у молях […]...
- ІОННИЙ І КОВАЛЕНТНИЙ ЗВ’ЯЗОК Хімія – універсальний довідник ВІД НАТРІЮ ДО АРГОНУ ІОННИЙ І КОВАЛЕНТНИЙ ЗВ’ЯЗОК Атоми того самого елемента притягують до себе електрони однаково, тому електрони на зв’язучій молекулярній орбіталі між однаковими атомами (у простих речовинах), можна сказати, однаковою мірою належать обом атомам. У цьому випадку кажуть про ковалентний зв’язок. Різні атоми притягують електрони з різною силою, тому […]...
- Іонний зв’язок Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЧНИЙ ЗВ’ЯЗОК І БУДОВА РЕЧОВИНИ Іонний зв’язок Утворення іонного зв’язку Іонний зв’язок за механізмом утворення нагадує ковалентний, але має принципову відмінність: у речовинах з іонним зв’язком атоми жорстко не з’єднуються один з одним, а просто притягуються електростатичними взаємодіями. Атоми лужних металів, наприклад Натрію, […]...
- ПРОБЛЕМА ЧИСТОЇ ВОДИ. ОХОРОНА ВОДОЙМ ВІД ЗАБРУДНЕННЯ. ОЧИЩЕННЯ ВОДИ НА ВОДООЧИСНИХ СТАНЦІЯХ ТА В ДОМАШНІХ УМОВАХ ДОСЛІДЖУЄМО НА УРОЦІ ТА ВДОМА ДОМАШНІЙ ЕКСПЕРИМЕНТ 5 Очищення води кип’ятінням і за допомогою побутового фільтра Завдання. Проведіть очищення водопровідної та колодязної води. Що робили Спостереження Дія 1. Порцію води об’ємом 1 л прокип’ятили упродовж 20-30 хвилин у чистій посудині. Дали воді відстоятися й охолонути, обережно злили так, щоб на дні залишилась невелика кількість рідини. […]...
- Хімічна рівновага – Оборотність хімічних реакцій – Хімічна реакція ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 4. Хімічна реакція 4.9. Оборотність хімічних реакцій За цією ознакою розрізняють: – реакції, які за однакових умов відбуваються у двох протилежних напрямках, називають оборотними. Наприклад, реакція синтезу сульфур(VI) оксиду (знак вказує саме на оборотність реакції): – необоротними називають реакції, які відбуваються тільки в […]...
- Протолітична теорія кислот і основ – РОЗЧИНИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 5. РОЗЧИНИ. ТЕОРІЯ ЕЛЕКТРОЛІТИЧНОЇ ДИСОЦІАЦІЇ § 5.13. Протолітична теорія кислот і основ Теорія електролітичної дисоціації пояснила численні явища і процеси, що відбуваються у водних розчинах електролітів. Так, наприклад, у різних реакціях нейтралізації NaOH + НСl = NaCl + Н2O; КОН + […]...
- Хімічна рівновага РОЗДІЛ 1 ПОВТОРЕННЯ ТА ПОГЛИБЛЕННЯ ТЕОРЕТИЧНИХ ПИТАНЬ КУРСУ ХІМІЇ ОСНОВНОЇ ШКОЛИ § 14. Хімічна рівновага Усвідомлення змісту цього параграфа дає змогу: Пояснювати суть хімічної рівноваги й умови її зміщення, принцип Ле Шательє; Вміти розрізняти оборотні та необоротні реакції, записувати їх рівняння; Керувати хімічними процесами завдяки зміщенню хімічної рівноваги і зміні швидкості хімічних реакцій. Пригадайте, які […]...
- ОБОРОТНІ РЕАКЦІЇ – ЕЛЕКТРОЛІТИ Хімія – універсальний довідник ЕЛЕКТРОЛІТИ ОБОРОТНІ РЕАКЦІЇ Реакція дисоціації води, рівняння якої наведено у попередньому параграфі, протікає незначною мірою. З кожного мільярда молекул води в ній беруть участь лише дві, тому концентрація кожного з іонів, які утворюються, мізерно мала (10-7 моль/л). Коли кажуть, що вода – слабкий електроліт, то мають на увазі, що вона слабко […]...
- ХІМІЧНА РІВНОВАГА – ХІМІЯ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ Хімія – універсальний довідник ХІМІЯ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ ХІМІЧНА РІВНОВАГА Реакція окиснення діоксиду сульфуру – оборотна. Це означає, що через деякий час після початку реакції в системі встановлюється рівновага: швидкість утворення SО3 дорівнює Швидкості його розкладання на SO2 і O2: За високої температури переважно протікає реакція розкладу (рівновага зміщена вліво), і в рівноважній суміші вміст продукту […]...
- Рівновага тіла – Статика 5. Механіка 5.4. Статика 5.4.8. Рівновага тіла Рівновага тіла – це стан тіла, при якому геометрична сума прикладених до нього сил і геометрична сума моментів цих сил відносно будь-якої точки дорівнюють нулю....
- РІВНОВАГА ПРИРОДНА Екологія – охорона природи РІВНОВАГА ПРИРОДНА – первинна екол. рівновага, створена на основі балансу незмінних або мало змінених діяльністю людини компонентів, що формують середовище, і прир. процесів. Р. п. – одна з найважливіших ознак живих систем, здатність цих систем розвиватися з досягненням клімаксу в ході сукцесії, що є достовірним індикатором Р. п....
- М’ЯКІСТЬ ВОДИ Екологія – охорона природи М’ЯКІСТЬ ВОДИ – низький вміст у воді карбонатів кальцію та магнію. Протилежне до жорсткості води – значного вмісту цих речовин у воді....
- Дисоціація води. Водневий показник ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 6. Суміші речовин. Розчини 6.8. Дисоціація води. Водневий показник Хімічно чиста вода дуже слабо проводить електричний струм. Провідність зумовлена дисоціацією: За температури 25 °С ступінь дисоціації води а = 1,8 · 10-9. Оскільки 1 л води (1000 г) містить 55,56 моль речовини, концентрації […]...
- ІОННИЙ ОБМІН Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ХІМІЧНА РІВНОВАГА ІОННИЙ ОБМІН Іонний обмін – це процес, у результаті якого іони, які знаходяться у твердій речовині, обмінюються з іонами, що знаходяться в розчині. Цей процес грунтується на здатності деяких природних і штучних високомолекулярних сполук-іонітів обмінювати радикали, що входять до їхнього складу, на іони, які знаходяться в розчині. […]...
- Оборотні й необоротні реакції. Хімічна рівновага Тема 2 ХІМІЧНІ РЕАКЦІЇ Урок 25 Тема уроку. Оборотні й необоротні реакції. Хімічна рівновага Цілі уроку: формувати уявлення учнів про хімічну рівновагу; ознайомити з класифікацією реакцій на оборотні й необоротні; показати необхідність зсуву хімічної рівноваги; формувати уявлення про фактори, що впливають на зсув хімічної рівноваги. Тип уроку: вивчення нового матеріалу. Форми роботи: фронтальне опитування, самостійна […]...
- Будова молекули води. Водневий зв’язок між молекулами води ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 6. Суміші речовин. Розчини 6.4. Будова молекули води. Водневий зв’язок між молекулами води У молекулі води є два ковалентні полярні зв’язки між атомом Оксигену і двома атомами Гідрогену. Через велику різницю електронегативності Оксигену (3,5) і Гідрогену (2,2) електронні хмари зміщені в бік Оксигену, […]...