Головна ⇒ 📌Довідник с фізики ⇒ МАСА АТОМІВ І МОЛЕКУЛ
МАСА АТОМІВ І МОЛЕКУЛ
Фізика підготовка до ЗНО комплексне видання
МОЛЕКУЛЯРНА ФІЗИКА І ТЕРМОДИНАМІКА
1. ОСНОВИ МОЛЕКУЛЯРНО-КІНЕТИЧНОЇ ТЕОРІЇ
1.3. МАСА АТОМІВ І МОЛЕКУЛ
Маси атомів і молекул прийнято порівнювати з 1/12 маси атома ізотопу Карбону 126С.
Відносною молекулярною масою Мr називають відношення маси молекули mo до 1/12 маси атома Карбону m0с (атомної одиниці маси, а. о. м.):
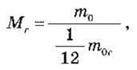
Де Мr – безрозмірна величина.
Маса молекули визначається за допомогою періодичної системи Менделєєва, де вказані відносні атомні маси речовин Мr.
Related posts:
- Відносна атомна маса, молекулярна маса, формульна маса ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 1. Основні хімічні поняття. Речовина 1.6. Відносна атомна маса, молекулярна маса, формульна маса Теоретична хімія має справу з атомами і молекулами, і вираження їхньої маси у грамах для розрахунків є незручним. Так, абсолютна маса атома Гідрогену становить 1,673 ·10-24 г, атома Сульфуру – […]...
- Відносна молекулярна маса Розділ 1 Початкові хімічні поняття 15 Відносна молекулярна маса Матеріал параграфа допоможе вам: > з’ясувати, що таке відносна молекулярна маса; > навчитись обчислювати відносні молекулярні маси. Маси молекул, як і атомів, надзвичайно малі. Тому в хімії використовують відносні маси молекул. Їх зазвичай називають відносними молекулярними масами. Відносна молекулярна маса – це відношення маси молекули до […]...
- МАСА АТОМА. АТОМНА ОДИНИЦЯ МАСИ. ВІДНОСНІ АТОМНІ МАСИ ХІМІЧНИХ ЕЛЕМЕНТІВ Тема 1 ПОЧАТКОВІ ХІМІЧНІ ПОНЯТТЯ & 11. МАСА АТОМА. АТОМНА ОДИНИЦЯ МАСИ. ВІДНОСНІ АТОМНІ МАСИ ХІМІЧНИХ ЕЛЕМЕНТІВ Вивчення параграфа допоможе вам: · розрізняти поняття “маса атома”, “атомна одиниця маси”, “відносна атомна маса хімічного елемента”; · порівнювати масу атомів. МАСА АТОМА. Як ваді відомо з попереднього параграфи, атоми мають вражаюче малі розміри. Відповідно й маса атомів […]...
- Відносна атомна маса ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 1. ОСНОВНІ ПОНЯТТЯ І ЗАКОНИ ХІМІЇ § 1.4. Відносна атомна маса Сучасні методи дослідження дають змогу визначити надзвичайно малі маси атомів з високою точністю. Наприклад, маса атома гідрогену становить 1,674 ∙ 10-27 кг, оксигену – 2,667 ∙ 10-26 кг, карбону – […]...
- Відносна атомна маса. Відносна молекулярна маса Контрольні запитання № 1. Відносна атомна маса – це відношення маси атома даного елемента до 1/12 маси атома Карбону. Відносна молекулярна маса М показує, у скільки разів маса молекули більша за 1/12 маси атома Карбону. Для речовин йонної будови хімічна формула відображає склад формульної одиниці. Тому для таких речовин використовують відносну формульну масу. № 2. […]...
- Атомна маса Хімія Загальна хімія Основні поняття, закони й теорії хімії Атомна маса Абсолютні значення мас атомів елементів – дуже малі величини, і користуватися ними незручно. Тому в розрахунках застосовують відносні значення мас атомів. Атомною одиницею маси (а. о. м.) називається 1/12 частина маси атома Карбону. Відносною атомною масою називається число, що показує, у скільки разів маса […]...
- § 11. МАСА АТОМА. АТОМНА ОДИНИЦЯ МАСИ, ВІДНОСНІ АТОМНІ МАСИ ХІМІЧНИХ ЕЛЕМЕНТІВ № 1. Атомна одиниця маси (а. о. м.) – маса 1/12 частини атома Карбону, ядро якого складається з 6 протонів і 6 нейтронів. № 2, 3. Число, яке одержують діленням маси атома конкретного хімічного елемента на атомну одиницю маси (приблизно на 1,662 • 10-27 кг) має назву відносна атомна маса хімічного елемента й позначається Аr. […]...
- Моль. Молярна маса ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 1. ОСНОВНІ ПОНЯТТЯ І ЗАКОНИ ХІМІЇ § 1.6. Моль. Молярна маса У Міжнародній системі одиниць (Сl) за одиницю кількості речовини прийнято моль. Моль – це кількість речовини, що містить стільки структурних одиниць (молекул, атомів, іонів, електронів чи інших), скільки атомів міститься […]...
- Маса атома. Відносна атомна маса Розділ 1 Початкові хімічні поняття 10 Маса атома. Відносна атомна маса Матеріал параграфа допоможе вам: > з’ясувати відмінність між масою атома і відносною атомною масою; > порівнювати маси атомів. Маса атома. Важливою характеристикою атома є його маса. Майже вся маса атома зосереджена в ядрі. Електрони мають настільки малу масу, що нею зазвичай нехтують. Зважувати атоми […]...
- Відносна молекулярна маса ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 1. ОСНОВНІ ПОНЯТТЯ І ЗАКОНИ ХІМІЇ § 1.5. Відносна молекулярна маса Відносною молекулярною масою Мr речовини називається величина, що дорівнює відношенню середньої маси молекули природного ізотопічного складу речовини до маси атома карбону 12С. Відносна молекулярна маса чисельно дорівнює сумі відносних атомних […]...
- ВІДНОСНА АТОМНА МАСА – ХІМІЧНИЙ ЕЛЕМЕНТ Хімія – універсальний довідник ХІМІЧНИЙ ЕЛЕМЕНТ ВІДНОСНА АТОМНА МАСА У даний час за атомну одиницю маси (а. о. м.) взято 1/12 частину маси атома Карбону, а саме його ізотопу 12С. Вона складає 1,66 – 10 -24 г. У хімії застосовується безрозмірна величина – відносна атомна маса. Її можна знайти, порівнюючи маси атомів елементів з 1 […]...
- МОЛЯРНА МАСА. КІЛЬКІСТЬ РЕЧОВИНИ Фізика підготовка до ЗНО комплексне видання МОЛЕКУЛЯРНА ФІЗИКА І ТЕРМОДИНАМІКА 1. ОСНОВИ МОЛЕКУЛЯРНО-КІНЕТИЧНОЇ ТЕОРІЇ 1.4. МОЛЯРНА МАСА. КІЛЬКІСТЬ РЕЧОВИНИ Один моль – кількість речовини, у якій міститься стільки ж молекул або атомів, скільки в Карбоні 126С масою 0,012 кг. Стала Авогадро (NА) – число атомів або молекул в 1 молі будь-якої речовини: Згідно із законом […]...
- ВІДНОСНА МОЛЕКУЛЯРНА МАСА. МАСОВА ЧАСТКА ЕЛЕМЕНТА В СКЛАДНІЙ РЕЧОВИНІ № 1. Відносну молекулярну масу також визначають на основі порівняння маси молекули з масою 1/12 частини атома Карбону, ядро якого містить шість протонів і шість нейтронів, тобто з атомною одиницею маси. Відносна молекулярна маса речовини показує, у скільки разів маса молекули більша за атомну одиницю маси. Як і відносна атомна маса, відносна молекулярна маса є […]...
- Маса і розміри молекул. Кількість речовини ВЛАСТИВОСТІ ГАЗІВ, РІДИН, ТВЕРДИХ ТІЛ* Урок № 4 Тема. Маса і розміри молекул. Кількість речовини Мета: конкретизувати положення про масу молекул, відносну молекулярну масу, кількість речовин, молярну масу, число Авогадро. Обладнання: періодична система елементів Менделєєва. План уроку 1. Визначення маси молекул та її розмірів. 2. Для чого ввели відносну атомну масу речовин. 3. Поняття кількості […]...
- РОЗМІРИ МОЛЕКУЛ І АТОМІВ Розділ 2. БУДОВА РЕЧОВИНИ §8 . АТОМИ ТА МОЛЕКУЛИ 3. РОЗМІРИ МОЛЕКУЛ І АТОМІВ ПРОВЕДЕМО ДОСЛІД Капнемо на поверхню спокійної води крапельку олії (краще взяти оливкову олію). Олія розтечеться по поверхні води дуже тонким шаром. Однак товщина олійної плівки не може бути меншою від розміру молекули олії, що й визначає максимальну площу плівки (рис. 8.7). […]...
- РУХ І ВЗАЄМОДІЯ АТОМІВ І МОЛЕКУЛ. ЗАЛЕЖНІСТЬ ШВИДКОСТІ РУХУ АТОМІВ І МОЛЕКУЛ ВІД ТЕМПЕРАТУРИ ТІЛА. ДИФУЗІЯ Мета: сформувати знання про безперервний хаотичний рух молекул та залежність швидкості руху від температури; сформувати експериментальні навички учнів; виховувати акуратність під час проведення експериментів, розвивати логічне мислення, вміння пояснювати фізичні явища та робити висновки з експерименту. Тип уроку: комбінований урок. Обладнання та наочність: обладнання лабораторної роботи, зошит із друкованою основою для виконання лабораторних робіт. Відеофрагмент: […]...
- Кількість речовини, молярна маса ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 1. Основні хімічні поняття. Речовина 1.7. Кількість речовини, молярна маса Кількість речовини п (або V, ню) – це фізична величина, яка визначає кількість частинок (молекул, атомів, йонів, йонних угруповань – асоціатів) у певній її порції. Одиницею вимірювання кількості речовини є моль. Моль – […]...
- МОДЕЛЬ ВІДШТОВХУВАННЯ ВАЛЕНТНИХ ЕЛЕКТРОННИХ ПАР ЦЕНТРАЛЬНОГО АТОМА – ПРОСТОРОВА КОНФІГУРАЦІЯ МОЛЕКУЛ Хімія – універсальний довідник БУДОВА РЕЧОВИНИ ПРОСТОРОВА КОНФІГУРАЦІЯ МОЛЕКУЛ МОДЕЛЬ ВІДШТОВХУВАННЯ ВАЛЕНТНИХ ЕЛЕКТРОННИХ ПАР ЦЕНТРАЛЬНОГО АТОМА Просторова конфігурація молекули визначається відштовхуванням електронних пар центрального атома: Просторове розташування чотирьох електронних пар умовно відповідає знаходженню їх у вершинах тетраедра (рис.9). Рис. 9. Міжелектронне відштовхування і структура молекул СН4, NН3, Н20. Тетраедричну конфігурацію має також іон амонію NH4+: […]...
- Валентність атомів – Здатність атомів утворювати сполуки ХІМІЧНИЙ ЗВ’ ЯЗОК 1.2 . Валентність атомів Якщо один атом з’єднується з іншим атомом, то залежно від виду атомів утворюються іони або молекули. – При утворенні іонного зв’язку валентні електрони приймаються або віддаються повністю. – При утворенні молекул валентні електрони йдуть на утворення спільних електронних пар. Число хімічних зв’язків за рахунок отриманих або відданих електронів, […]...
- Спектри випромінювання атомів і молекул 2-й семестр АТОМНА І ЯДЕРНА ФІЗИКА УРОК 2/79 Тема. Спектри випромінювання атомів і молекул Мета уроку: ознайомити учнів з лінійчастими й молекулярними спектрами випромінювання. Тип уроку: урок вивчення нового матеріалу. ПЛАН УРОКУ Контроль знань 4 хв. 1. Ядерна модель атома. 2. Недоліки ядерної моделі атома. 3. Квантові постулати Бора. Демонстрації 6 хв. Відео-фрагменти фільму “Спектральний […]...
- Відносні атомні маси хімічних елементів Тема 1 Початкові хімічні поняття & 7. Відносні атомні маси хімічних елементів Опанувавши цю тему, ви зможете: – розуміти кількісну характеристику атома; – розрізняти поняття “відносна атомна маса” і “маса атома”; – знати одиницю, щодо якої обчислюють відносні атомні маси елементів, а також першу класифікацію елементів на металічні й неметалічні; – уміти знаходити значення відносних […]...
- МАСА. ЦЕНТР МАСИ Фізика підготовка до ЗНО комплексне видання МЕХАНІКА 2. ОСНОВИ ДИНАМІКИ 2.1. ОСНОВНІ ЗАКОНИ ДИНАМІКИ. СИЛА. РІВНОДIЙНА СИЛА 2.1.4. МАСА. ЦЕНТР МАСИ Маса – фізична величина, яка кількісно характеризує інертні властивості тіла. Інертність полягає в тому, що для зміни швидкості руху тіла даною силою потрібен деякий час. Чим більшим є цей час, тим інертнішим є тіло. […]...
- Відносна молекулярна маса речовини. Масова частка елемента в складній речовині Тема 1 Початкові хімічні поняття & 12. Відносна молекулярна маса речовини. Масова частка елемента в складній речовині Опанувавши цю тему, ви зможете: – розуміти поняття “відносна молекулярна маса”, “масова частка елемента в складній речовині”; – уміти обмислювати відносну молекулярну масу за формулами речовин, масову частку елемента в складній речовині; – формувати навички в обчисленнях за […]...
- Хімічні формули речовин. Відносна молекулярна маса, її обчислення за хімічними формулами ТЕМА 1. ПОЧАТКОВІ ХІМІЧНІ ПОНЯТТЯ Урок 11. Хімічні формули речовин. Відносна молекулярна маса, її обчислення за хімічними формулами Цілі: на основі знань про хімічні формули речовин вивчити, що таке відносна молекулярна маса речовини; навчитись обчислювати відносну молекулярну масу речовини за її формулою; розвивати знання учнів про хімічну формулу й уміння нею користуватися; розвивати логічне мислення; […]...
- Відносна молекулярна маса речовини, її обчислення за хімічною формулою Тема 1 ПОЧАТКОВІ ХІМІЧНІ ПОНЯТТЯ Урок 15 Тема. Відносна молекулярна маса речовини, її обчислення за хімічною формулою Цілі: поглибити поняття про хімічну формулу, її використання для розрахунків; дати поняття про відносну молекулярну масу; формувати вміння й навички обчислювання за хімічними формулами; навчити визначати відносну молекулярну масу простих і складних речовин за їх формулами. Тип уроку: […]...
- Тема 1. Атомно-молекулярна будова речовини – ОСНОВНІ ПОНЯТТЯ, ЗАКОНИ І ЗАКОНОМІРНОСТІ В ХІМІЇ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА ІІ ЗАВДАННЯ ДЛЯ ПЕРЕВІРКИ ЗНАНЬ ОСНОВНІ ПОНЯТТЯ, ЗАКОНИ І ЗАКОНОМІРНОСТІ В ХІМІЇ Тема 1. Атомно-молекулярна будова речовини Серед чотирьох наведених варіантів відповідей виберіть одну правильну 1. Позначте визначення атома: A. Найменша частинка, що входить до складу молекули і зберігає її властивості; Б. Електронейтральна частинка речовини, що […]...
- Обчислення кількості атомів (молекул) у певній кількості речовини Тема 1 КІЛЬКІСТЬ РЕЧОВИНИ. РОЗРАХУНКИ ЗА ХІМІЧНИМИ ФОРМУЛАМИ УРОК 4 Тема. Обчислення кількості атомів (молекул) у певній кількості речовини Цілі уроку: формувати вміння і практичні навички хімічних обчислень з використанням понять “кількість речовини”, “моль”, “стала Авогадро”. Тип уроку: формування вмінь і навичок. Форми роботи: керована практика, самостійна робота. Обладнання: Періодична система хімічних елементів Д. І. […]...
- Атомна одиниця маси. Відносна атомна маса хімічних елементів Тема 1 ПОЧАТКОВІ ХІМІЧНІ ПОНЯТТЯ Урок 8 Тема. Атомна одиниця маси. Відносна атомна маса хімічних елементів Цілі уроку: розширити знання учнів про періодичну систему елементів; закріпити знання учнів про хімічний елемент, хімічну символіку; ознайомити учнів з поняттям абсолютної та відносної атомної маси, одиницею вимірювання відносної атомної маси – атомною одиницею маси (а. о. м.); навчити […]...
- ВІДНОСНА МОЛЕКУЛЯРНА МАСА. МАСОВА ЧАСТКА ЕЛЕМЕНТА В СКЛАДНІЙ РЕЧОВИНІ Тема 1 ПОЧАТКОВІ ХІМІЧНІ ПОНЯТТЯ & 16. ВІДНОСНА МОЛЕКУЛЯРНА МАСА. МАСОВА ЧАСТКА ЕЛЕМЕНТА В СКЛАДНІЙ РЕЧОВИНІ Вивчення параграфа допоможе вам: · обчислювати відносну молекулярну масу речовини за її формулою; · обчислювати масову частку елемента в складній речовині; · обчислювати відносну молекулярну масу сполуки за відомими масовими частками елементів Молекули, як і атоми, мають дуже малу […]...
- Вправа 106-114 № 106. Відносна молекулярна маса – це відношення маси молекули до 1/12 маси атома Карбону. Її позначають Мr. Її розраховують за хімічною формулою (б). Маса дорівнює сумі відносних мас атомів, які містяться в молекулі. № 107. Найменшу відносну масу має речовина водень: Мr(Н2) = 2 • Аr(Н) = 2 • 1 = 2. № 108. […]...