Обчислення кількості атомів (молекул) у певній кількості речовини
Тема 1
КІЛЬКІСТЬ РЕЧОВИНИ. РОЗРАХУНКИ ЗА ХІМІЧНИМИ ФОРМУЛАМИ
УРОК 4
Тема. Обчислення кількості атомів (молекул) у певній кількості речовини
Цілі уроку: формувати вміння і практичні навички хімічних обчислень з використанням понять “кількість речовини”, “моль”, “стала Авогадро”.
Тип уроку: формування вмінь і навичок.
Форми роботи: керована практика, самостійна робота.
Обладнання: Періодична система хімічних елементів Д. І. Менделєєва.
ХІД УРОКУ
I. Організація класу
II. Актуалізація опорних
1. Тестові завдання (на дошці)
1) Кількість речовини вимірюється в одиницях:
А) моль;
Б) метр;
В) літр.
2) Число частинок, що міститься у 2 моль:
А) 12,04 – 1023;
Б) 6,02 – 1023;
В) 3,01 – 1023.
3) В 1 моль вуглекислого газу СO2 міститься:
А) 1,67 – 1023 молекул;
Б) 44 молекули;
В) 6,02 – 1023 молекул.
2. Якою формулою виражається взаємозв’язок між кількістю речовини та сталою Авогадро?
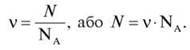
3. У чому полягає фізичний зміст “кількості речовини”?
III. Поглиблення знань, формування вмінь і навичок
Керована практика
Задача 1
Обчисліть кількість
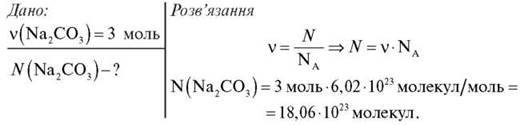
Відповідь: 18,06 – 1023 молекул.
Задача 2
Обчисліть кількість атомів Оксигену у 2 моль вуглекислого газу СO2.

2) Одна молекула СO2 містить два атоми Оксигену, отже
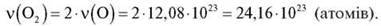
Відповідь: 24,16 – 1023 атомів.
Задача 3
Обчисліть кількість речовини сульфатної кислоти H2SO4 у зразку, що містить 3,01 – 1023 молекул.
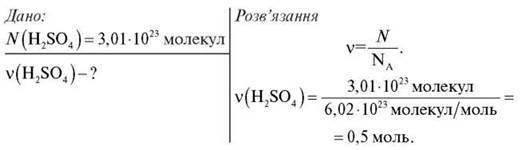
Відповідь: 0,5 моль.
IV. Самостійна робота під керівництвом учителя з картками
Завдання: обчисліть число молекул складної речовини й число атомів кожного хімічного елемента в заданій кількості речовини.
Варіант | Формула речовини | Кількість речовини | Число молекул | Число атомів | |
І | K2SO4 | 0,5 моль | К | S | О |
II | NaNO3 | 1,5 моль | Na | N | О |
III | Са(ОН)2 | 0,8 моль | Са | Са | Н |
IV | Н3РO4 | 2 моль | Н | Р | O |
Після виконання завдання виписуємо відповіді на дошці, коригуємо. Складаємо алгоритм розв’язання.
1. Обчислити число молекул складної речовини за формулою
N =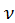 – Na.
– Na.
2. За хімічною формулою речовини визначити число атомів кожного елемента в молекулі складної речовини.
3. Обчислити кількість атомів хімічного елемента в заданій кількості речовини.
V. Керована практика. Розвивальне завдання
Обчисліть кількість речовини кисню, що прореагує без залишку із залізом кількістю речовини 2 моль із утворенням ферум(ІІІ) оксиду.
Для того щоб розв’язати задачу, згадаймо курс хімії 7 класу.
– Що показує рівняння хімічної реакції?
– Які речовини взаємодіють між собою (формули речовин).
– В якому співвідношенні ці речовини взаємодіють одна з одною (коефіцієнти в рівнянні реакції).
Правило. Кількість речовини будь-яких попарно взятих речовин у рівнянні реакції співвідносяться як їхні коефіцієнти в рівнянні реакції.
Розв’яжемо задачу.

3) За рівнянням хімічної реакції, 4 моль заліза реагують із 3 моль кисню:
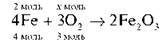
4) Складемо пропорцію:
2/4 = х/3;
4х = 6;
Х = 1,5.
Отже, 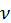 (O2) = 1,5 моль.
(O2) = 1,5 моль.
Відповідь: 1,5 моль кисню реагують із 2 моль заліза.
VI. Підбиття підсумків
VII. Домашнє завдання
Опрацювати відповідний параграф підручника, відповісти на питання.
Творче завдання. В якій кількості речовини ферум(ІІІ) оксиду міститься 18,06 – 1023 атомів Феруму? Скільки атомів Феруму міститься в такій же кількості речовини ферум(ІІ) оксиду?