Обчислення масової частки й маси речовини в розчині
Тема 1
РОЗЧИНИ
Урок 8
Тема уроку. Обчислення масової частки й маси речовини в розчині
Цілі уроку: закріпити знання про масову частку розчиненої речовини; формувати навички й уміння обчислювати масову частку розчиненої речовини, застосовувати ці знання для обчислення маси розчиненої речовини, приготування розчинів із заданою масовою часткою розчиненої речовини.
Тип уроку: застосування знань, умінь і навичок.
Форми роботи: розв’язання задач, індивідуальна і групова робота.
Обладнання: таблиця розчинності, картки-завдання.
ХІД
I. Організація класу
II. Перевірка домашнього завдання.
Актуалізація опорних знань
Перевіряємо таблицю, звіряємо відповіді, записуємо на дошці формули для обчислення.
III. Формування вмінь. Творче застосування знань, умінь і навичок
Задача 1
До розчину натрій сульфату масою 250 г з масовою часткою солі 15 % додали 50 г води. Обчисліть масову частку розчиненої речовини в новому розчині.
Дано:
M1(розч.) = 250 г
M(H2O) = 50 г
?1 = 15 %
?2 – ?
Розв’язання
Розчин | M(реч.) | M(розч.) | ?, % |
1 | 250 | 250 | 15 |
2 | 37,5 | 300 | 12,5 |
Задача 2
У розчині купрум(ІІ) сульфату масою 125 г з масовою часткою 20 % додатково розчинили 10 г купрум(ІІ) сульфату.
Розчин | ?, % | M(реч.) | M(розч.) |
1 | 20 | 125 – 0,2 = 25 | 125 |
2 | 26 | 35 | 135 |
Задача 3
Обчисліть масову частку розчину, одержаного в результаті зливання 25 г розчину сульфатної кислоти з масовою часткою 70 % і 40 г розчину сульфатної кислоти з масовою часткою 20 %.
Розв’язання
Спосіб 1
Розчин | ?, % | M(реч.) | M(розч.) |
1 | 70 | 70 – 0,25 = 17,5 | 25 |
2 | 20 | 45 – 0,2 = 9 | 45 |
3 | 37,8 | 26,5 | 70 |
Спосіб 2
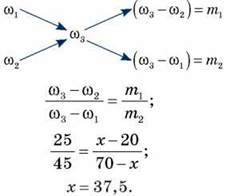
Відповідь: 37,5 %.
Задача 4
Обчисліть масову частку речовини в розчині, одержаному в результаті змішування 40 г розчину натрій хлориду з масовою часткою 15 % і 160 г розчину з масовою часткою речовини 20 %.
Розчин | ?, % | M(реч.) | M(розч.) |
1 | 15 | 40 – 0,15 = 6 г | 40 г |
2 | 20 | 160 – 0,2 = 32 г | 160 г |
3 | 19 | 38 г | 200 г |
Відповідь: 19 %.
Задача 5
У хімічних розрахунках широко використовується молярна концентрація – кількість розчиненої речовини в 1 л розчину.
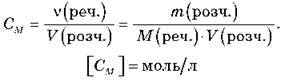
Обчисліть молярну концентрацію розчину сульфатної кислоти масою 225 г (? = 1,5 г/мл) з масовою часткою 52 %.
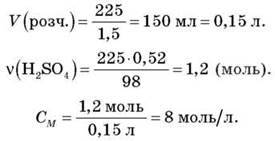
Відповідь: 8 моль/л.
Задача 6*
Молярна концентрація розчину натрій гідроксиду – 5 моль/л (? = 1,2 г/мл). Обчисліть масову частку речовини в розчині.
Розв’язання
1) m(NaOH) = 5 – 40 г/моль = 200 г.
2) m(розч.)= 1000/1,2 = 833 (г).
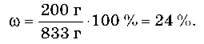
Відповідь: 24 %.
IV. Самостійна робота з картками
Обчисліть масу солі й води для приготування розчину масою:
Варіант І – 700 г з масовою часткою 17 %;
Варіант ІІ – 400 г з масовою часткою 24 %;
Варіант ІІІ – 600 г з масовою часткою 21 %.
V. Підбиття підсумків уроку, виставлення оцінок
VI. Домашнє завдання
Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи.
Творче завдання. Скласти завдання на розведення або змішування розчинів.