Основи – ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК
Хімія підготовка до ЗНО та ДПА
Комплексне видання
ЧАСТИНА І
ЗАГАЛЬНА ХІМІЯ
ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК
Основи
Поняття про основи, їхній склад та назви
Неорганічні основи ще називають гідроксидами, тому що вони складаються з двох частин: атомів металічних елементів та гідроксигруп Е(ОН)х. Наприклад, NaOH, Са(ОН)2, Аl(OН)3.
Основи – це складні речовини, які складаються з атома металічного елемента та однієї або кількох гідроксигруп.
З точки зору теорії кислот та основ Арреніуса основам можна дати таке визначення:
Гідроксигрупа одновалентна, тому число цих груп у складі основи дорівнює валентності металічного елемента. Назви гідроксидів складаються з двох слів: перше – назва металічного елемента, а друге слово “гідроксид”. Якщо металічний елемент може виявляти кілька валентностей, то в назві також указують його валентність римськими цифрами в дужках. Наприклад:
I
NaOH – натрій гідроксид;
II
Са(ОН)2 – кальцій гідроксид;
III
Аl(OН)3 – алюміній гідроксид;
IV
Ті(ОН)4 – титан(ІV) гідроксид.
Фізичні
На сьогодні відомі гідроксиди майже всіх металічних елементів. Властивості цих сполук значною мірою залежать від їхньої розчинності у воді, тому основи поділяють на дві групи – розчинні у воді, або луги, і нерозчинні у воді основи.
Луги – це тверді безбарвні речовини, без запаху, добре розчинні у воді, милкі на дотик. Розплави й розчини лугів проводять електричний струм. При розчиненні у воді лугів виділяється велика кількість теплоти, й розчин нагрівається. Тверді гідроксиди Натрію й Калію настільки гігроскопічні (поглинають газувату воду з повітря), що на повітрі розпливаються. На відміну від усіх лугів, кальцій гідроксид (гашене вапно) малорозчинний у воді. Його насичений розчин називають вапняною водою, а суспензію у воді – вапняним молоком.
Нерозчинні гідроксиди – тверді за звичайних умов речовини, без запаху, не проводять електричний струм, не притягаються магнітом і, звісно ж, не розчиняються у воді. Якщо нерозчинні гідроксиди добувають із розчинів, то вони випадають у вигляді драглистих осадів.
Гідроксиди Натрію та Калію при нагріванні плавляться й киплять без розкладання. Усі інші гідроксиди при нагріванні розкладаються на оксид металічного елемента та воду:
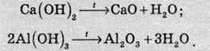
Гідроксиди (основи) | |
Розчинні у воді (луги) | Нерозчинні у воді |
LiOH, NaOH, КОН, RbOH, CsOH, Са(ОН)2, Sr(OH)2, Ва(ОН)2 | Аl(ОН)3, Fe(OH)2, Сr(ОН)3 тощо |
Виявлення основ
Так само, як і кислоти, луги можна виявити у водних розчинах за допомогою індикаторів. У присутності лугу лакмус набуває синього забарвлення, а метилоранж стає жовтим. Найкращим індикатором лугів є фенолфталеїн – у нейтральному середовищі (у чистій воді) та кислотному середовищі він безбарвний, а в присутності лугів набуває яскравого малинового кольору. Але нерозчинні гідроксиди забарвлення індикаторів не змінюють.
Забарвлення деяких індикаторів у кислотному, нейтральному та лужному середовищах
Індикатор | Забарвлення в розчині | ||
У кислотному середовищі | У нейтральному середовищі | У лужному середовищі | |
Лакмус | Червоний | Фіолетовий | Синій |
Метилоранж | Червоний | Жовтогарячий | Жовтий |
Фенолфталеїн | Безбарвний | Безбарвний | Малиновий |
Використання основ
На практиці здебільшого використовують тільки луги, у першу чергу натрій гідроксид та кальцій гідроксид. Кальцій гідроксид має технічну назву “гашене вапно”. Його використовують в основному в будівництві для виготовлення різних будівельних сумішей: штукатурки, шпаклівки тощо. Вапняним молоком (суспензією кальцій гідроксида у воді) навесні підбілюють низ стовбурів дерев, щоб застерегти від мурах. Також кальцій гідроксид використовують у цукровій промисловості, для виготовлення зубних паст. Натрій гідроксид використовують при виробництві мила, ліків, у шкіряній промисловості, для очищення нафти тощо.
Безпека під час роботи з основами
Луги є їдкими речовинами: вони роз’їдають шкіру, дерево, папір, можуть бути причиною серйозних опіків шкіри та слизових оболонок. Недарма натрій гідроксид називають їдким натром, а калій гідроксид – їдким калі. Вовняна тканина, занурена в концентрований розчин натрій гідроксиду, набухає й перетворюється в драглеподібну масу. Якщо розчин лугу, котрий потрапив на руку, не змити водою, шкіру починає щипати, і незабаром утворюється виразка. Працюючи з лугами, слід одягати захисні окуляри, оскільки потрапляння лугів у очі є вкрай небезпечним. Якщо луг випадково потрапив на шкіру, його треба негайно змити великою кількістю проточної води, а потім, у разі потреби, протерти ушкоджену ділянку шкіри слабким розчином боратної або оцтової кислоти.