Реакції в розчинах електролітів. Складання молекулярних і йонно-молекулярних рівнянь
ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання
РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ
6. Суміші речовин. Розчини
6.10. Реакції в розчинах електролітів. Складання молекулярних і йонно-молекулярних рівнянь
За нормальних умов тверді речовини зазвичай не вступають між собою в хімічні реакції. Хоч би один з реагентів повинен бути в газоподібному чи рідкому (розчиненому) стані. Отже, у хімії часто мають справу з реакціями між розчиненими у воді речовинами. Реакції між розчиненими електролітами – це реакції між окремими
– у результаті випадає осад (↓), тобто утворюється продукт реакції, який у воді не розчиняється або є малорозчинним;
– виділяється газ (↑), тобто утворюються леткі сполуки, або
– утворюється малодисоційована речовина (наприклад, вода).
Зауважимо, що при складанні йонно-молекулярних рівнянь добре розчинні сполуки записують у вигляді йонів, а слабкі електроліти, погано розчинні та леткі речовини (H2S, СО2, SО2) – у молекулярній формі:
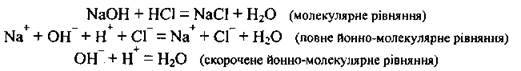
Розгляньмо найважливіші випадки
1. Реакції нейтралізації (взаємодія кислоти з основою):
– сильної кислоти із сильною основою:
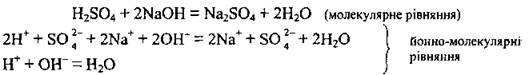
– слабкої кислоти із сильною основною (у цьому разі слабкі кислоти, а також кислоти, у яких ступінь дисоціації у розбавлених розчинах менше 50 %, пишуть у недисоційованій формі (це стосується таких кислот, как H2SО3, HNО2, HF, Н3РО4):
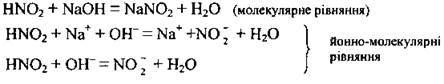
– слабкої основи із сильною кислотою:
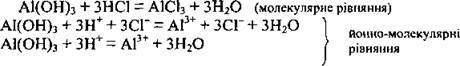
2. Реакції з утворенням летких речовин:

3. Реакції з утворенням малорозчинних солей, основ та амфотерних гідроксидів:
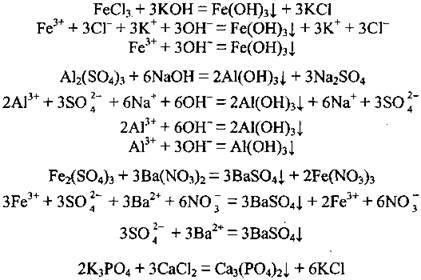
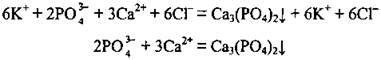
Related posts:
- РЕАКЦІЇ В РОЗЧИНАХ ЕЛЕКТРОЛІТІВ – ЕЛЕКТРОЛІТИ Хімія – універсальний довідник ЕЛЕКТРОЛІТИ РЕАКЦІЇ В РОЗЧИНАХ ЕЛЕКТРОЛІТІВ У розчинах електролітів у хімічну взаємодію вступають іони. З’ясуємо, у яких випадках це відбувається. Якщо змішати водні розчини кухонної солі (хлориду натрію) і вапняної води (розчину гідроксиду кальцію), то зовнішніх змін не спостерігається. Формально можна написати З огляду на те, що всі чотири речовини (хлорид і […]...
- Гідроліз солей як окремий випадок реакцій йонного обміну у водних розчинах електролітів ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 6. Суміші речовин. Розчини 6.11. Гідроліз солей як окремий випадок реакцій йонного обміну у водних розчинах електролітів У хімії часто стикаються з явищем гідролізу1 – хімічної взаємодії речовин з водою. Найбільше практичне значення має гідроліз солей. Гідроліз солей – це хімічна взаємодія солей […]...
- Практична робота № 2. Реакції іонного обміну в розчинах електролітів Тема 1 РОЗЧИНИ Урок 16 Тема уроку. Практична робота № 2. Реакції іонного обміну в розчинах електролітів Цілі уроку: перевірити вміння використовувати практичні знання про електролітичну дисоціацію, навички дослідження розчинів, складання іонних рівнянь; уміння спостерігати, робити висновки. Тип уроку: практичного застосування знань, умінь і навичок. Форми роботи: самостійна практична робота. Обладнання: таблиця розчинності, набір хімічних […]...
- Складання рівнянь окисно-відновних реакцій – ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 7. ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ § 7.3. Складання рівнянь окисно-відновних реакцій Застосовуються два методи складання рівнянь окисно – відновних реакцій – метод електронного балансу і метод напівреакцій. Метод електронного балансу. За цим методом порівнюють ступені окиснення атомів у вихідних і кінцевих речовинах, […]...
- Реакції іонного обміну – РОЗЧИНИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 5. РОЗЧИНИ. ТЕОРІЯ ЕЛЕКТРОЛІТИЧНОЇ ДИСОЦІАЦІЇ § 5.11. Реакції іонного обміну Згідно з теорією електролітичної дисоціації всі реакції у водних розчинах електролітів є реакціями між іонами. Вони називаються іонними реакціями, а рівняння цих реакцій – іонними рівняннями. Вони простіші, ніж рівняння реакцій, […]...
- Порядок реакції – Вираження швидкості реакції ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ 3. Вираження швидкості реакції 3.2 . Порядок реакції На основі теорії зіткнення для різних типів молекулярних реакцій можна записати вирази для швидкості реакції: Константа k – константа швидкості реакції. Через спільний вплив різних чинників на швидкість реакції результати експериментів часто не відповідають теоретичним припущенням. Тому певна реакція описується експериментально виведеним рівнянням (виразом) […]...
- Реакції обміну між розчинами електролітів, умови їх протікання Тема 1 РОЗЧИНИ УРОК 14 Тема уроку. Реакції обміну між розчинами електролітів, умови їх протікання Цілі уроку: показати процеси, що протікають у розчинах електролітів як реакції обміну між іонами; ознайомити з умовами їх протікання; формувати навички складання іонних рівнянь. Тип уроку: формування вмінь і навичок та їх творчого застосування. Форми роботи: розповідь учителя, демонстраційний експеримент, […]...
- РЕАКЦІЇ ОБМІНУ – ТИПИ ХІМІЧНИХ РЕАКЦІЙ Хімія – універсальний довідник ТИПИ ХІМІЧНИХ РЕАКЦІЙ РЕАКЦІЇ ОБМІНУ Реакції між складними хімічними речовинами, в результаті яких відбувається обмін між ними окремими атомами або групами атомів, називаються реакціями обміну. Наприклад: Реакції обміну (крім сильно екзотермічної реакції нейтралізації) зазвичай супроводжуються невеликим тепловим ефектом, тобто відбувається лише невелика зміна внутрішньої енергії системи, і вона не може бути […]...
- РЕАКЦІЇ ЗАМІЩЕННЯ – ТИПИ ХІМІЧНИХ РЕАКЦІЙ Хімія – універсальний довідник ТИПИ ХІМІЧНИХ РЕАКЦІЙ РЕАКЦІЇ ЗАМІЩЕННЯ Реакції між простою і складною речовиною, в результаті яких атоми простої речовини заміщають атоми одного з елементів складної речовини, називаються реакціями заміщення. Наприклад: Рушійною силою реакцій заміщення є утворення більш міцних сполук. З хімічної точки зору чим активніший хімічний елемент, тим міцніші сполуки він утворює, і […]...
- Електроліз водних розчинів електролітів – ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 7. ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ § 7.7. Електроліз водних розчинів електролітів Слід розрізняти електроліз розплавлених електролітів і їх розчинів. В останньому випадку в процесах можуть брати участь молекули води. Як приклад розглянемо електроліз концентрованого водного розчину хлориду натрію (електроди вугільні). В цьому […]...
- Механізм утворення естерів – Реакції естерифікації ОРГАНІЧНІ РЕАКЦІЇ 4. Реакції естерифікації Реакцію обміну спиртів з карбоновими кислотами називають реакцією естерифікації, при відщеплюванні води утворюються естери. Приклад. Із метанової (мурашиної) кислоти і метанолу утворюється метиловий естер метанової кислоти: Естерифікація оборотна (омилення) і веде до встановлення рівноваги між початковими речовинами і продуктами реакції. Механізм утворення естерів Оскільки дана реакція оборотна, то й усі […]...
- СКЛАДАННЯ РІВНЯНЬ ОКИСНО-ВІДНОВНИХ РЕАКЦІЙ З ВИКОРИСТАННЯМ СТУПЕНІВ ОКИСНЕННЯ ЕЛЕМЕНТІВ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС РЕАКЦІЇ ЗІ ЗМІНОЮ СТУПЕНІВ ОКИСНЕННЯ ЕЛЕМЕНТІВ СКЛАДАННЯ РІВНЯНЬ ОКИСНО-ВІДНОВНИХ РЕАКЦІЙ З ВИКОРИСТАННЯМ СТУПЕНІВ ОКИСНЕННЯ ЕЛЕМЕНТІВ Окисник – речовина, що містить елемент, у якого в ході реакції ступінь окиснення знижується внаслідок прийому електронів; процес приєднання електронів називається відновленням. Відновник – це речовина, що містить елемент, у якого в ході реакції […]...
- Молекулярність реакції – Вираження швидкості реакції ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ 3. Вираження швидкості реакції Згідно з теорією зіткнення, збільшення вдвічі кількості частинок реагенту в певному об’ємі веде до збільшення кількості зіткнень вдвічі і, відповідно, до збільшення швидкості реакції вдвічі. При збільшенні втричі концентрації частинок відбувається збільшення швидкості реакції втричі і т. д. 3.1 . Молекулярність реакції Реакції, в яких від початкових речовин […]...
- Структура молекулярних граток речовин – Ковалентний зв’язок – Типи хімічного зв’язку ХІМІЧНИЙ ЗВ’ ЯЗОК 2. Типи хімічного зв’язку 2.3. Ковалентний зв’язок Структура молекулярних граток речовин Молекулярні речовини утворюють у твердому агрегатному стані молекулярну гратку. На відміну від іонної гратки між молекулами в молекулярній решітці існують лише слабкі вандерваальсові зв’язки. Запам’ятайте: усі неметали, оксиди неметалів, безводні кислоти й органічні речовини у твердому стані утворюють молекулярну гратку. Через […]...
- Дисоціація кислот, основ і солей у водних розчинах – РОЗЧИНИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 5. РОЗЧИНИ. ТЕОРІЯ ЕЛЕКТРОЛІТИЧНОЇ ДИСОЦІАЦІЇ § 5.8. Дисоціація кислот, основ і солей у водних розчинах За допомогою теорії електролітичної дисоціації дають означення й описують властивості кислот, основ і солей. Кислотами називаються електроліти, під час дисоціації яких як катіони утворюються тільки катіони […]...
- Вільна енергія реакції Гіббса – Рушійна сила хімічних реакцій ЕНЕРГЕТИКА ХІМІЧНИХ РЕАКЦІЙ 3. Рушійна сила хімічних реакцій 3.4. Вільна енергія реакції Гіббса Кожна реакція характеризується двома тенденціями: – система речовин прагне перейти у стан з якомога меншою ентальпією; – система речовин прагне перейти в стан з якомога більшою ентропією. Тому реакція Проходить самочинно в той бік, де знижується ентальпія реакції і зростає її ентропія. […]...
- Класифікація хімічних реакцій – ХІМІЧНІ РЕАКЦІЇ ТА ЗАКОНОМІРНОСТІ ЇХ ПЕРЕБІГУ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЧНІ РЕАКЦІЇ ТА ЗАКОНОМІРНОСТІ ЇХ ПЕРЕБІГУ Класифікація хімічних реакцій Класифікація за числом та складом вихідних реагентів і продуктів реакції Реакція сполучення – реакція, внаслідок якої з кількох речовин з відносно простим складом утворюється одна велика речовина з більш складною структурою. А + В […]...
- Теорія електролітичної дисоціації. Іонні реакції I СЕМЕСТР ПОВТОРЕННЯ ОСНОВНИХ ПИТАНЬ КУРСУ ХІМІЇ ОСНОВНОЇ ШКОЛИ (4 год.) УРОК 3 Тема уроку. Теорія електролітичної дисоціації. Іонні реакції Цілі уроку: актуалізувати знання учнів про процеси, що протікають у розчинах; узагальнити знання про електролітичну дисоціацію речовин; удосконалювати вміння й навички складання повних і скорочених іонно-молекулярних рівнянь реакцій. Тип уроку: повторення й систематизації знань. Форми […]...
- Складні ефіри (естери). Реакції етерифікації та омилення – КИСНЕВМІСНІ ОРГАНІЧНІ СПОЛУКИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина III. ОРГАНІЧНА ХІМІЯ Розділ 17. КИСНЕВМІСНІ ОРГАНІЧНІ СПОЛУКИ § 17.13. Складні ефіри (естери). Реакції етерифікації та омилення Добування складних ефірів. При взаємодії карбонових кислот зі спиртами утворюються складні ефіри. Наприклад, з оцтової кислоти й етилового спирту за наявності каталізатора(концентрованої сірчаної або соляної кислоти) добувають складний […]...
- Реакції в гетерогенному і гомогенному середовищі ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ Більшість хімічних реакцій “миттєво” не відбуваються. Для реакції між початковими речовинами й утворенням продуктів потрібний певний час, який може бути дуже коротким. Запам’ятайте: реакції між Іонами відбуваються, як правило, набагато швидше, ніж реакції між молекулами. 1. Реакції в гетерогенному і гомогенному середовищі Реакції можуть відбуватися між речовинами в гетерогенному середовищі (наприклад, суміші […]...
- Класифікація окисно-відновних реакцій – ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 7. ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ § 7.5. Класифікація окисно-відновних реакцій Звичайно розрізняють три типи окисно-відновних реакцій: міжмолекулярні, внутрішньомолекулярні і реакції диспропорціонування. До міжмолекулярних належать реакції, у яких окисник і відновник входять до складу різних речовин. Розглянуті в §7.3 І 7.4 реакції належать […]...
- Швидкість хімічної реакції – Хімічні реакції Хімія Загальна хімія Хімічні реакції Швидкість хімічної реакції Швидкість хімічної реакції Визначається кількістю речовини, що прореагувала за одиницю часу в одиниці об’єму. Формула середньої швидкості хімічної реакції: де – середня швидкість хімічної реакції, – зміна концентрації реагенту, – час. Чинники, що впливають на швидкість хімічної реакції 1) Природа реагуючих речовин. 2) Агрегатний стан реагуючих речовин. […]...
- IОННО-ЕЛЕКТРОННИЙ МЕТОД СКЛАДАННЯ РІВНЯНЬ ОКИСНО-ВІДНОВНИХ РЕАКЦІЙ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС РЕАКЦІЇ ЗІ ЗМІНОЮ СТУПЕНІВ ОКИСНЕННЯ ЕЛЕМЕНТІВ IОННО-ЕЛЕКТРОННИЙ МЕТОД СКЛАДАННЯ РІВНЯНЬ ОКИСНО-ВІДНОВНИХ РЕАКЦІЙ Іонно-електронний метод – це метод напівреакцій. Наприклад: Кількість молів приєднаних електронів дорівнює кількості молів втрачених електронів:...
- Опис швидкості реакції – Швидкість реакції ШВИДКІСТЬ ХІМІЧНИХ РЕАКЦІЙ 2. Швидкість реакції 2.3 . Опис швидкості реакції Швидкість реакції можна описати як зміну концентрації початкової речовини і як зміну продукту реакції за певний проміжок часу. І в одному і в іншому випадку за певний проміжок часу вона визначається за кутом нахилу січної відповідного графіка с(t). В один і той самий проміжок […]...
- Ентропія реакції – Рушійна сила хімічних реакцій ЕНЕРГЕТИКА ХІМІЧНИХ РЕАКЦІЙ 3. Рушійна сила хімічних реакцій 3.3. Ентропія реакції У кожній реакції впорядкований стан системи змінюється і, отже, змінюється ентропія. Зміна ентропії реакції ∆SR, як і ентальпії реакції, визначається як різниця суми ентропій продуктів реакції і суми ентропій початкових речовин: Приклад. Під час реакції газоподібного гідроген хлориду з газоподібним амоніаком з двох “невпорядкованих” […]...
- Гідроліз солей РОЗДІЛ 1 ПОВТОРЕННЯ ТА ПОГЛИБЛЕННЯ ТЕОРЕТИЧНИХ ПИТАНЬ КУРСУ ХІМІЇ ОСНОВНОЇ ШКОЛИ § 13. Гідроліз солей Усвідомлення змісту цього параграфа дає змогу: Пояснювати поняття “гідроліз солей” і суть цього процесу; характеризувати різні випадки гідролізу; Вміти наводити приклади гідролізу і складати рівняння відповідних реакцій; Прогнозувати реакцію середовища та експериментально її визначати. Пригадайте, які речовини називаються солями та […]...
- ТЕПЛОВИЙ ЕФЕКТ РЕАКЦІЇ. ЕНТАЛЬПІЯ РЕАКЦІЇ – ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ ТЕПЛОВИЙ ЕФЕКТ РЕАКЦІЇ. ЕНТАЛЬПІЯ РЕАКЦІЇ Кількість теплоти Q, яку передали системі, йде на зміну її внутрішньої енергії ΔUі на здійснення системою роботи* W проти зовнішніх сил (зовнішнього тиску р) (рис. 32): Рис. 32. Робота, яку виконує хімічна система проти зовнішнього тиску (поршень невагомий). Вуглекислий газ, який […]...
- Тепловий ефект реакції. Екзотермічні й ендотермічні реакції. Термохімічні рівняння Тема 2 ХІМІЧНІ РЕАКЦІЇ Урок 24 Тема уроку. Тепловий ефект реакції. Екзотермічні й ендотермічні реакції. Термохімічні рівняння Цілі уроку: розширити уявлення про хімічні реакції на прикладі ендотермічних і екзотермічних реакцій; ознайомити учнів з поняттями “тепловий ефект хімічної реакції”, “термохімічні рівняння”; формувати навички й уміння складати термохімічні рівняння реакцій, розв’язувати задачі з їх використанням. Тип уроку: […]...
- Швидкість хімічної реакції – ХІМІЧНІ РЕАКЦІЇ ТА ЗАКОНОМІРНОСТІ ЇХ ПЕРЕБІГУ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ХІМІЧНІ РЕАКЦІЇ ТА ЗАКОНОМІРНОСТІ ЇХ ПЕРЕБІГУ Швидкість хімічної реакції Хімічні реакції відрізняються одна від одної тривалістю їхнього протікання. Деякі хімічні реакції відбуваються миттєво (наприклад, вибух воднево-кисневої суміші, реакції обміну з утворенням осаду), інші – досить швидко (горіння речовин), треті – повільно (більшість реакцій […]...
- ГІДРОЛІЗ СОЛЕЙ – ВУГЛЕЦЬ І ЙОГО СПОЛУКИ Хімія – універсальний довідник ВУГЛЕЦЬ І ЙОГО СПОЛУКИ ГІДРОЛІЗ СОЛЕЙ У нейтральних розчинах, тобто за відсутності кислот і лугів, у результаті дисоціації (дуже слабкої) води утворюються однакові кількості іонів Н+ і ОН-: Додавання до води кислоти збільшує концентрацію іонів Н+ і, зміщуючи рівновагу дисоціації води вліво, знижує концентрацію іонів ОН-. Отже, кислий розчин містить більше […]...