Реакції води з оксидами
Розділ 3 Вода
28 Реакції води з оксидами
Матеріал параграфа допоможе вам:
> дізнатися про деякі хімічні властивості води;
> з’ясувати, що таке гідроксиди;
> навчитися складати формули основ і кислот.
Вода виявляє достатню хімічну активність. Вона взаємодіє з багатьма речовинами – і простими, і складними, серед яких є й оксиди.
> Які сполуки називають оксидами? Наведіть формули і хімічні назви кількох оксидів.
Реакції води з оксидами металічних елементів. Під час деяких робіт на будівництві, присадибній
СаО + Н3О = Са(ОН)2.
Мал. 80. Гасіння вапна
Хімічна назва продукту реакції – кальцій гідроксид. Слово гідроксид є скороченням словосполучення гідрат оксиду2.
Гідроксиди – сполуки металічних елементів із загальною формулою М(ОН)n.
Літера М у наведеній формулі замінює символ металічного елемента.
Вода взаємодіє також з оксидами Натрію, Барію, кількох інших металічних елементів першої та другої груп
Реакція води з оксидом є реакцією сполучення.
1 Формулу води зазвичай записують останньою в кожній частиш хімічного рівняння.
2 Слово гідрат походить від грецького) hydor – вода.
Цікаво знати
Технічні назви натрій гідроксиду NaOН – їдкий натр, каустична сода (від грецького kaustikos – їдкий).
Складемо рівняння такої реакції за участю натрій оксиду Na2O. Щоб вивести формулу її продукту – натрій гідроксиду, “збираємо” усі атоми, наявні в формулах реагентів, і записуємо їх в одну формулу, причому спочатку – атоми металічного елемента (Натрію), потім – Оксигену і Гідрогену1:
Na2O + Н2О = [Na2O2Н2].
Отриману формулу спрощуємо, зменшивши індекси вдвічі, а двійку записуємо як коефіцієнт:
Na2O + Н3О = 2NaOH.
При складанні рівняння реакції води з барій оксидом ВаО виявимо, що однакові індекси у формулі гідроксиду будуть лише біля атомів Оксигену і Гідрогену. Ці атоми помістимо в дужки, за якими запишемо спільний індекс:
ВаО + Н2О = [ВаО2Н2] = Ва(ОН)2.
Барій гідроксид
Формули гідроксидів можна вивести й без запису хімічних рівнянь. Для цього використовують значення валентності металічного елемента і групи атомів ОН, або гідроксильної групи. Ви знаєте, що Натрій – одновалентний елемент. Гідроксильна група є складовою молекули води, у якій вона сполучена з одним атомом Гідрогену: 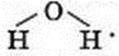 Отже, ця група атомів також одновалентна. (Валентність – властивість не лише атомів, а й груп сполучених атомів.) Звідси формула натрій гідроксиду – NaOH.
Отже, ця група атомів також одновалентна. (Валентність – властивість не лише атомів, а й груп сполучених атомів.) Звідси формула натрій гідроксиду – NaOH.
► Виведіть формулу магній гідроксиду.
Гідроксиди Натрію, Калію, Кальцію, Барію, багатьох інших металічних елементів об’єднують у велику групу сполук, загальна назва яких – основи.
1 Допоміжні хімічні записи поміщатимемо в квадратні дужки.
Цікаво знати
У промисловості, техніці використовують старі назви кислот – вугільна (Н2СО3), сірчана (Н2SO4), азотна (НNO3).
Більшість основ не розчиняється у воді, а відповідні оксиди з водою не взаємодіють. Нерозчинні основи добувають, здійснюючи інші реакції.
Для малорозчинних і розчинних у воді основ використовують спільну назву – луги. Серед цих сполук найбільшого практичного значення набули гідроксиди Натрію, Калію і Кальцію.
Реакції води з оксидами неметалічних елементів. Відомо, що вуглекислий газ здатний розчинятися у воді. У розчиненому етапі він міститься в мінеральній воді, газованих напоях. Незначна частина вуглекислого газу вступає в хімічну реакцію з водою:
СО2 + Н2О = Н2СО3.
Сполука, що утворюється при цьому, падає рідині кислуватого смаку. Її хімічна назва – карбонатна кислота; вона походить від назви “кислототворного” елемента Карбону.
Вода реагує майже з усіма оксидами неметалічних елементів (за винятком силіцій(ІV) оксиду SiO2 та декількох інших). Продуктами цих реакцій є кислоти.
Формулу продукту реакції води з оксидом неметалічного елемента можна скласти, “зібравши” разом усі атоми, наявні в формулах реагентів. Першими у формулі кислоти записують атоми Гідрогену, а останніми – атоми Оксигену:
SО3 + Н2О = H2SО4;
Сульфатна кислота
N2О5 + Н2О = [Н2N2O6] = 2HNO3.
Нітратна кислота
Розглянемо, як взаємодіє вода із фосфор(V) оксидом. Під час цієї реакції виділяється багато теплоти, і частила води швидко випаровується (мал. 81):

Мал. 81. Взаємодія води із фосфор(V) оксидом
P2O5 + Н2O = 2НРO3.
Метафосфатна кислота
Кислота, що утворюється, також реагує з водою:
НРO3 + Н2O = Н3РО4.
Ортофосфатна кислота
Відтак, у разі надлишку води взаємодія речовин відбувається згідно з рівнянням
Р2O5 + 3Н2O = 2Н3РО4.
Отже, оксиду Р2О5відповідають дві кислоти – НРО3 і Н3РО4.
Установити, який оксид відповідає певній кислоті, досить просто. Якщо молекула кислоти містить два атоми Гідрогену, із неї “вилучаємо” молекулу води:
Н2SО3 – Н2O => SO2.
У разі наявності в молекулі кислоти одного або трьох атомів Гідрогену виходимо із двох молекул сполуки:
2Н3ВО3 – 3Н3О => В2O3.
Цікаво знати
Оксиди СаО і Р2O5 завдяки їхній здатності активно взаємодіяти з водою використовують для осушування газів.
ВИСНОВКИ
Вода вступає в реакції сполучення з деякими оксидами металічних елементів і майже всіма оксидами неметалічних елементів.
Сполуки металічних елементів із загальною формулою М(ОН)n називають гідроксидами. Більшість цих сполук належить до
Основ. Розчинні і малорозчинні у воді основи називають лагами.
Під час реакцій води з оксидами нeметалічних елементів утворюються кислоти.
?
205. Які сполуки називають гідроксидами, основами, лугами?
206. Допишіть схеми реакцій і складіть хімічні рівняння:
А) Li2О + Н2О -> …;
SО2 + Н2О -> …;
Б) SrO + Н2О -> …;
L2О5 + Н2O -> … .
Укажіть серед продуктів реакцій основи та кислоти.
207. Яка формула оксиду, якщо продуктом його реакції з водою є:
А) магній гідроксид;
Б) калій гідроксид;
В) селенатна кислота H2SeO4;
Г) перхлоратна кислота НСlO4?
208. Знайдіть масові частки Оксигену: а) в оксиді Р2O5; б) у кислоті Н3РO4.
209. Яку масу натрій гідроксиду потрібно розчинити в 3 л води, щоб виготовити розчин із масовою часткою NaOH 0,2?
210. До 100 мл розчину нітратної кислоти з її масовою часткою 60 % (густина цього розчину – 1,37 г/мл) додали 200 мл води. Обчислiть масову частку кислоти в добутому розчині.