Рівняння Шредінгера
ФІЗИКА
Частина 5 АТОМНА ФІЗИКА
Розділ 16 ХВИЛЬОВІ ВЛАСТИВОСТІ РЕЧОВИНИ
16.3. Рівняння Шредінгера
У 1925 р., коли ідеї де Бройля ще не були підтверджені експериментально, Е. Шредінгер і В. Гейзенберг поклали в основу створеної ними квантової (хвильової) механіки уявлення про хвильові властивості частинок речовини. Тоді було опубліковано результати теоретичних досліджень Е. Шредінгера, В. Гейзенберга, М. Борна, П. Дірака, В. О. Фока, В. Паулі та ін.
Із підрозділу 16.2 відомо, що електрони поводять себе як хвилі, довжина яких визначається
Розглянемо дослід Дж. П. Томсона з дифракцією електронів, в якому через тонку металеву пластинку проходив вузький пучок електронів. При цьому на фотопластинці фіксувалась система дифракційних кілець. Почорніння пластинки в кожному місці визначалося інтенсивністю падаючої електронної хвилі. Очевидно, що почорніння пропорційне кількості електронів, які попадали в це місце пластинки. Для виявлення хвильових
Нехай нас цікавить ймовірність перебування електрона в певному об’ємі простору з координатами 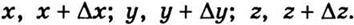 Ця ймовірність дорівнюватиме
Ця ймовірність дорівнюватиме 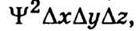 де ψ – амплітуда електронної хвилі. Отже, ψ2 є ймовірністю попадання електрона в певний об’єм простору. На противагу класичній квантова механіка не може точно показати траєкторію руху електрона. Можна лише визначити ймовірність знаходження електрона в певному місці простору в певний момент часу.
де ψ – амплітуда електронної хвилі. Отже, ψ2 є ймовірністю попадання електрона в певний об’єм простору. На противагу класичній квантова механіка не може точно показати траєкторію руху електрона. Можна лише визначити ймовірність знаходження електрона в певному місці простору в певний момент часу.
Амплітуда електронної хвилі ψ, що називається також хвильовою функцією, залежить від просторових координат і в загальному випадку від часу.
Отже, за аналогією з вектором 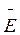 електромагнітної хвилі трактуватимемо ψ2dV, розраховану для об’єму dV, як величину, що визначає ймовірність перебування частинки в цьому об’ємі, а ймовірність знайти частинку будь-де в просторі
електромагнітної хвилі трактуватимемо ψ2dV, розраховану для об’єму dV, як величину, що визначає ймовірність перебування частинки в цьому об’ємі, а ймовірність знайти частинку будь-де в просторі 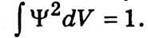 Це рівняння називають умовою нормування.
Це рівняння називають умовою нормування.
Для спрощення скористаємось стаціонарним рівнянням для амплітуди монохроматичної хвилі:
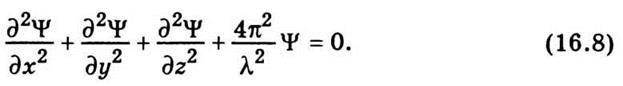
У це рівняння слід вкласти фізичні властивості тієї частинки, яку описує функція ψ. Зрозуміло, що для цього треба використати співвідношення, яке пов’язує хвильові й корпускулярні властивості частинок, тобто формулу де Бройля. Підставивши в (16.8) λ = h / р, дістанемо
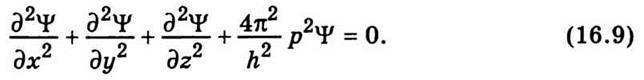
Ураховуючи, що кінетична енергія частинки W пов’язана з її імпульсом р співвідношенням 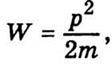 рівняння (16.9) можна переписати так:
рівняння (16.9) можна переписати так:
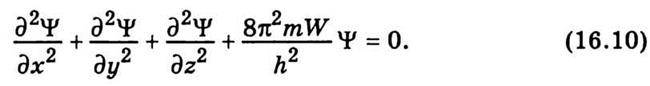
Проте цього рівняння досить лише для встановлення траєкторії частинки, що вільно рухається. Якщо ж на частинку діятимуть якісь зовнішні сили, то її поведінка визначатиметься тими самими полями, які діють на цю частинку. Повна енергія Е частинки, що рухається в силовому полі, є сумою кінетичної W і потенціальної U енергій: Е = W + U. При русі частинки в полі всі три величини Е, W і U будуть змінними. Скориставшись тим, що хвильове рівняння (16.10) містить кінетичну енергію W, після заміни W = Е – U остаточно дістанемо
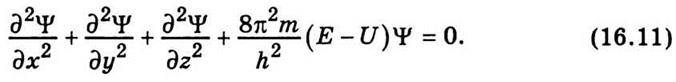
Це рівняння називають стаціонарним рівнянням Шредінгера. В такому вигляді воно справедливе лише для тих задач, коли потенціальна енергія U не залежить від часу, тобто U = =U (х, у, z). У загальному випадку слід ураховувати залежність хвильової функції ψ та потенціальної енергії U частинки від часу. Функція набуватиме того або іншого значення залежно від зовнішніх умов, в яких перебуває мікрочастинка. Ці зовнішні умови – сили, що діють на мікрочастинку, – в рівнянні (16.11) подані потенціальною функцією U(х, у, z). Константи h i m, що входять у рівняння Шредінгера, становлять собою сталу Планка і масу мікрочастинки. Проте рівняння (16.11) недостатньо для визначення функції ψ. Треба ще врахувати, що для цієї функції мають справджуватись деякі умови, що випливають з її фізичного змісту. Функція ψ характеризує ймовірність перебування мікрочастинки в певному елементі об’єму і через це має бути скінченною (ймовірність не може перевищувати одиницю), однозначною (ймовірність не може бути неоднозначною величиною) і неперервною (ймовірність не може змінюватися стрибкоподібно). До того ж амплітуда ψ у кожній точці простору є комплексним числом. Тому для обчислення ймовірності треба брати не ψ2, а квадрат модуля амплітуди |ψ|2.
Рівняння (16.11) справедливе лише для мікрочастинок, що рухаються зі швидкостями, малими порівняно із швидкістю світла, і має розв’язок для дискретного ряду значень повної енергії. Якщо рівняння (16.11) застосувати до задачі атома гідрогену, підставивши в нього замість U кулонівську енергію взаємодії електрона і ядра, то воно матиме скінченні й однозначні розв’язки тільки за таких значень повної енергії, які дістають для стаціонарних станів за теорією Бора. Отже, рівняння Шредінгера за своїми математичними властивостями вже містить у собі умови квантування, які в теорії Бора доводилось постулювати.
Отже, хвильова функція ψ – основна характеристика стану мікрооб’єктів, які вивчає квантова механіка. Вона задовольняє рівняння Шредінгера, яке є основним рівнянням квантової механіки. За своїм значенням рівняння Шредінгера в квантовій механіці аналогічне другому закону Ньютона – основному закону класичної механіки. Подібно до того як у класичній механіці за допомогою другого закону Ньютона розв’язують задачі, пов’язані з рухом макротіл, так у квантовій механіці за допомогою рівняння Шредінгера розв’язують задачі, пов’язані з рухом мікрооб’єктів. Так само як рівняння Ньютона для руху макротіл, рівняння Шредінгера для мікрочастинок не виводиться, а постулюється.