Складання найпростіших окисно-відновних реакцій, підбір коефіцієнтів
Тема 2
ХІМІЧНІ РЕАКЦІЇ
Урок 28
Тема уроку. Складання найпростіших окисно-відновних реакцій, підбір коефіцієнтів
Цілі уроку: розвивати навички складання окисно-відновних реакцій; закріпити навички складання хімічних рівнянь на прикладі найпростіших окисно-відновних реакцій, застосування методу електронного балансу для розміщення коефіцієнтів у рівняннях хімічних реакцій, що протікають зі зміною ступеня окиснення.
Тип уроку: узагальнення й систематизації знань, умінь і навичок.
Форми роботи: виконання тренувальних
Обладнання: періодична система хімічних елементів Д. І. Менделєєва, таблиця розчинності, картки-завдання.
ХІД УРОКУ
I. Організація класу
II. Перевірка домашнього завдання.
Актуалізація опорних знань
Перевіряємо домашнє завдання, коментуємо помилки.
III. Самостійна робота за індивідуальними завданнями
Учні отримують індивідуальне завдання – рівняння на картці, виконують його під керівництвом учителя. Через 3-5 хв. учні, які виконали завдання, обмінюються картками й виконують наступне завдання. Учитель регулює рівень завдань відповідно до рівня навчальних досягнень
Завдання 1. Розставте коефіцієнти в рівняннях реакцій методом електронного балансу, укажіть окисники й відновники:
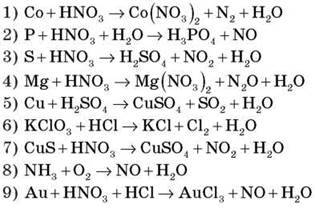
IV. Виконання тренувальних вправ (практика на прикладах)
Завдання 2. Запишіть у іонній формі рівняння ОВР, записані на дошці.
Для виконання наступного завдання учні об’єднуються в малі групи. Для наступної перевірки завдання в групах повторюються.
Завдання 3
1) Запишіть рівняння реакцій для здійснення перетворень, укажіть серед них рівняння ОВР.
2) Запишіть для них електронний баланс, укажіть окисник і відновник.
3) Запишіть рівняння 2 і 3 в іонній формі.
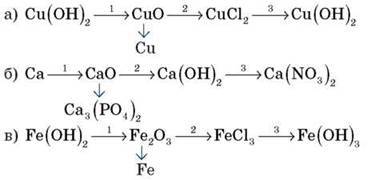
Завдання 4. Обчисліть об’єм водню, що виділиться в результаті взаємодії:
А) 8,6 г натрію з водою;
Б) 0,48 моль алюмінію із сульфатною кислотою;
В) 20 г сплаву цинку зі сріблом із хлоридною кислотою (масова частка срібла в сплаві – 12 %).
Завдання 5*. Обчисліть масу розчинів нітратної та хлоридної кислот, яку необхідно взяти для розчинення 10 г золота. Масова частка концентрованої нітратної кислоти – 63 %, хлоридної кислоти – 35 %.
V. Домашнє завдання
Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи.
Творче завдання. Підготувати розповідь про значення окисно-відновних реакцій у життєдіяльності людини.